Foram encontradas 120 questões.
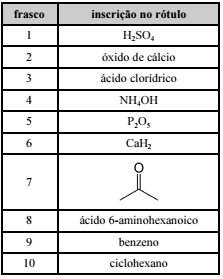
Apesar de apresentarem nomes distintos, os frascos 9 e 10 contêm os mesmos compostos.
Provas
Considerando-se que a constante do produto de solubilidade do cloreto de prata em água seja 1,0×10-10 mol/L, em uma solução saturada desse sal a concentração de íons prata será superior a 5,0 mg/L.
Provas

O pH de uma solução obtida pela mistura de 50 mL de NaOH 0,1 mol/L e 50 mL de HCl 0,25 mol/L é inferior a 2.
Provas

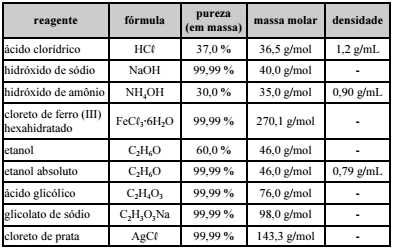
A tabela acima apresenta reagentes utilizados para o preparo de algumas soluções. Com base nessas informações, julgue o item a seguir.
Para se preparar 1,0 L de uma solução aquosa 0,1 mol/L de Fe3+ são necessários 10,8 g do reagente FeCl 3·6H2O.
Provas

Em 500 mL de uma solução de NaOH 0,2 mol/L, a massa de NaOH contida é maior que 5,0 g.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais

A mistura de 100 mL de etanol a 60,0 % com 100 mL de etanol absoluto produz uma solução final de concentração superior a 75,0 % em massa.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Considere as situações I e II a seguir. I.
A figura abaixo representa a curva de titulação obtida pela titulação de 50 mL de uma solução de um ácido fraco monoprótico com NaOH 0,1 mol/L, bem como a primeira derivada dessa curva.
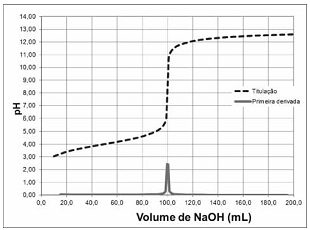
II. Na titulação de 20 mL de uma solução de Fe2+, foram gastos 5 mL de uma solução de dicromato 0,01 mol/L para que houvesse mudança de cor do indicador. Nesse caso, o Fe2+ foi completamente oxidado a Fe3+ e o Cr2O7 2- foi reduzido a Cr3+.
Na situação I, a concentração do ácido titulado é o dobro da concentração da base utilizada nessa titulação.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Considere as situações I e II a seguir. I.
A figura abaixo representa a curva de titulação obtida pela titulação de 50 mL de uma solução de um ácido fraco monoprótico com NaOH 0,1 mol/L, bem como a primeira derivada dessa curva.

II. Na titulação de 20 mL de uma solução de Fe2+, foram gastos 5 mL de uma solução de dicromato 0,01 mol/L para que houvesse mudança de cor do indicador. Nesse caso, o Fe2+ foi completamente oxidado a Fe3+ e o Cr2O7 2- foi reduzido a Cr3+.
O ácido titulado na situação I é mais forte que o ácido propiônico, que tem pK a = 4,9.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Considere as situações I e II a seguir. I.
A figura abaixo representa a curva de titulação obtida pela titulação de 50 mL de uma solução de um ácido fraco monoprótico com NaOH 0,1 mol/L, bem como a primeira derivada dessa curva.

II. Na titulação de 20 mL de uma solução de Fe2+, foram gastos 5 mL de uma solução de dicromato 0,01 mol/L para que houvesse mudança de cor do indicador. Nesse caso, o Fe2+ foi completamente oxidado a Fe3+ e o Cr2O7 2- foi reduzido a Cr3+.
Na situação II, a concentração de Fe2+ na amostra é superior a 0,010 mol/L.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Considere as situações I e II a seguir. I.
A figura abaixo representa a curva de titulação obtida pela titulação de 50 mL de uma solução de um ácido fraco monoprótico com NaOH 0,1 mol/L, bem como a primeira derivada dessa curva.

II. Na titulação de 20 mL de uma solução de Fe2+, foram gastos 5 mL de uma solução de dicromato 0,01 mol/L para que houvesse mudança de cor do indicador. Nesse caso, o Fe2+ foi completamente oxidado a Fe3+ e o Cr2O7 2- foi reduzido a Cr3+.
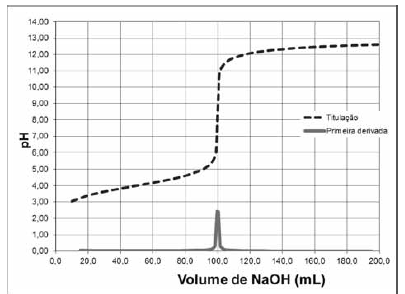
II. Na titulação de 20 mL de uma solução de Fe2+, foram gastos 5 mL de uma solução de dicromato 0,01 mol/L para que houvesse mudança de cor do indicador. Nesse caso, o Fe2+ foi completamente oxidado a Fe3+ e o Cr2O7 2G foi reduzido a Cr3+.
Com base nas situações apresentadas acima, julgue o item a seguir, relativos à química analítica clássica.
Diferentemente da volumetria de neutralização, a volumetria
de oxirredução é limitada pela impossibilidade de se utilizar
indicadores que acusem o final da titulação por meio da
mudança de cor do sistema.
Provas
Caderno Container