Foram encontradas 120 questões.
Acerca de ligações químicas e estruturas moleculares, julgue o item seguinte.
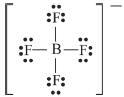
A estrutura de Lewis para o íon tetrafluoroborato (BF4−) é a mostrada a seguir.
Provas
Acerca de ligações químicas e estruturas moleculares, julgue o item seguinte.
O físico-químico Gilbert Newton Lewis propôs a regra do octeto.
Provas
Acerca de ligações químicas e estruturas moleculares, julgue o item seguinte.
O modelo da repulsão dos pares de elétrons da camada de valência aplicado à molécula SF4 leva à conclusão de que sua estrutura molecular é piramidal quadrática.
Provas
Acerca de ligações químicas e estruturas moleculares, julgue o item seguinte.
O físico-químico Gilbert Newton Lewis explicou o modelo das ligações químicas.
Provas
No que se refere aos fundamentos dos métodos espectroscópicos de análise, julgue o próximo item.
A maioria dos compostos aromáticos não heterocíclicos não substituídos apresentam rendimentos quânticos de fluorescência elevados o suficiente para uma análise bem sucedida por espectroscopia de fluorescência. Moléculas com sistemas de vários anéis aromáticos e com estruturas planares rígidas costumam apresentar alta fluorescência.
Provas
No que se refere aos fundamentos dos métodos espectroscópicos de análise, julgue o próximo item.
As bandas de absorção são normalmente muito mais amplas nos espectro de UV-VIS que nos de infravermelho (IV).
Provas
No que se refere aos fundamentos dos métodos espectroscópicos de análise, julgue o próximo item.
Vários tipos de transições entre níveis de energia quantizados dão origem aos espectros moleculares de UV-VIS, entre as quais se destacam as transições n → π* e π → π*, porque envolvem grupos funcionais característicos das substâncias e comprimentos de onda que são facilmente acessíveis.
Provas
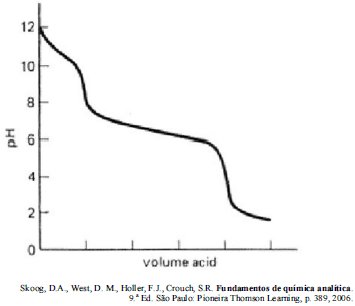
A figura anterior mostra a curva de titulação de uma amostra que pode conter NaOH, Na2CO3 e NaHCO3, em quaisquer proporções, em que o titulante é HCl 0,100 mol/L.
|
indicador |
intervalo do viragem (pH) |
|
azul de timol |
1,2 – 2,8 |
|
alaranjado de metila |
3,1 – 4,4 |
|
púrpura de bromocresol |
5,2 – 6,8 |
|
fenolftaleína |
8,3 – 10,0 |
Com relação a essa situação hipotética e considerando os intervalos de viragem de alguns indicadores, informados na tabela precedente, julgue o item subsequente.
Se a curva de titulação tivesse apenas um ponto de inflexão negativa, então seria correto concluir que a amostra conteria apenas NaOH.
Provas

A figura anterior mostra a curva de titulação de uma amostra que pode conter NaOH, Na2CO3 e NaHCO3, em quaisquer proporções, em que o titulante é HCl 0,100 mol/L.
|
indicador |
intervalo do viragem (pH) |
|
azul de timol |
1,2 – 2,8 |
|
alaranjado de metila |
3,1 – 4,4 |
|
púrpura de bromocresol |
5,2 – 6,8 |
|
fenolftaleína |
8,3 – 10,0 |
Com relação a essa situação hipotética e considerando os intervalos de viragem de alguns indicadores, informados na tabela precedente, julgue o item subsequente.
Ácidos fracos podem ser determinados por titulometria de neutralização, mas não os ânions deles derivados.
Provas

A figura anterior mostra a curva de titulação de uma amostra que pode conter NaOH, Na2CO3 e NaHCO3, em quaisquer proporções, em que o titulante é HCl 0,100 mol/L.
|
indicador |
intervalo do viragem (pH) |
|
azul de timol |
1,2 – 2,8 |
|
alaranjado de metila |
3,1 – 4,4 |
|
púrpura de bromocresol |
5,2 – 6,8 |
|
fenolftaleína |
8,3 – 10,0 |
Com relação a essa situação hipotética e considerando os intervalos de viragem de alguns indicadores, informados na tabela precedente, julgue o item subsequente.
É adequado utilizar púrpura de bromocresol e azul de timol como indicadores, do primeiro e do segundo pontos de equivalência, respectivamente.
Provas
Caderno Container