Foram encontradas 40 questões.
Os efluentes de laboratório que contêm metais pesados não devem ser lançados no esgotamento sanitário, sendo recomendável a sua precipitação como parte do tratamento. O sulfeto de mercúrio (II), por exemplo, é solúvel em água na concentração de 10−5 g/L a 25 ºC. O seu produto de solubilidade, KPS, será da ordem de:
Provas
Alguns fatores são importantes para a seleção da fase móvel que será usada em uma separação por cromatografia líquida de alta eficiência. Nesse contexto, é CORRETO afirmar:
Provas
Uma solução contendo 2,0 g de um composto clorado foi tratada com 50 mL de solução de nitrato de prata 0,1 mol/L, com precipitação de cloreto de prata. A prata remanescente em solução foi titulada com tiocianato de potássio 0,05 mol/L, gastando-se 10 mL até o ponto final. Sendo a massa molar da substância analisada de 285,5 g/mol, a pureza do produto analisado é de:
Provas
O soro fisiológico consiste numa solução de cloreto de sódio 0,5%. Considerando que a densidade do soro fisiológico é de 1,0 g/cm3, sua concentração molar é:
Provas
O esquema a seguir representa a eletrólise ígnea de cloreto de potássio, com eletrodos de grafite.
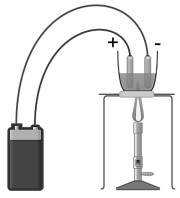
Acerca do processo citado, assinale a alternativa CORRETA:
Provas
Considere as reações descritas nas equações I a V:
I. !$ S !$8 + 12 !$ O !$2 → 8 !$ S !$!$ O !$3
II. 2 !$ K !$!$ M !$!$ n !$!$ O !$4 + !$ H !$2!$ O !$2 → 2 !$ K !$!$ O !$!$ H !$ + 2 !$ M !$!$ n !$!$ O !$2 + 2 !$ O !$2
III. !$ C !$!$ a !$!$ C !$!$ O !$3 → !$ C !$!$ a !$!$ O !$ + !$ C !$!$ O !$2
IV. 2 !$ I !$!$ C !$!$ l !$ + !$ B !$!$ r !$2 → 2 !$ I !$!$ B !$!$ r !$ + !$ C !$!$ l !$2
V. !$ K !$!$ C !$!$ l !$!$ O !$3 + !$ M !$!$ n !$!$ O !$2 → !$ K !$!$ O !$2 + !$ M !$!$ n !$!$ C !$!$ l !$!$ O !$3
As reações anteriores podem ser descritas, respectivamente, como:
Provas
A figura a seguir representa um esquema para a produção de gás cloro em escala laboratorial.
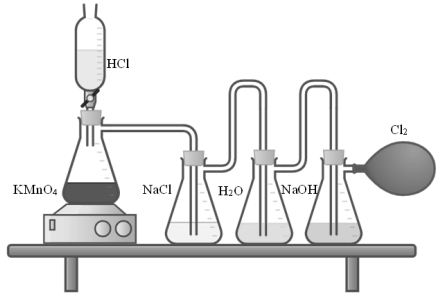
A reação que descreve o processo é:
!$ K !$!$ M !$!$ n !$!$ O !$4 + !$ H !$!$ C !$!$ l !$ → !$ K !$!$ C !$!$ l !$ + !$ M !$!$ n !$!$ C !$!$ l !$2 + !$ H !$2!$ O !$ + !$ C !$!$ l !$2
Admitindo-se que o processo é realizado nas condições normais de temperatura e pressão, e que o gás cloro se comporte como gás ideal, quais quantidades de reagentes devem ser utilizadas para a obtenção de 1,4 L de gás cloro?
Provas
A separação de cadeias polipeptídicas pode ser realizada por eletroforese em gel, utilizando-se um tampão, que mantém as condições para a passagem da corrente e manutenção do valor de pH do sistema. Para produzir um tampão de pH 8,8, deve-se utilizar uma base cujo ácido conjugado tenha o pKa de:
Provas
A reação de oxidação do ácido sulfídrico pelo permanganato de potássio, na presença de ácido sulfúrico, produz sulfato de potássio, sulfato de manganês (II), água e enxofre. Caso uma amostra de 500 g contenha 3,4 % de ácido sulfídrico, a quantidade de enxofre produzida será de:
Provas
Um determinado contaminante será analisado por espectrofotometria. Para construir a curva padrão, foram determinadas as absorbâncias de soluções com as seguintes concentrações do contaminante:
Concentração (mol/L) | Absorbância (A) |
0,10 | 0,0025 |
0,20 | 0,0055 |
0,30 | 0,0081 |
0,40 | 0,0105 |
Uma técnica de laboratório determinou a equação da reta (A em função da concentração), em seguida mediu a absorbância de uma amostra de água contaminada, encontrando 0,0136. Dessa forma, pode-se concluir que a concentração do contaminante na amostra de água é:
Provas
Caderno Container