Foram encontradas 50 questões.
Outra análise importante que deve ser feita ao se propor a utilização de um novo combustível é determinar seu poder calorífico, ou seja, a quantidade de energia liberada pela sua queima. Como a queima ocorre em temperaturas elevadas, uma correção do poder calorífico com a temperatura pode ser necessária. Assinale a alternativa que indica o poder calorífico da combustão da amônia, produzindo monóxido de nitrogênio, segundo a equação não balanceada, que ocorre a 1025 ºC:

Provas
Atualmente, há várias pesquisas que buscam combustíveis alternativos para os combustíveis baseados no carbono, com o objetivo de reduzir as emissões de dióxido de carbono (CO2). Uma dessas possibilidades é usar a amônia como combustível, já que sua combustão não emite CO2. Porém, a combustão da amônia pode produzir óxidos de nitrogênio que são poluentes atmosféricos importantes, assim, deve-se olhar com cautela essa alternativa. Assinale a alternativa que indica o volume de ar, contendo 21% (v/v) de oxigênio, necessário para produzir 500 L de dióxido de nitrogênio, a 1027 ºC e 1,3 atm, durante a combustão da amônia, produzindo dióxido de nitrogênio, segundo a equação não balanceada:
NH3(g) + O2(g) → NO2(g) + H2O(g)
Provas
O conhecimento da geometria das espécies químicas permite estimar propriedades físicas e prever como cada espécie interage com outras. Qual é a alternativa que apresenta a geometria de cada espécie química a seguir, RESPECTIVAMENTE?
I. BrF3
II. ClF5
III. I3–
IV. H2Te
V. BrF4–
Provas
O iodo pode ser utilizado para fazer experimentos simples em laboratório que permitem analisar fenômenos físicos e químicos. Um desses experimentos consiste em aquecer ligeiramente cristais de iodo sólido num tubo de ensaio para se observar a formação de um vapor violeta. Uma outra possibilidade de experimento é colocar cristais de iodo num tubo de ensaio com água destilada à temperatura ambiente e observar que a solubilidade do iodo é pequena. Em seguida, acrescentando-se uma pequena quantidade de iodeto de potássio ao tubo com agitação, percebe-se que o sólido se dissolve totalmente.
Analise as afirmações a seguir, relacionadas aos experimentos descritos anteriormente, e marque a alternativa INCORRETA:
Provas
Recentemente, uma carga com material radioativo foi roubada em São Paulo e, felizmente, recuperada sem maiores problemas. Um dos elementos radioativos contidos nessa carga era um isótopo do germânio (\( G \)\( e \)) utilizado em exames na medicina nuclear. Sabendo que o ![]() é um emissor de pósitrons, seu decaimento radioativo gera:
é um emissor de pósitrons, seu decaimento radioativo gera:
Provas
A figura a seguir apresenta a redução na energia de ativação de uma reação devido à utilização de um catalisador.

Figura 2 – Energia em função do caminho da reação.
Utilizando a Lei de Arrhenius, calcule a razão entre as constantes de velocidade da reação com catalisador (k2) e sem catalisador (k1), a 27 ºC e 1 atm. A alternativa que apresenta essa razão é:
Dado: R = 8,314 J/mol.K
Provas
O azeite de oliva extravirgem possui ácidos graxos monoinsaturados, vitaminas e antioxidantes naturais, sendo um dos componentes da “dieta mediterrânea” considerada uma das mais saudáveis do mundo. Os principais antioxidantes são compostos fenólicos que, segundo a Agência Europeia para a Segurança Alimentar, devem existir na concentração de 250 ppm para que um azeite seja de primeira qualidade. Considerando um consumo diário de 30 mL de azeite extravirgem de ótima qualidade, calcule a massa de compostos fenólicos ingeridos. A alternativa que apresenta o valor obtido, aproximadamente, é:
Dado: densidade azeite = 0,920 g/mL
Provas
Algumas pesquisas sobre fusão nuclear utilizam um equipamento denominado Tokamak. Nesse equipamento, campos magnéticos são usados para confinar plasma a altíssimas temperaturas, por isso os Tokamaks são feitos com materiais de elevado ponto de fusão.
O tungstênio pode ser utilizado nos Tokamaks por ser o metal com maior ponto de fusão. É possível se obter tungstênio metálico a partir do mineral scheelita (CaWO4) através da sequência de reações não balanceadas:
CaWO4 + HCl → CaCl2 + H2WO4
H2WO4 → H2O + WO3
WO3 + C → CO2 + W
Calcule a massa de scheelita necessária para se obter 183,84 kg de tungstênio num processo com 80% de rendimento. A alternativa que apresenta o valor obtido, aproximadamente, é:
Provas
O trítio (3H) é um isótopo do hidrogênio utilizado nas pesquisas sobre fusão nuclear, um possível método de obtenção de energia que tem sido alvo de intensas pesquisas. O 3H é radioativo e sofre decaimento de primeira ordem. A figura a seguir apresenta resultados do decaimento de 1,00 g de trítio com o passar do tempo:
Dado: ln 2 = 0,693
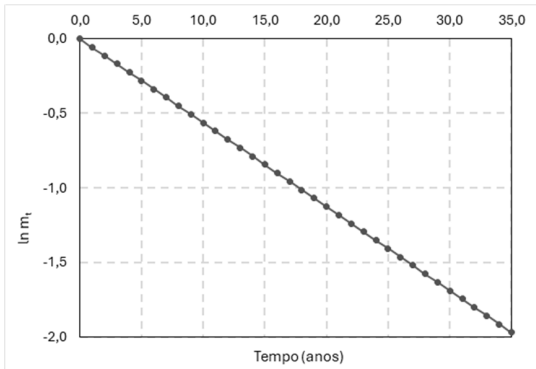
Figura 1 – Logaritmo natural da massa de 3H em função do tempo em anos.
Utilizando dados do gráfico anterior, calcule o tempo de meia-vida do trítio. A alternativa que apresenta o valor obtido, aproximadamente, é:
Provas
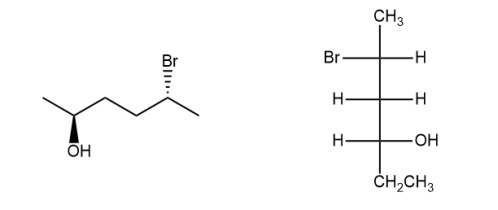
Os estereoisômeros têm seus átomos ligados na mesma sequência, mas diferem no arranjo de seus átomos no espaço, são substâncias diferentes que não se convertem facilmente, por isso podem ser separados. Há dois tipos de estereoisômeros: enantiômeros e diasteroisômeros.
Sobre as moléculas a seguir, assinale a opção CORRETA:
Provas
Caderno Container