Foram encontradas 50 questões.
Acerca do que consta no Código de Ética Profissional do Servidor Público Civil do Poder Executivo Federal (Decreto nº 1.171/1994) e no Sistema de Gestão da Ética do Poder Executivo Federal (Decreto nº 6.029/2007), assinale a alternativa CORRETA:
Provas
A técnica de Espectroscopia de Infravermelho (IV) é um método de análise que fornece evidências da presença de grupos funcionais presentes na estrutura de substâncias, podendo ser usada para identificar um composto ou investigar sua composição química. Entre as afirmações abaixo, indique aquela que NÃO ESTÁ CORRETA:
Provas
Na determinação gravimétrica de chumbo (II) através da precipitação na forma de cromato de chumbo (II), o precipitante pode ser obtido indiretamente na solução através da reação:
![]()
Após o balanceamento correto da reação anterior, a soma dos menores coeficientes estequiométricos inteiros do membro dos produtos é:
Provas
O urânio-233 (233U) é físsil e sofre decaimento, segundo a reação nuclear:
![]()
Calcule a energia liberada quando 1 mol de urânio-233 decai. A alternativa que apresenta o valor CORRETO é:
Dados: Velocidade da luz ![]()
![]()
Provas
O tório (Th) é um elemento mais abundante na crosta terrestre do que o urânio (U). Além disso, o decaimento radioativo dos isótopos do tório produz menos resíduos. Por isso, cada vez mais pesquisas são desenvolvidas para contornar os problemas tecnológicos da utilização de isótopos do tório como combustível em usinas de fissão nuclear. No ciclo do Th como combustível, ocorrem as seguintes reações nucleares:
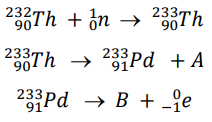
As espécies químicas A e B são, RESPECTIVAMENTE:
Provas
A tabela de potenciais padrão de redução é utilizada para determinar a diferença de potencial (ddp) de um sistema eletroquímico quando este está na temperatura de 25ºC, pressão de 1 atm e as concentrações das espécies envolvidas são de 1 mol/L. Caso pelo menos uma dessas condições se altere, a diferença de potencial, normalmente, também sofre variação. Porém, em alguns casos, pode acontecer da ddp do sistema ser igual à do estado padrão, mesmo que alguma alteração ocorra. Para o sistema eletroquímico espontâneo envolvendo íons magnésio e íons cobre (I), a 25ºC e 1 atm, quais concentrações fora do estado padrão, respectivamente, levam a uma ddp igual à do estado padrão?
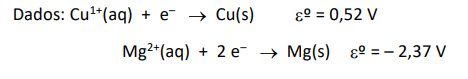
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Numa aula prática de Química, serão utilizados 800 mL de solução de NaOH 0,5 mol/L. Porém, não foi encontrada nenhuma solução com a concentração necessária, havendo disponíveis apenas as seguintes soluções de NaOH:
Solução A: 1,0 mol/L
Solução B: 5 g/L
Solução C: 0,25 mol/L
O técnico de laboratório resolveu o problema misturando quantidades adequadas de cada solução. Sabendo que foram utilizados 100 mL da solução B, quais foram os volumes utilizados das soluções A e C, RESPECTIVAMENTE?
Provas
A emissão de óxidos de nitrogênio nos processos de combustão provoca um problema ambiental sério porque esses óxidos são poluentes primários e geram poluentes secundários através de ciclos fotoquímicos na atmosfera. Normalmente, o óxido de nitrogênio emitido em maior quantidade é o NO que se oxida a NO2 quando reage com oxigênio:
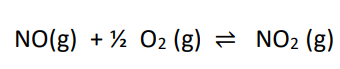
Calcule a constante de equilíbrio do sistema anterior, no estado padrão, utilizando dados termodinâmicos:
Dados: \( \Delta \)Gºf (NO2(g)) = + 52 kJ/mol ; \( \Delta \)Gºf (NO(g)) = + 87 kJ/mol; R = 8,314 J/mol.K
A opção que apresenta a alternativa CORRETA é:
Provas
As medalhas de ouro entregues aos primeiros lugares nos jogos olímpicos não são de ouro maciço. Tais medalhas são feitas de prata maciça com uma camada de ouro depositada. Nas olimpíadas de Paris, as medalhas recebidas pelas pessoas que conquistaram as primeiras colocações tinham massa total de 529 g. Desse total, além do ouro depositado, 505 g eram de prata e havia uma placa de ferro, retirada da torre Eiffel, com massa de 18 g.
Considerando que o ouro foi depositado na medalha de prata a partir da eletrólise de uma solução de nitrato auroso, calcule a intensidade de corrente necessária para que o processo demorasse 1 h para cada medalha e assinale a alternativa CORRETA.
Provas
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Química OrgânicaPropriedades Químicas dos Compostos Orgânicos
Uma das características dos íons complexos de metais de transição é a cor que resulta, entre outras coisas, da interação dos fótons da luz com os elétrons d do metal. A seguir, são apresentados alguns íons complexos e suas respectivas cores:

Os nomes oficiais dos íons complexos anteriores são encontrados, RESPECTIVAMENTE, na alternativa:
Provas
Caderno Container