Foram encontradas 244 questões.
Na microscopia ótica a parte do equipamento em que se
coloca a lâmina para ser analisada e a outra que possibilita
o deslocamento anteroposterior e lateral para movimentar o
preparado são, respectivamente,
Provas
Questão presente nas seguintes provas
A esterilização tem o objetivo de destruir quaisquer micro-organismos presentes em materiais de uso laboratorial,
inclusive esporos. Assim, o processo que utiliza calor úmido
com temperaturas acima de 100° C, em alta pressão, é a
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A acidez de frutas cítricas, como a laranja e o limão, é devido
à presença do ácido 2-hidroxi-1,2-3-propanotricarboxílico,
mais conhecido por ácido cítrico, C6H8O7 (massa molar =
192,0 g mol-1). A sua estrutura é mostrada na figura a seguir. 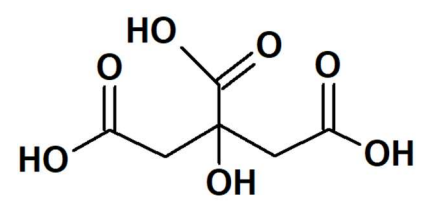
Para se determinar o teor percentual massa/volume (% m/V) em um determinado limão, coletou-se 2,0 mL do sumo deste limão e titulou-se, em triplicata, através de técnica adequada, com solução padronizada de NaOH 0,110 mol L-1 na presença de indicador fenolftaleína até atingir o ponto de equivalência. Gastou-se, em média, 12,0 mL da base. Desta forma, o valor calculado para o teor % (m/V) de ácido cítrico no limão é igual a

Para se determinar o teor percentual massa/volume (% m/V) em um determinado limão, coletou-se 2,0 mL do sumo deste limão e titulou-se, em triplicata, através de técnica adequada, com solução padronizada de NaOH 0,110 mol L-1 na presença de indicador fenolftaleína até atingir o ponto de equivalência. Gastou-se, em média, 12,0 mL da base. Desta forma, o valor calculado para o teor % (m/V) de ácido cítrico no limão é igual a
Provas
Questão presente nas seguintes provas
O fenômeno do decaimento radioativo ocorre naturalmente
quando o núcleo de um átomo de determinado elemento
químico se torna instável e, consequentemente, se fragmenta,
emitindo radiações eletromagnéticas e desintegrando-se.
Um dos principais tipos é o decaimento beta, que promove
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Ácidos fracos são espécies químicas muito pouco dissociadas
em meio aquoso. Um exemplo é o ácido acético (CH3COOH),
que possui uma constante de dissociação ácida, Ka, igual a
1,8x10-5 e está em equilíbrio com os íons acetato, CH3COOe próton, H+
, conforme a equação a seguir.
CH3COOH(aq) ⇄ CH3COO- (aq) + H+ (aq)
Dado: pH = -log [H+]
Suponha que foi preparada, em laboratório, uma solução aquosa de ácido acético 0,2 mol L-1. O pH dessa solução possui valor aproximado de
CH3COOH(aq) ⇄ CH3COO- (aq) + H+ (aq)
Dado: pH = -log [H+]
Suponha que foi preparada, em laboratório, uma solução aquosa de ácido acético 0,2 mol L-1. O pH dessa solução possui valor aproximado de
Provas
Questão presente nas seguintes provas
O balanceamento de equações químicas é a etapa mais
importante no estudo prévio de reações químicas. Ele
envolve o ajuste dos coeficientes estequiométricos, de
modo que o número de átomos de cada elemento seja igual
em ambos os lados da equação, ou seja, no lado do(s)
reagente(s) e do(s) produto(s). Considere a equação a
seguir.
Cu(s) + HNO3(aq) → Cu(NO3)2(aq) + NO(g) + H2O(l)
Balanceando-se a equação de oxirredução acima com algarismos inteiros, determina-se que o somatório de todos os seus coeficientes estequiométricos é igual a
Cu(s) + HNO3(aq) → Cu(NO3)2(aq) + NO(g) + H2O(l)
Balanceando-se a equação de oxirredução acima com algarismos inteiros, determina-se que o somatório de todos os seus coeficientes estequiométricos é igual a
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
O modelo de repulsão dos pares de elétrons da camada de
valência, RPECV, fornece um método confiável de prever as
formas das moléculas e dos íons poliatômicos. Ele é
baseado na ideia de que pares de elétrons isolados e de
ligação na camada de valência de um elemento repelem uns
aos outros e buscam ficar o mais longe possível uns dos
outros, sendo possível, então, determinar a geometria de
uma dada molécula ou íon. A aplicação desse modelo ao
íon tetracloroiodato, ICl4-
, informa que esse íon possui
geometria molecular
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Ácidos concentrados comerciais são amplamente utilizados
em laboratório de ensino e pesquisa em reações químicas.
Uma forma de uso convencional é o emprego de soluções
diluídas desses ácidos. Suponha que um químico preparou
25,0 mL de uma solução aquosa 1,0 mol L-1 de ácido
clorídrico (HCl) a partir do ácido concentrado disponível em
estoque (considere: massa molar HCl = 36,5 g mol-1; Teor
% (m/m) = 36,5 – 38,5% e d = 1,19 g mL-1). O volume
utilizado do ácido concentrado, em mL, para preparar a
referida solução foi igual a
Provas
Questão presente nas seguintes provas
Em um laboratório, são utilizadas diferentes vidrarias para
medir volumes de líquidos. Dentre elas, são exemplos de
vidrarias empregadas para medir volumes exatos de líquidos:
Provas
Questão presente nas seguintes provas
Uma célula galvânica é constituída por um eletrodo de
magnésio (Mg), mergulhado em uma solução 1,0 mol L-1 de
Mg2+, e por um eletrodo de prata (Ag), mergulhado em uma
solução 1,0 mol L-1 de Ag+. Dados os potenciais padrões de
redução a seguir.
Ag+ (aq) + e- (aq) → Ag(s) E° = 0,80 V Mg2+(aq) + 2e- (aq) → Mg(s) E° = -2,37 V
Determina-se que o potencial padrão da célula em volts, a 25 °C, é
Ag+ (aq) + e- (aq) → Ag(s) E° = 0,80 V Mg2+(aq) + 2e- (aq) → Mg(s) E° = -2,37 V
Determina-se que o potencial padrão da célula em volts, a 25 °C, é
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container