Foram encontradas 715 questões.
O isótopo tório-232 \((^{232}_{90}Th)\) é um elemento radioativo que sofre um processo de decaimento por emissão de uma partícula alfa (α), transformando-se em um nuclídeo mais estável. Com base nesse processo de decaimento, os números de prótons e nêutrons do nuclídeo formado são, respectivamente,
Provas
Em uma aula experimental de cinética química, conduzida pelo professor de química, foi possível determinar a lei de velocidade da seguinte reação:
NO(g) + ½ O2(g) → NO2(g)
Sabe-se que a reação é de primeira ordem em relação ao NO e de terceira ordem global. Diante dessas informações, analise as assertivas e assinale a alternativa que aponta a(s) correta(s).
I. A lei de velocidade da reação é: v = k [NO] [O2]2 .
II. Se a concentração de NO for aumentada em um fator de 1,5, mantendo a concentração de O2 constante, a velocidade da reação aumenta em um fator de 0,75.
III. Se a concentração de O2 for aumentada em um fator de 1,5, mantendo a concentração de NO constante, a velocidade da reação aumenta em um fator de 2,25.
Provas
Considere a fórmula estrutural da molécula orgânica a seguir:
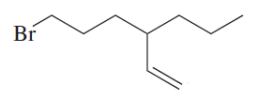
Com base nessa estrutura, assinale a alternativa que apresenta o nome oficial correto da molécula de acordo com as regras da IUPAC.
Provas
Em relação à propriedade periódica denominada energia de ionização, assinale a alternativa INCORRETA.
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Iônico: Conceitos, Diluição de Ostwald, Efeito do Íon Comum
Em uma aula experimental de química, o professor demonstrou o efeito da acidez sobre o equilíbrio entre os íons dicromato e cromato, representado pela seguinte equação química:
Cr2O72- (aq) + H2O(l) ⇌ 2 CrO42- (aq) + 2 H+ (aq)
Com base nesse equilíbrio químico e de acordo com o princípio de Le Châtelier, analise as assertivas e assinale a alternativa que aponta a(s) correta(s).
I. A adição de ácido clorídrico favorece o deslocamento do equilíbrio no sentido da formação de mais íons dicromato.
II. A adição de hidróxido de sódio favorece o deslocamento do equilíbrio no sentido da formação de mais reagentes.
III. A diminuição do pH favorece o deslocamento do equilíbrio no sentido da formação de mais produtos.
Provas
Considerando as reações em solução aquosa a seguir, assinale a alternativa que apresenta uma reação de oxirredução.
Provas
Uma seringa hermética contém 25,0 mL de gás CO2 à temperatura de 2 °C. Sob pressão constante, a temperatura do gás é elevada para 57 °C. Diante dessas informações e considerando o comportamento ideal para o gás CO2, assinale a alternativa que apresenta o volume de gás CO2 após o aumento de temperatura. Dado: 0 °C = 273 K.
Provas
Durante procedimento experimental, o professor de química preparou uma solução que resultou da mistura de uma solução de benzoato de sódio com uma solução de ácido benzoico (Ka = 6,5×10−5 , pKa ≈ 4,2), à temperatura de 25 °C. As concentrações de ácido benzoico e de benzoato de sódio, na solução final, são iguais a 0,1 mol/L cada. Diante dessas informações e desconsiderando o equilíbrio de autoionização da água, analise as assertivas e assinale a alternativa que aponta a(s) correta(s). Dado: Kw = 1,0×10−14 (25 °C).
I. A referida mistura consiste em uma solução tampão.
II. A solução resultante apresenta caráter básico.
III. A solução final apresenta uma concentração de íons H3O+ igual ao valor da constante de acidez (Ka).
Provas
Dados os valores da constante de produto de solubilidade (Kps) dos sais de prata a 25 °C, assinale a alternativa que apresenta a sequência correta desses sais, em ordem crescente de solubilidade molar, nessa mesma temperatura.
Kps (AgBr) = 5,3×10−13 .
Kps (AgI) = 8,5×10−17
Kps (AgCN) = 5,9×10−17 .
Kps (AgCl) = 1,8×10−10 .
Kps (AgSCN) = 1,0×10−12 .
Provas
A fermentação é um processo bioquímico complexo no qual a glicose é convertida em etanol e dióxido de carbono, conforme demonstrado na reação (não balanceada) a seguir:
C6H12O6(s) → C2H5OH(l) + CO2(g)
Um técnico de determinado laboratório, responsável pelo processo de fermentação, utilizou a quantidade de 1 kg de glicose para a produção de etanol. Sabendo que a reação foi completa, assinale a alternativa que apresenta o volume de etanol, aproximado, que foi produzido nesse processo.
Dado: densidade do etanol = 0,8 g/mL.
Provas
Caderno Container