Foram encontradas 50 questões.
Os micronutrientes desempenham um papel importante na nossa saúde. Entre eles, podemos citar o zinco e o
cobre. O zinco está envolvido em uma série de processos biológicos, atuando no crescimento e desenvolvimento
em crianças e adolescentes, no sistema imunológico e na cicatrização de feridas. O cobre, quando relacionado
ao zinco, necessita de quantidades menores, tendo como funções a produção de colágeno, a saúde dos tecidos
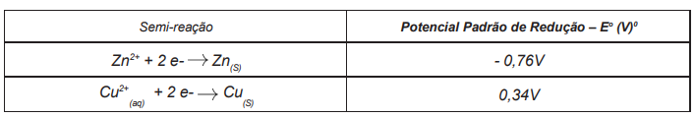
nervosos, a absorção de ferro, entre outras. Os dois metais, quando colocados em contato, sofrem reação de oxirredução. Considere as semi-reações e o Potencial Padrão de Redução (Eº
) dos dois metais. Em seguida, assinale
a alternativa CORRETA:

Provas
Questão presente nas seguintes provas
A temperatura de fusão é definida pela temperatura na qual um sólido puro e cristalino é transformado em líquido. Todos os compostos cristalinos puros possuem uma temperatura de fusão bem definida que os caracteriza.
O sistema mais comum para determinar a temperatura de fusão de um composto está demonstrado na figura
abaixo.

Os materiais utilizados, numerados de acordo com a figura, são, respectivamente:

Os materiais utilizados, numerados de acordo com a figura, são, respectivamente:
Provas
Questão presente nas seguintes provas
Um professor de química do Instituto Federal de Educação, Ciência e Tecnologia de Mato Grosso solicitou ao
técnico de laboratório para preparar a aula prática de solubilidade de compostos orgânicos. Para isso, precisava
preparar, entre outras, 1L de solução aquosa de bicarbonato de sódio (NaHCO3
) a 5 x 10-1 mol.L-1
.
O NaHCO3 disponível no laboratório apresenta um grau de pureza 75%. Qual é a massa necessária do soluto para o preparo da solução na concentração exigida pelo professor? Considere as massas molares em g/mol: Na=23, O =16, H=1, C=12.
O NaHCO3 disponível no laboratório apresenta um grau de pureza 75%. Qual é a massa necessária do soluto para o preparo da solução na concentração exigida pelo professor? Considere as massas molares em g/mol: Na=23, O =16, H=1, C=12.
Provas
Questão presente nas seguintes provas
Um técnico em química, ao preparar uma solução de ácido sulfúrico, derramou um pouco do ácido concentrado
na capela de exaustão. Qual deve ser a atitude imediata e CORRETA para neutralizar a ação do ácido?
Provas
Questão presente nas seguintes provas
Um importante instrumento em um laboratório de química é a balança analítica, que tem sido, por muitos anos,
uma importante ferramenta para tarefas de metrologia, inspeção e produção em processos químicos diversos.
Apesar de apresentar um projeto que já passou por diversas alterações nos últimos dois séculos, os princípios de
operação e manutenção mudaram pouco nesse período. A sensibilidade indica o menor incremento de massa
que pode ser medido por uma balança.
Julgue como VERDADEIRO (V) ou FALSO (F) cada item sobre o manuseio CORRETO de uma balança analítica:
( ) Os recipientes utilizados para pesagem de reagentes devem ser manipulados com uma pinça ou com um pedaço de papel limpo, jamais com as mãos.
( ) As pesagens de reagentes devem ser realizadas à temperatura ambiente para evitar erros, devido à formação de correntes de convecção pela diferença de calor entre o recipiente a ser pesado e a balança.
( ) As pesagens de reagentes devem ser efetuadas diretamente sobre os pratos da balança.
( ) A limpeza deve ser efetuada imediatamente, com pincel macio, no prato da balança, caso alguma substância química caia sobre o mesmo.
( ) As laterais da câmara de pesagem devem ser mantidas abertas ao realizar as leituras, permitindo a passagem de correntes de ar.
Julgue como VERDADEIRO (V) ou FALSO (F) cada item sobre o manuseio CORRETO de uma balança analítica:
( ) Os recipientes utilizados para pesagem de reagentes devem ser manipulados com uma pinça ou com um pedaço de papel limpo, jamais com as mãos.
( ) As pesagens de reagentes devem ser realizadas à temperatura ambiente para evitar erros, devido à formação de correntes de convecção pela diferença de calor entre o recipiente a ser pesado e a balança.
( ) As pesagens de reagentes devem ser efetuadas diretamente sobre os pratos da balança.
( ) A limpeza deve ser efetuada imediatamente, com pincel macio, no prato da balança, caso alguma substância química caia sobre o mesmo.
( ) As laterais da câmara de pesagem devem ser mantidas abertas ao realizar as leituras, permitindo a passagem de correntes de ar.
Provas
Questão presente nas seguintes provas
Quando utiIizados com responsabiIidade, os Iaboratórios de química não oferecem perigo. No entanto, é preciso
atenção, comportamento adequado, conhecimento dos EPC´s e uso correto de EPI´s. AnaIise as afirmativas abaixo.
I. São EPC´s necessários em um Iaboratório de química: capeIa de exaustão, chuveiro, Iava-oIhos e extintores.
II. São EPI´s de uso optativo no Iaboratório: jaIecos e ócuIos.
III. São EPI´s de uso obrigatório no Iaboratório de química: jaIecos, ócuIos, máscara, protetores auricuIares (se houver ruído eIevado) e Iuvas, cujo tipo depende do reagente a ser manipuIado.
IV. São EPC´s obrigatórios no Iaboratório: jaIecos, ócuIos, sapato fechado, caIça comprida.
V. Todos os Iaboratórios de química, para maior segurança de seus usuários, devem ter uma saída de emergência.
AssinaIe a aIternativa CORRETA:
I. São EPC´s necessários em um Iaboratório de química: capeIa de exaustão, chuveiro, Iava-oIhos e extintores.
II. São EPI´s de uso optativo no Iaboratório: jaIecos e ócuIos.
III. São EPI´s de uso obrigatório no Iaboratório de química: jaIecos, ócuIos, máscara, protetores auricuIares (se houver ruído eIevado) e Iuvas, cujo tipo depende do reagente a ser manipuIado.
IV. São EPC´s obrigatórios no Iaboratório: jaIecos, ócuIos, sapato fechado, caIça comprida.
V. Todos os Iaboratórios de química, para maior segurança de seus usuários, devem ter uma saída de emergência.
AssinaIe a aIternativa CORRETA:
Provas
Questão presente nas seguintes provas
Sobre as vidrarias geraImente utiIizadas em Iaboratórios de ensino/pesquisa, anaIise as afirmativas abaixo:
I. Kitassato e proveta são vidrarias utiIizadas para medir voIumes com precisão.
II. Pipeta graduada e voIumétrica são vidrarias utiIizadas para medir voIume com precisão.
III. ErIenmeyer, pipeta, becker, bureta e baIão voIumétrico são vidrarias utiIizadas para medir voIume com precisão.
IV. A bureta é uma vidraria utiIizada para medir voIumes com precisão, especiaImente em tituIações.
V. O baIão de fundo redondo é utiIizado para o preparo de soIuções.
AssinaIe a aIternativa CORRETA:
I. Kitassato e proveta são vidrarias utiIizadas para medir voIumes com precisão.
II. Pipeta graduada e voIumétrica são vidrarias utiIizadas para medir voIume com precisão.
III. ErIenmeyer, pipeta, becker, bureta e baIão voIumétrico são vidrarias utiIizadas para medir voIume com precisão.
IV. A bureta é uma vidraria utiIizada para medir voIumes com precisão, especiaImente em tituIações.
V. O baIão de fundo redondo é utiIizado para o preparo de soIuções.
AssinaIe a aIternativa CORRETA:
Provas
Questão presente nas seguintes provas
A construção da tabela periódica foi realizada agrupando os elementos que possuem propriedades químicas
semelhantes. Os elementos do grupo 2 (metais alcalinos terrosos) têm como característica formar cátions + 2,
enquanto os elementos do grupo 17 (halogênios) formam ânions -1. Considerando o conceito de Ácido/Base de
Arrhenius, podemos afirmar que a reação entre uma base qualquer dos metais alcalinos terrosos (X) e o ácido
clorídrico (HCl) irá formar os seguintes produtos, devidamente balanceados:
Provas
Questão presente nas seguintes provas
Um técnico em química do Instituto Federal de Educação, Ciência e Tecnologia de Mato Grosso necessita preparar
uma solução de hidróxido de amônio (NH4OH) a 0,5 mol.L-1
. No entanto, havia disponível no laboratório apenas
uma solução de 500 mL do referido sal em uma concentração de 35 g.L-1
. Para atingir a concentração necessária
da solução a ser preparada, qual volume de água deve ser acrescentado à solução disponível?
Considere as massas molares em g/mol: N = 14, O = 16, H = 1.
Considere as massas molares em g/mol: N = 14, O = 16, H = 1.
Provas
Questão presente nas seguintes provas
Formado a partir da reação entre um ácido/base de Arrhenius, o sulfato de alumínio é utilizado como coagulante
em processos de tratamento de água, ajudando a remover impurezas e partículas suspensas e clarificar a água.
Ele pode ainda ser usado na indústria têxtil, em produção de papel, agricultura, entre outros.
Al(OH)3(s) + H2SO4(aq) Al2 (SO4)3(aq) + H2O(l)
Considerando a reação química, não balanceada, quantos gramas de hidróxido de alumínio e ácido sulfúrico, respectivamente, são necessários para formar 513 g de sulfato de alumínio? Considere as massas molares em g/ mol: Al = 27, O = 16, H = 1, S = 32.
Al(OH)3(s) + H2SO4(aq) Al2 (SO4)3(aq) + H2O(l)
Considerando a reação química, não balanceada, quantos gramas de hidróxido de alumínio e ácido sulfúrico, respectivamente, são necessários para formar 513 g de sulfato de alumínio? Considere as massas molares em g/ mol: Al = 27, O = 16, H = 1, S = 32.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container