Foram encontradas 40 questões.
Provas
Os espectrômetros são equipamentos que nos permitem obter informações ópticas acerca da matéria. Para distinguirmos quais propriedades estamos querendo observar, devemos utilizar o equipamento adequado à necessidade. Sobre as representações esquemáticas dos equipamentos mostrados na FIGURA 5, podemos afirmar que
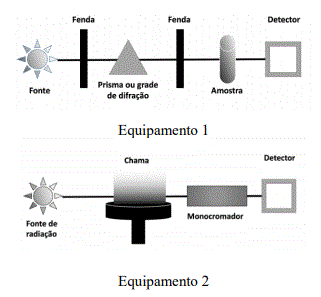
FIGURA 5: Esquemas de dois diferentes equipamentos para medidas ópticas.
Provas
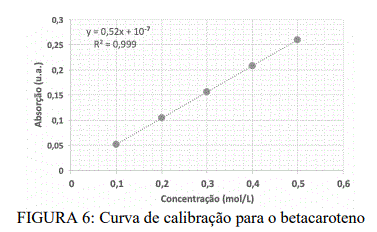
Em um laboratório de química, é muito comum utilizar as balanças como instrumentos de medidas. Diferentes tipos de balanças podem ser utilizadas, a depender do tipo de medida a qual se deseja realizar. Algumas vezes é importante realizar apresentações de química ao público, como se faz, por exemplo, em atividades do tipo Show da Química. Nesses casos, faz-se necessária a utilização das balanças portáteis. Porém, em um laboratório, os tipos mais comuns de balanças encontradas são aquelas denominadas de analítica e semianalítica. Em um laboratório de química do IFPE, dois estudantes do Curso Médio Técnico Integrado de Química realizaram uma série de pesagem de uma mesma massa de glicose. O estudante 1 utilizou, para isso, uma balança semianalítica, e o estudante 2 utilizou uma balança analítica. Os dados das pesagens foram apresentados sob a forma de um gráfico, como mostrado na FIGURA 4.

Sobre a análise dos resultados e sabendo que o valor real da massa é igual a 1,0000 + 0,0001g, podemos afirmar que
Provas
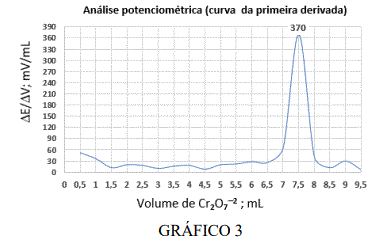
Uma amostra contendo íons de Fe+2(aq) foi submetida a uma análise pelo método de titulação potenciométrica utilizando uma célula que consiste de um eletrodo de calomelano saturado e um eletrodo indicador de platina. A amostra líquida contendo íons de Fe+2(aq) foi preparada conforme protocolo de análise e diluída para 100 mL com água deionizada. Em seguida, uma alíquota de 20 mL foi retirada e foi submetida à titulação com solução de K2Cr2O7 0,0166 M. O GRÁFICO 3 representa a variação do potencial por unidade de titulante ( Δ E/V; mV/mL) em função do volume da solução de K2Cr2O7 adicionada
A equação iônica está representada a seguir:
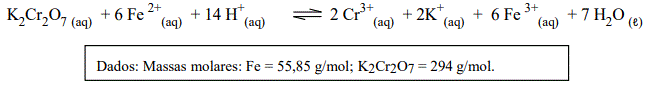
Assinale a alternativa que apresenta a massa do íon Fe+2(aq) presente na amostra inicial.
Provas

![]()
Provas
Uma pesquisa foi realizada com um grupo de profissionais que trabalham em laboratórios de química com o propósito de certificar o conhecimento dos pictogramas de perigo que são informados na rotulagem de produtos químicos. Os pictogramas dessa pesquisa estão de acordo com a ABNT NBR 14725 e são:

Obs.: A borda dos pictogramas é de cor vermelha.
O resultado da pesquisa está ilustrado no GRÁFICO 2, o qual mostra o percentual de acertos por pictograma.

Analise as afirmativas e assinale a que indica CORRETAMENTE o significado de 3 pictogramas que obtiveram índice de acerto inferior a 50% no resultado da pesquisa.
Provas
Com o objetivo de executar a calibração de uma pipeta volumétrica de 25 mL, classe A, medições consecutivas foram realizadas utilizando água, na temperatura de 25°C, até a aferição da vidraria e o volume do líquido dispensado foi pesado, empregando-se massas de aço inoxidável. Esse procedimento foi repetido por 3 vezes, e os valores, anotados na TABELA 1.

SKOOG, D. A.; WEST, D. M.; HOLLER, F. J.; CROUCH, S. R.et al. Fundamentos de química analítica. 8ª ed. São Paulo: Thomson Learning, 2006, 45p.
Utilizando a TABELA 1, o QUADRO 1 e os seus conhecimentos de estatística, calcule o desvio padrão e assinale a alternativa que apresenta esse valor numérico aproximado.
Provas
O método de Volhard foi utilizado para determinar a pureza de uma amostra de 0,164 g de brometo de potássio. Inicialmente a massa de brometo de potássio foi dissolvida em 50 mL de água destilada e foi adicionado um excesso de 45 mL de solução de nitrato de prata a 0,03 M, que reagem na proporção de 1:1 precipitando os íons de brometo presentes na solução. Em sequência, o excesso de Ag+ foi determinado, por retrotitulação, utilizando 6,50 mL de uma solução padrão de tiocianato de potássio (KSCN) a 0,07 M, meio ácido. Utilizando seus conhecimentos sobre cálculos estequiométricos e análise volumétrica, assinale a alternativa que apresenta o valor aproximado do percentual de pureza da amostra inicial de KBr.
![]()
Provas
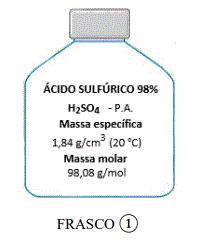
Na preparação de 500 mL de uma solução de ácido sulfúrico 4 mol/L, um determinado volume foi retirado
do frasco ![]() e diluído em água destilada até completar o volume desejado. Toda a preparação ocorreu
com cuidado e em atenção às normas de segurança, contudo a padronização da solução ácida com
hidróxido de sódio acarretou um fator de correção da molaridade igual 0,85.
e diluído em água destilada até completar o volume desejado. Toda a preparação ocorreu
com cuidado e em atenção às normas de segurança, contudo a padronização da solução ácida com
hidróxido de sódio acarretou um fator de correção da molaridade igual 0,85.
Assinale a alternativa que contém o volume de ácido sulfúrico devido para a preparação da solução a 4 mol/L e o volume real utilizado na prática, respectivamente
Provas
As análises de volumetria de oxidação-redução necessitam de reações químicas balanceadas que forneçam os coeficientes estequiométricos para subsidiar os cálculos químicos. A FIGURA 3 corresponde à equação química, não balanceada, da reação de oxidação do álcool propano-1,2,3-triol (C3H8O3), em meio ácido, utilizando ânions de dicromato (Cr2O72- ).
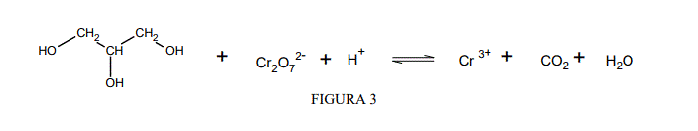
Utilizando os seus conhecimentos sobre balanceamento químico de reações, analise as afirmativas e assinale a CORRETA.
Provas
Caderno Container