Foram encontradas 40 questões.
O sistema formal de nomenclatura para compostos orgânicos é proposto pela União Internacional de Química Pura e Aplicada (IUPAC). Norteando o sistema IUPAC de nomenclatura, está o princípio fundamental de que cada composto diferente deve ter um nome não ambíguo. Assim, através de um conjunto sistemático de regras, a IUPAC fornece diferentes nomes para mais de 16 milhões de compostos orgânicos conhecidos.
Assinale a alternativa que apresenta CORRETAMENTE o nome sistemático IUPAC para cada um dos compostos a seguir.
I.
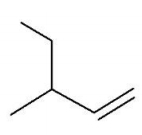
II.
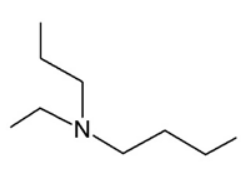
III.
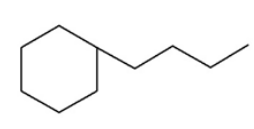
IV.
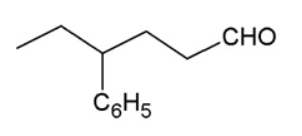
Provas
Na tabela a seguir, são apresentados os pontos de ebulição (pe), medidos em °C, a 1 atm, para 5 compostos orgânicos diferentes:
Composto | pe(ºC) |
A | -11,7 |
B | 0,5 |
C | 9,5 |
D | 36,1 |
E | 138,0 |
Os compostos A, B, C, D e E podem ser, respectivamente:
Provas
Em relação à estrutura molecular e ligações do carbono, assinale a alternativa em que todas as afirmativas está(ão) CORRETA(S):
I. Os ângulos de ligação nos átomos de carbono da molécula de etano são todos de 109,5°, e a ligação carbono-carbono é uma ligação do tipo sigma formada por dois orbitais sp3 .
II. Na molécula de eteno a ligação dupla carbono-carbono consiste em uma ligação sigma (σ) e uma ligação pi (π); a ligação σ resulta da superposição frontal de dois orbitais sp2 e a ligação π resulta da superposição lateral de dois orbitais p.
III. O etino é um composto no qual dois átomos de carbono são hidridizados sp, com ângulos de ligação de 180°, e apresenta restrição de rotação dos grupos ligados pela ligação tripla, restrição que também ocorre na ligação dupla dos alcenos.
IV. A ligação simples carbono-carbono é mais curta que a ligação dupla carbono-carbono, e a ligação dupla carbono-carbono é mais curta que a ligação tripla carbono-carbono.
Provas
Relacione as colunas 1 e 2, identificando a correspondência a respeito das funções orgânicas:
Coluna 1:
1. A função tem fórmula geral RCO2R’ (ou RCOOR’), onde um grupo carbonila está ligado a um grupo alcoxila (−OR).
2. Apresenta as fórmulas RCONH2, RCONHR’ ou RCONR’R’’, onde o grupo carbonila está ligado a um átomo de nitrogênio sustentando hidrogênios e/ou grupos alquila.
3. O carbono e o nitrogênio do grupo funcional são hibridizados sp e a fórmula da função é R−CN.
4. A função apresenta um grupo carbonila ligado a um grupo hidroxila, e tem fórmula geral RCO2H.
5. A fórmula geral da função é R−O−R ou R−O−R’, onde R’ pode ser um grupo alquila (ou fenila) diferente de R.
Coluna 2:
( ) Éster.
( ) Nitrila.
( ) Ácido carboxílico.
( ) Amida.
( ) Éter.
Assinale a alternativa que indica a sequência CORRETA, de cima para baixo.
Provas
Um reator contém NH3, N2 e H2 em equilíbrio a certa temperatura. As concentrações de equilíbrio são [NH3] = 0,30 mol/L, [N2] = 0,10 mol/L e [H2] = 2,00 mol/L. Assinale a alternativa CORRETA, que indica a constante de equilíbrio Kc para a síntese da amônia se a reação for representada por:
N2(g) + 3H2(g) ↔ 2NH3(g)
Provas
O equilíbrio químico resulta de um balanço entre as reações direta e inversa. Na maioria dos casos, este equilíbrio é um tanto sensível. Variações nas condições experimentais podem perturbar o equilíbrio e deslocar sua posição, dando origem a uma maior ou menor quantidade do produto desejado. Com relação aos fatores que afetam um sistema reacional em equilíbrio, assinale a alternativa INCORRETA:
Provas
Considere a reação de primeira ordem A → B apresentada no diagrama a seguir:

t = 0 segundos
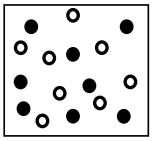
t = 15 segundos
Legenda
A ![]()
B ![]()
Assinale a alternativa CORRETA, que indica a constante de velocidade da reação (k), e quantas moléculas de A e de B estão presentes no tempo de 45 segundos.
Provas
Considere um sistema com reações sucessivas, no qual A é convertido em B, que é seguidamente convertido em C.
A → B → C
Admitindo que as duas etapas do sistema sejam de primeira ordem, assinale a alternativa CORRETA, que é compatível com as variações de [A], [B] e [C] em função do tempo:
![]()
Provas
Em um processo de eletrólise, uma corrente de 2,0 A passa por uma solução de íons de prata, durante 30 minutos, ocorrendo deposição de cobre no cátodo, segundo a reação a seguir:
Ag+ (aq) + e -→ Ag(s)
Qual massa de cobre, em gramas, foi depositada no cátodo? (Constante de Faraday: 9,65x104C).
Provas
Considerando pilha Cd(s)│Cd2+ (aq)||Ni2+ (aq)│Ni(s) e os dados dos potenciais de redução em solução aquosa a 25ºC, a seguir: E°Cd = -0,40V; E°Ni = -0,25V.
Analise as afirmativas, identificando com “V” as VERDADEIRAS e com “F” as FALSAS, assinalando a seguir a alternativa CORRETA, na sequência de cima para baixo:
( ) Na reação da pilha o níquel atua como agente redutor e o cádmio como agente oxidante.
( ) O eletrodo de Cd é o anodo da pilha eletroquímica, no qual há oxidação; sendo assim, tem polaridade negativa.
( ) Considerando os dados dos potenciais padrões, o valor de E°global a 25ºC é +0,15V, indicando que a reação é favorável aos produtos.
( ) Considerando os dados dos potenciais padrões, o valor de E°global a 25ºC é -0,65V, indicando que a reação é favorável aos reagentes.
( ) O fluxo de elétrons, no circuito externo da pilha, flui do eletrodo de Ni para o eletrodo Cd.
Provas
Caderno Container