Foram encontradas 40 questões.
Dadas as seguintes semi-reações:
Fe+2(aq) + 2 e- → Fe(s) E° = - 0,44 V Pb+2(aq) + 2 e- → Pb(s) E°= - 0,13 V
E considerando a formação de uma pilha, são feitas as seguintes afirmativas:
I. A reação que ocorre no cátodo é Pb+2(aq) + 2 e- → Pb(s). II. A Pilha pode ser representada por Fe2+(aq) / Fe(s) // Pb2+(aq) / Pb(s). III. A voltagem da pilha é igual a 0,31 V. IV. A reação não é espontânea.
Assinale a alternativa em que todas as afirmativas estão CORRETAS:
Fe+2(aq) + 2 e- → Fe(s) E° = - 0,44 V Pb+2(aq) + 2 e- → Pb(s) E°= - 0,13 V
E considerando a formação de uma pilha, são feitas as seguintes afirmativas:
I. A reação que ocorre no cátodo é Pb+2(aq) + 2 e- → Pb(s). II. A Pilha pode ser representada por Fe2+(aq) / Fe(s) // Pb2+(aq) / Pb(s). III. A voltagem da pilha é igual a 0,31 V. IV. A reação não é espontânea.
Assinale a alternativa em que todas as afirmativas estão CORRETAS:
Provas
Questão presente nas seguintes provas
Um técnico em química realizou a
determinação das entalpias de combustão (ΔHº)
de três combustíveis:
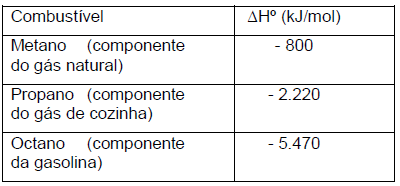
Com base nesses dados, são feitas as seguintes afirmativas:
I. O poder calorífico do Propano é maior que do Octano. II. A queima de um mol de Metano absorve cerca de 50 kJ de energia. III. A energia proveniente da queima de 1 kg de Metano é cerca de 2,8 vezes menor que a energia da queima de 1 kg de Propano.
Assinale a alternativa em que toda(s) a(s) afirmativa(s) está(ão) CORRETA(S):

Com base nesses dados, são feitas as seguintes afirmativas:
I. O poder calorífico do Propano é maior que do Octano. II. A queima de um mol de Metano absorve cerca de 50 kJ de energia. III. A energia proveniente da queima de 1 kg de Metano é cerca de 2,8 vezes menor que a energia da queima de 1 kg de Propano.
Assinale a alternativa em que toda(s) a(s) afirmativa(s) está(ão) CORRETA(S):
Provas
Questão presente nas seguintes provas
A figura abaixo representa um
cromatograma obtido por cromatografia gasosa e
correspondente à separação de uma mistura
contendo dois componentes x e y. Este fato tem
como base a distribuição seletiva dos diferentes
componentes de uma amostra entre duas fases
imiscíveis.
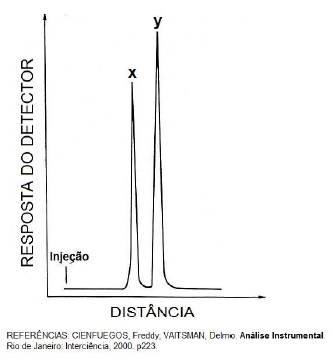
Com base no que foi exposto, são feitas as seguintes afirmações:
I. Neste caso, a fase móvel é um gás, e a fase fixa pode ser um sólido ou líquido não volátil. II. A figura mostra que o componente y foi mais retido pela coluna cromatográfica. III. Os componentes x e y devem ser polares. IV. A capacidade de separar os componentes x e y depende das respostas do detector. V. O gás de arraste numa análise cromatográfica precisa ser puro e ter inércia química.
Assinale a alternativa que apresenta somente afirmações CORRETAS.

Com base no que foi exposto, são feitas as seguintes afirmações:
I. Neste caso, a fase móvel é um gás, e a fase fixa pode ser um sólido ou líquido não volátil. II. A figura mostra que o componente y foi mais retido pela coluna cromatográfica. III. Os componentes x e y devem ser polares. IV. A capacidade de separar os componentes x e y depende das respostas do detector. V. O gás de arraste numa análise cromatográfica precisa ser puro e ter inércia química.
Assinale a alternativa que apresenta somente afirmações CORRETAS.
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma grande variedade de bebidas
industrializadas contém açúcar (sacarose -
C12H22O11) na sua composição. São exemplos
refrigerantes, néctares e concentrados de fruta.
Um técnico em química, responsável pelo
controle de qualidade de uma empresa,
determinou a quantidade média de sacarose de
duas versões de um refrigerante:
“Normal”: 60 g de sacarose em frascos de 500 mL. “Light” (teor reduzido de açúcar): 100 g de sacarose em frascos de 1 L. Dado: densidade do refrigerante a 20 °C = 1,04 g/mL
Assinale a alternativa em que a afirmativa está INCORRETA:
“Normal”: 60 g de sacarose em frascos de 500 mL. “Light” (teor reduzido de açúcar): 100 g de sacarose em frascos de 1 L. Dado: densidade do refrigerante a 20 °C = 1,04 g/mL
Assinale a alternativa em que a afirmativa está INCORRETA:
Provas
Questão presente nas seguintes provas
É comum em laboratórios de química o
emprego de diversas vidrarias, cada uma delas
apropriada para um tipo de uso. Abaixo são
explicitadas algumas vidrarias (primeira coluna)
que servem para realização de algumas ações
específicas (segunda coluna). Relacione a
segunda coluna com a primeira, levando em
conta a vidraria adequada para cada finalidade.
PRIMEIRA COLUNA I. Bureta. II. Proveta. III. Balão volumétrico. IV. Pipeta graduada. V. Pipeta volumétrica.
SEGUNDA COLUNA ( ) Livrar volumes fixos com precisão. ( ) Livrar volumes variados com precisão. ( ) Livrar volumes variados. ( ) Conter ou livrar volumes variados. ( ) Conter volumes fixos com precisão.
Assinale a alternativa que apresenta a associação CORRETA entre a vidraria (primeira coluna) e a sua função (segunda coluna), na ordem de cima para baixo.
PRIMEIRA COLUNA I. Bureta. II. Proveta. III. Balão volumétrico. IV. Pipeta graduada. V. Pipeta volumétrica.
SEGUNDA COLUNA ( ) Livrar volumes fixos com precisão. ( ) Livrar volumes variados com precisão. ( ) Livrar volumes variados. ( ) Conter ou livrar volumes variados. ( ) Conter volumes fixos com precisão.
Assinale a alternativa que apresenta a associação CORRETA entre a vidraria (primeira coluna) e a sua função (segunda coluna), na ordem de cima para baixo.
Provas
Questão presente nas seguintes provas
Átomos das famílias 14, 15, 16 e 17 da
Tabela Periódica, que se encontram até o terceiro
período, podem formar ligações duplas ou triplas.
Em qual das alternativas há a ocorrência de
apenas uma ligação dupla na molécula formada
por átomos destas famílias e períodos da Tabela
Periódica?
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
- Química OrgânicaHidrocarbonetos
O quadro abaixo relaciona a fórmula
estrutural com exemplos de aplicação no
cotidiano dos compostos orgânicos:
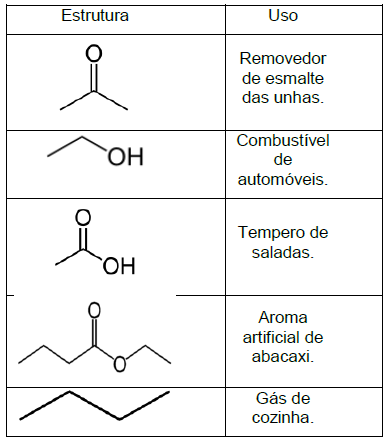
A sequência CORRETA que apresenta o nome dos compostos orgânicos, de cima para baixo, é:

A sequência CORRETA que apresenta o nome dos compostos orgânicos, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
Um técnico em química teve a tarefa de
armazenar diferentes substâncias. Para tanto,
resolveu separá-las de acordo com as
respectivas funções químicas. As substâncias
eram: NaCl, CaCO3, Ca(OH)2, CaO, Na2O, NaOH,
H2SO4 e HCl.
A alternativa que apresenta apenas as substâncias classificados como óxidos é:
A alternativa que apresenta apenas as substâncias classificados como óxidos é:
Provas
Questão presente nas seguintes provas
Os metais alcalinos são extremamente
reativos, inclusive com a água. Qual das
alternativas apresenta a equação química que
representa corretamente a reação de um desses
metais com água?
Provas
Questão presente nas seguintes provas
Os métodos colorimétricos e
espectrofotométricos, frequentemente usados,
são muito importantes para as análises químicas
quantitativas. Assinale a alternativa que expressa
CORRETAMENTE o princípio básico desses
métodos.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container