Foram encontradas 40 questões.
De acordo com determinada abordagem do processo ensino e aprendizagem, privilegia-se um ou outro aspecto do fenômeno educacional (Mizukami, 1986). Analise a concepção de avaliação nas diferentes abordagens e numere corretamente a coluna da esquerda de acordo com a da direita.
( ) O professor deverá considerar as soluções erradas ou incompletas dos alunos, pois não se pode deixar de levar em conta os diferentes estágios de desenvolvimento.
( ) O aluno assume responsabilidade pelas formas de controle de sua aprendizagem.
( ) A avaliação é elemento constituinte da própria aprendizagem, pois fornece dados para o próximo comportamento a ser modelado.
( ) A avaliação é realizada visando à reprodução do conteúdo comunicado em sala de aula.
( ) A avaliação consiste na autoavaliação ou avaliação mútua da prática educativa por professor e alunos.
1. Abordagem Tradicional
2. Abordagem Comportamentalista
3. Abordagem Humanista
4. Abordagem Cognitivista
5. Abordagem Sociocultural.
A ordem CORRETA de associação, de cima para baixo, é:
( ) O professor deverá considerar as soluções erradas ou incompletas dos alunos, pois não se pode deixar de levar em conta os diferentes estágios de desenvolvimento.
( ) O aluno assume responsabilidade pelas formas de controle de sua aprendizagem.
( ) A avaliação é elemento constituinte da própria aprendizagem, pois fornece dados para o próximo comportamento a ser modelado.
( ) A avaliação é realizada visando à reprodução do conteúdo comunicado em sala de aula.
( ) A avaliação consiste na autoavaliação ou avaliação mútua da prática educativa por professor e alunos.
1. Abordagem Tradicional
2. Abordagem Comportamentalista
3. Abordagem Humanista
4. Abordagem Cognitivista
5. Abordagem Sociocultural.
A ordem CORRETA de associação, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
A equação de Clapeyron para os gases ideias leva em conta a hipótese de Avogadro que diz: “Volumes iguais de gases diferentes nas mesmas condições de pressão e temperatura contêm o mesmo número de moléculas”. Esta equação, no entanto, não se aplica de forma adequada aos gases reais, para os quais se apresenta a seguinte equação:
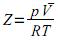
A respeito dos gases ideais e reais, assinale a alternativa CORRETA.
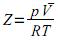
A respeito dos gases ideais e reais, assinale a alternativa CORRETA.
Provas
Questão presente nas seguintes provas
Em uma escola de Ensino Técnico Integrado ao Ensino Médio, um trabalho foi proposto com o intuito de desenvolver competências em Educação Ambiental. O tema escolhido para trabalhar com adolescentes de três turmas das 3as fases foi “Como descartar corretamente pilhas e baterias”. Para ajudar na reflexão sobre os riscos ambientais desses materiais foi elaborada uma cartilha e os alunos foram informados sobre o local na cidade onde podem levar suas pilhas e baterias usadas. Nessa cartilha, vários conceitos da eletroquímica foram explicados, bem como os efeitos do descarte inadequado destes materiais. Leia com atenção as afirmações a seguir e marque V para as verdadeiras e F para as falsas, conforme os conceitos sobre as pilhas e baterias.
( ) As pilhas que não podem ser recarregadas são classificadas como sistemas eletroquímicos primários ou baterias primárias.
( ) O destino ideal de pilhas e baterias usadas deveria ser o aterro controlado, pois todo o lixo recebe uma cobertura de PVC ou argila, o que evita contaminação do ambiente.
( ) As baterias de níquel/cádmio são baterias secundárias e de longa duração.
( ) Na pilha alcalina não há formação de gás hidrogênio, pois o meio é básico.
( ) Nas pilhas de mercúrio, usadas em relógios e calculadoras, o mercúrio é oxidado a óxido de mercúrio, que é solúvel e pode contaminar o solo se descartada incorretamente.
Assinale a opção que contenha a sequência CORRETA de cima para baixo.
( ) As pilhas que não podem ser recarregadas são classificadas como sistemas eletroquímicos primários ou baterias primárias.
( ) O destino ideal de pilhas e baterias usadas deveria ser o aterro controlado, pois todo o lixo recebe uma cobertura de PVC ou argila, o que evita contaminação do ambiente.
( ) As baterias de níquel/cádmio são baterias secundárias e de longa duração.
( ) Na pilha alcalina não há formação de gás hidrogênio, pois o meio é básico.
( ) Nas pilhas de mercúrio, usadas em relógios e calculadoras, o mercúrio é oxidado a óxido de mercúrio, que é solúvel e pode contaminar o solo se descartada incorretamente.
Assinale a opção que contenha a sequência CORRETA de cima para baixo.
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
As amidas são compostos relativamente pouco reativos dentre os derivados de ácidos carboxílicos, sendo abundante nos seres vivos devido a uma grande estabilidade encontrada nos sistemas orgânicos. Muitos fármacos, como a benzilpenicilina (penicilina G) possuem grupamentos amida em sua estrutura.
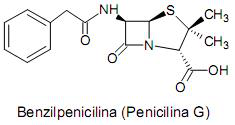
As amidas podem ser preparadas pela reação de um cloreto de ácido com uma amina, então, na intensão de produzir um repelente de insetos muito utilizado pela indústria cosmética conhecido como DEET, com nomenclatura IUPAC de N,N-dietil-3-metilbenzamida, assinale a alternativa CORRETA que indica quais reagentes um químico deve procurar em seu almoxarifado:

As amidas podem ser preparadas pela reação de um cloreto de ácido com uma amina, então, na intensão de produzir um repelente de insetos muito utilizado pela indústria cosmética conhecido como DEET, com nomenclatura IUPAC de N,N-dietil-3-metilbenzamida, assinale a alternativa CORRETA que indica quais reagentes um químico deve procurar em seu almoxarifado:
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Em uma aula prática, os alunos foram divididos em equipes e cada uma deveria preparar 500 mL de uma solução de NaOH 2M. Uma das equipes utilizou essa solução para titular 10 mL de uma solução padronizada de H2SO4 2M. Nessa titulação, foram gastos 25 mL da solução preparada. Com base nesses dados, assinale a alternativa CORRETA.
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias Inorgânicas
- Sistemas de EquilíbrioSistemas Heterogêneos: Produto de Solubilidade (Kps)
Avalie as asserções abaixo.
Se um precipitado de cromato de prata está em equilíbrio com sua solução saturada, pode-se afirmar que há um equilíbrio heterogêneo
PORQUE
o Ag2CrO4 está na fase sólida, enquanto íons Ag⁺ e CrO42⁻ estão na fase dissolvida, sendo a expressão do produto de solubilidade igual à soma das concentrações molares dos íons. Assinale a alternativa CORRETA.
Se um precipitado de cromato de prata está em equilíbrio com sua solução saturada, pode-se afirmar que há um equilíbrio heterogêneo
PORQUE
o Ag2CrO4 está na fase sólida, enquanto íons Ag⁺ e CrO42⁻ estão na fase dissolvida, sendo a expressão do produto de solubilidade igual à soma das concentrações molares dos íons. Assinale a alternativa CORRETA.
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma técnica de laboratório depara-se com um grande frasco de uma solução de ácido clorídrico com um rótulo onde constava a concentração em porcentagem em massa: 28% (m/m). Com o objetivo de determinar a concentração em quantidade de matéria da solução, a técnica afere a densidade da solução, encontrando o valor de 1,3 g/mL. Qual a concentração da solução em questão? (dado: HCl = 36,5 g/mol)
Assinale a alternativa CORRETA.
Assinale a alternativa CORRETA.
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Em um laboratório de química precisamos preparar soluções de concentrações variadas. Associe a coluna da direita com a da esquerda de acordo com as características finais das soluções que devemos preparar, considerando que a massa molar do NaOH como 40 g/mol.
( 1 ) NaOH 0,1 mol/L
( 2 ) NaOH 3%
( 3 ) NaOH 50 mM
( 4 ) NaOH 5 g/L
( ) Diluir 25 µL de uma solução a 3 mol/L e diluir até 100 µL.
( ) Diluir 50 mL de uma solução a 16 g/L até 200 mL.
( ) Diluir 10 mL de uma solução a 1,25 mol/L até 100 mL.
( ) Diluir 2 mL de solução a 25 % até 250 mL.
A ordem CORRETA de associação, de cima para baixo, é:
( 1 ) NaOH 0,1 mol/L
( 2 ) NaOH 3%
( 3 ) NaOH 50 mM
( 4 ) NaOH 5 g/L
( ) Diluir 25 µL de uma solução a 3 mol/L e diluir até 100 µL.
( ) Diluir 50 mL de uma solução a 16 g/L até 200 mL.
( ) Diluir 10 mL de uma solução a 1,25 mol/L até 100 mL.
( ) Diluir 2 mL de solução a 25 % até 250 mL.
A ordem CORRETA de associação, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
O hipoclorito de sódio é empregado como desinfetante e desodorante nas indústrias alimentícias, empresas de abastecimento de água, rejeitos de esgoto e em atividades domésticas. Como agente alvejante é muito útil para ser usado com o algodão, o linho, a juta, a seda artificial e a polpa de papel. O método mais comum para fabricá-lo é mediante o tratamento da solução de hidróxido de sódio pelo cloro gasoso, conforme a reação:
Cl2 + 2NaOH ? NaCl + H2O + NaClO
O outro método de produção é a eletrólise de uma solução concentrada de cloreto de sódio, com o que se obtêm o mesmo produto.
Sobre esse segundo método de produção do hipoclorito de sódio, assinale a alternativa CORRETA.
Cl2 + 2NaOH ? NaCl + H2O + NaClO
O outro método de produção é a eletrólise de uma solução concentrada de cloreto de sódio, com o que se obtêm o mesmo produto.
Sobre esse segundo método de produção do hipoclorito de sódio, assinale a alternativa CORRETA.
Provas
Questão presente nas seguintes provas
No gerenciamento de águas e efluentes de uma indústria, o químico determinou que uma das análises necessárias a serem executadas era a avaliação da água de lavagem de um reator, com a finalidade de se determinar se esta poderia ser descartada no meio ambiente. Encontrou-se numa dessas águas a concentração de 2,0 × 10-9 mol/L de HNO3. Qual o valor de pH desta água?
Assinale a alternativa CORRETA.
Assinale a alternativa CORRETA.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container