Foram encontradas 40 questões.
Os antiácidos estomacais, conhecidos popularmente como “sais de frutas”, são medicamentos indicados para as pessoas que apresentam os sintomas de azia, má digestão e acidez estomacal. Os sais de frutas podem ser ingeridos na forma de comprimido ou em pó efervescente. Antes de serem ingeridos, eles são colocados em contato com a água para iniciar uma reação química e, assim, estarem prontos para serem ingeridos. Com base nessas informações, assinale a alternativa abaixo que representa a ocorrência da reação química mais rapidamente:
Provas
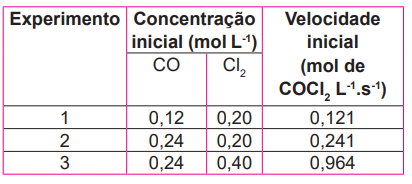
O gás cloreto de carbonila, mesmo sendo muito tóxico, é usado como precursor de síntese de vários compostos orgânicos. Abaixo, temos a reação de síntese do cloreto de carbonila, a partir da reação entre o CO e Cl2 em uma determinada temperatura. Analise os dados experimentais da tabela e assinale a alternativa que possui a ordem de reação.
CO(g) + CI2(g) → COCI2(g)
Provas
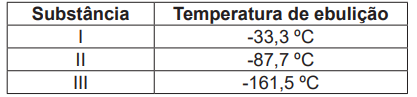
As interações intermoleculares influenciam diversas propriedades físico-químicas das substâncias, como temperatura de fusão e de ebulição, viscosidade, solubilidade, dentre outras propriedades. A tabela a seguir apresenta a temperatura de ebulição de três substâncias, denominadas I, II e III.
Fonte: ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de Química: Questionando a vida moderna e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018. p.191.
Considerando a relação existente entre as interações intermoleculares e a temperatura de ebulição, e comparando a temperatura de ebulição das três substâncias, assinale a alternativa que identifica, corretamente, a fórmula química das substâncias I, II e III. São dados os números atômicos dos elementos químicos H (Z=1), C (Z=6), N (Z=7) e P (Z=15).
Provas
Quantas horas de eletrólise são necessárias para produzir 6,0 gramas de magnésio metálico a partir de cloreto de magnésio fundido, utilizando uma corrente de 10,0 A? Considere que a massa molar do magnésio seja 24,0 g mol-1 e a constante de faraday seja 96500 C mol-1.
Provas
Cloratos metálicos são agentes oxidantes fortes e podem ser preparados por reações de neutralização, envolvendo um ácido e uma base de Arrhenius. Para preparar o sal clorato férrico, assinale a alternativa que contém o ácido e a base de Arrhenius que devem ser utilizados na reação de neutralização.
Provas
Um estudante de química deseja neutralizar parcialmente uma solução básica para utilizá-la em seu experimento no laboratório de química. Inicialmente, ele possui 800 mL de uma solução aquosa de hidróxido de sódio de concentração molar de 0,25 mol L-1. Para neutralizar parcialmente esta solução básica, o aluno vai utilizar 200 mL de solução aquosa de ácido clorídrico de concentração molar de 0,50 mol L-1. Após a neutralização parcial, escolha a alternativa que apresente o valor correto de pH da solução resultante:
Provas
Dois diferentes frascos limpos, secos e hermeticamente fechados contém em equilíbrio as espécies referentes às reações químicas conforme a seguir:
Frasco A: REAÇÃO A : H2(g) + I2(g) ⇌ 2HI(g)
Frasco B: REAÇÃO B: 2NO2(g) ⇌ 2NO(g) + O2(g)
Considere os gases como ideias.
Se o volume de cada frasco for reduzido para um terço do volume inicial, é possível observar que:
Provas
Em um reator estão presentes os gases H2, I2 e HI em equilíbrio químico. Medidas foram realizadas para descobrir as concentrações dos gases e os seguintes resultados foram encontrados: [I2] = 1,6 x 10-3 mol L-1, [HI] = 2,0 x 10-3 mol L-1 e [H2] = 5,0 x 10-5 mol L-1. Sabendo que a temperatura dentro do reator é de 700 K, assinale a alternativa que apresenta o valor da constante de equilíbrio de formação do HI.
Provas
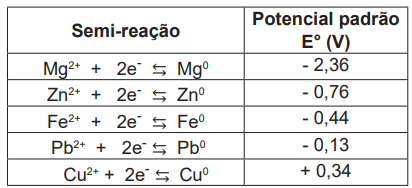
Peças metálicas constituídas do metal ferro são afetadas, com o passar do tempo, pelo processo de corrosão. Para a proteção dessas peças, podem ser utilizados outros metais que evitam ou postergam a corrosão. Estes metais adicionados são chamados de metais ou eletrodos de sacrifício. Considere os potenciais-padrão de redução dos metais na tabela a seguir:
Fonte: JONES, L.; ATKINS, P. Princípios de Química:
Questionando a vida moderna e o meio ambiente. 5. Ed.
Porto Alegre: Bookman, 2012. p.532.
Os metais adequados para proteger essas peças metálicas contra a corrosão são:
Provas
A cal virgem, também conhecida como óxido de cálcio (CaO) é um composto com aplicações em diversas áreas, como na indústria agrícola, siderúrgica, química, construção civil, no tratamento de resíduos e na indústria de papel e celulose. Sua produção se dá a partir do carbonato de cálcio (CaCO3), que é decomposto termicamente em cal virgem (CaO) e gás carbônico (CO2), de acordo com a reação química:
CaCO3(s) → CaO(s) + CO2(g)
A produção da cal virgem gera gás carbônico, um gás conhecido pelo seu papel na intensificação do efeito estufa. Qual o volume aproximado, nas CNTP, de gás carbônico produzido a partir da decomposição térmica de 250 kg de carbonato de cálcio? Utilize as massas molares (g mol-1) dos elementos C = 12, O = 16 e Ca = 40. Considere o rendimento da reação igual a 100 %, o comportamento do gás é ideal e a constante dos gases R = 0,082 atm L mol-1 K-1.
Provas
Caderno Container