Foram encontradas 39 questões.
Leia: “A avaliação dá grande flexibilidade de julgamento ao professor devendo ser praticada com responsabilidade. Um dos exemplos disso é o costumeiro “arredondamento de notas”, que consiste em o professor aumentá-las ou diminuí-las segundo critérios por ele definidos e nem sempre explicitados. Esse arredondamento é feito com base nessa modalidade de avaliação (VILLAS BOAS, 2006).” – Lemos, P. S.; Sá, L. P., 2013.
A que tipo de avaliação se refere o texto acima?
Provas
Questão presente nas seguintes provas
Dentre os eletrodos de segunda classe, utilizados como referência, destaca-se o eletrodo de prata/cloreto de prata.
Considerando que o produto de solubilidade do AgCl é 1,8 x 10-10 M2 e que o potencial de redução da prata é de +0,80 V, qual a equação que expressa o potencial padrão de redução deste eletrodo?
Provas
Questão presente nas seguintes provas
A figura abaixo refere-se à titulação de um ácido fraco com uma base forte.
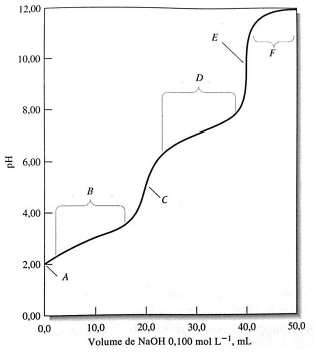
A partir da interpretação dos dados descritos na curva de titulação, qual alternativa está correta?
Provas
Questão presente nas seguintes provas
Foi estudada, em diferentes condições de análise, a reação gasosa xX + yY → wW + zZ obtendo-se os seguintes resultados:
| Concentração inicial (mol . L-1) |
Velocidade Inicial
(mol . L-1 . h-1)
|
||
| [X] | [Y] | ||
| 3 x 10-3 | 3 x 10-3 | 9 x 10-5 | |
| 6 x 10-3 | 3 x 10-3 | 36 x 10-5 | |
| 6 x 10-3 | 6 x 10-3 | 144 x 10-5 | |
De acordo com esses dados, a constante de velocidade da reação acima é igual a
Provas
Questão presente nas seguintes provas
O alumínio pode ser determinado por titulação com solução de sal dissódico de EDTA. Uma amostra de 1,00 g contendo Al2O3 requer 20,50 mL de solução de EDTA. Para titular 25,00 mL de uma solução 0,1000 mol L-1 de CaCl2 se gastou 30,00 mL de EDTA.
Qual a percentagem de Al2O3 na amostra?
Provas
Questão presente nas seguintes provas
Quando o ácido oxálico é titulado com uma base forte sua curva de titulação (pH vs. volume gasto de titulante) apresenta duas zonas de tamponamento, decorrentes da presença de pares conjugados produzidos durante a reação de neutralização.
Com base no valor das constantes de ionização do referido ácido (5,6 x 10-2 M e 5,2 x 10-5 M), o potencial hidrogeniônico na região de tamponamento, onde os íons oxalato e mono-hidrogeno-oxalato estão presentes em quantidades equimolares, é
Provas
Questão presente nas seguintes provas
O ácido nítrico pode ser obtido a partir da amônia por meio das seguintes etapas:
Etapa I: 6NH3(g) + 15/2O2(g) !$ \rightleftharpoons !$ 6NO(g) + 9H2O(g) !$ \Delta H !$ = - 1359 kJ
Etapa II: 3 NO(g) + 3/2 O2(g) !$ \rightleftharpoons !$ 3 NO2(g) !$ \Delta H !$ = - 170 kJ
Etapa III: 3NO2(g) + H2O(g) !$ \rightleftharpoons !$ 2HNO3(g) + NO(g) !$ \Delta H !$ = - 135 kJ
Considerando a etapa global de produção do ácido nítrico, totalmente ionizável em água e em equilíbrio, é correto afirmar que
Provas
Questão presente nas seguintes provas
Você está se preparando para acampar e precisa levar gás butano para aquecer água. Considere que, para aquecer 1 L de água de 17°C até a temperatura de ebulição (ignorando as perdas de calor), é necessário obter 400 kJ de calor e que a equação termoquímica de combustão do butano é: 2 C4H10 (g) + 13 O2 (g) → 8 CO2 (g) + 10 H2O (l) !$ \Delta H° !$ = - 5756 kJ
A quantidade, em massa (g), de butano necessária para aquecer a água será aproximadamente igual a
Provas
Questão presente nas seguintes provas
Niels Bohr foi um físico dinamarquês responsável por aperfeiçoar a teoria atômica proposta por Rutherford (sistema planetário), que se tornou falha para explicar, dentre outras coisas, o porquê de o elétron não perder energia durante os movimentos de rotação em torno do núcleo e colidir com ele, mas permanecer em órbita constante sem tornar o átomo instável. Baseando-se nos fundamentos de Max Planck, Bohr reformulou a teoria atômica estabelecendo alguns postulados.
Qual alternativa apresenta corretamente um dos postulados de Bohr?
Provas
Questão presente nas seguintes provas
Um volume de 10,0 mL de uma solução alcoólica é diluído em água até 500,0 mL (solução A). Uma alíquota de 10,0 mL da solução A é destilada e o etanol é coletado em 50,00 mL de uma solução ácida (H2SO4) contendo K2Cr2O7 0,1000 eq L-1, onde é oxidado à ácido acético. O excesso de K2Cr2O7 não reagido é titulado com 16,24 mL de Fe2+ 0,1006 eq L-1, conforme descrevem as reações abaixo:
2Cr2O72- + 3C2H5OH + 16H+ → 4Cr3+ + 3CH3COOH + 11H2O
Cr2O72- + 6Fe2+ + 14H+ → 2Cr3+ + 6Fe3+ + 7H2O
Qual a percentagem (%p/v) de etanol na amostra?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container