Foram encontradas 80 questões.
Considere a célula voltaica descrita pela notação eletroquímica a seguir:
Ni(s) | Ni2+ (aq) || Ag+ (aq) | Ag(s)
Sabendo que essa célula opera sob condições-padrão e a 25 °C, assinale a alternativa que apresenta o valor aproximado da variação de energia livre padrão (\( \Delta Gº \)) para a reação desenvolvida nessa célula.
Dados:
Constante Faraday (F) = 96.485 C/mol elétron.
Potenciais-padrão redução (25 °C):
E° (Ag+/Ag0) = +0,80 V.
E° (Ni2+/Ni0) = −0,25 V.
Provas
Em uma investigação forense, foi utilizado o corante vermelho do Nilo (Nile red) para a detecção de impressões digitais em diferentes superfícies. Esse corante apresenta a seguinte estrutura molecular:
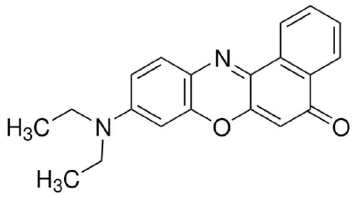
A partir dessa estrutura molecular, de suas propriedades e do conhecimento sobre ligações químicas e estereoquímica, assinale a alternativa INCORRETA.
Provas
Os óxidos são substâncias formadas pela combinação do oxigênio, elemento mais eletronegativo, com outro elemento. Eles podem ser classificados em óxidos ácidos, básicos, anfóteros e neutros. Com base nessa classificação, assinale a alternativa que apresenta um óxido anfótero.
Provas
Em relação às características das ligações iônicas e à estabilidade dos sólidos iônicos, designada pela energia de rede, analise as assertivas e assinale a alternativa que aponta a(s) correta(s).
I. A energia de rede de um sólido iônico não depende dos raios iônicos.
II. A energia de rede do LiCl é menor que a energia de rede do CsCl.
III. A força de atração eletrostática entre os íons no sólido MgO é maior quando comparada aos íons do sólido Na2O.
Provas
A reação entre o fósforo branco e o gás cloro é demonstrada na equação química (não balanceada) a seguir:
P4(s) + Cl2(g) → PCl3(l)
Com base na estequiometria dessa reação, assinale a alternativa que apresenta a massa aproximada de gás cloro necessária para reagir completamente com 8,0x1024 moléculas de fósforo branco.
Dados: NA = 6,0x1023 mol−1.
Provas
Em uma titulação, a mudança de cor de um indicador químico ocasiona um erro absoluto constante de +0,03 ml na leitura do volume do titulante. Tendo em vista essa situação, assinale a alternativa que apresenta o erro relativo percentual quando o volume total de titulante é 25,00 ml.
Provas
João é o perito responsável por uma investigação criminal e, para proceder à análise pericial, necessita utilizar vários reagentes, dentre eles o ácido nítrico. Para esse propósito, foi necessário preparar 500 ml de uma solução de HNO3 0,10 mol/L a partir do ácido nítrico concentrado (pureza 70% m/m; d = 1,40 g/ml). Considerando essas informações, assinale a alternativa que apresenta o volume aproximado de ácido nítrico concentrado necessário para obter a referida solução.
Provas
Todos os complexos a seguir são tetraédricos, formados por ligantes de campo fraco, e apresentam configuração de spin alto. Com base nessas informações, assinale a alternativa que apresenta o único complexo diamagnético.
Provas
Uma solução aquosa de hipobromito de sódio (NaOBr), com concentração de 0,20 mol/L a 25 °C, encontra-se completamente dissociada. Considerando essa informação e que há um equilíbrio estabelecido entre os íons em solução, assinale a alternativa correta.
Dados (a 25 °C): Ka (HOBr) = 2,0x10−9; Kw = 1,0x10−14.
Provas
Considerando os seguintes métodos volumétricos de análise e a aplicação desses métodos, relacione as colunas e assinale a alternativa com a sequência correta.
1. Método argentométrico de Mohr.
2. Complexometria.
3. Volumetria ácido-base.
4. Volumetria de oxirredução.
( ) Determinação da alcalinidade total da água.
( ) Determinação de íons Ca2+ e Mg2+ em água.
( ) Determinação de íons Fe (II) com dicromato de potássio.
( ) Determinação de íons cloreto.
Provas
Caderno Container