Foram encontradas 290 questões.
- FundamentosPropriedades das Substâncias
- Química CinéticaTransformações Químicas
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Química OrgânicaCadeias Carbônicas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
- Transformações Químicas e EnergiaTermoquímica
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
O carbureto (carbeto de cálcio) é um sólido empregado tanto para iluminação quanto para processos de solda, devido à formação de acetileno (C2H2), quando da sua exposição à água, de acordo com a equação não balanceada:
CaC2(s) + H2O(l) → Ca(OH)2(aq) + C2H2(g)
Uma amostra de 10g de um sólido contendo 40,0% de carbeto de cálcio foi colocada em 200g de água, produzindo acetileno. Considere que as impurezas são imiscíveis em água e não interferem na produção de acetileno e que, na reação, todo o carbureto foi convertido em acetileno. Com base no exposto, a quantidade mais próxima de acetileno produzida e o pH do meio aquoso após a reação serão: Dados:massas molares: H: 1g/mol; C: 12g/mol; O: 16g/mol; Ca:40g/mol
solubilidade do Ca(OH)2(aq) = 1,2g/L
Provas
- FundamentosPropriedades das Substâncias
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
O ferro metálico pode ser obtido industrialmente por meio da seguinte reação não balanceada:
Fe2O3(s) + CO(g) → Fe(s) + CO2(g)
Considerando uma reação com transformação
total de produtos em reagentes, assinale a
alternativa correta sobre esse processo.
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Em uma ação policial para combate ao tráfico de substâncias psicoativas (“drogas de abuso”), foram apreendidos 10.000 (dez mil) tubos plásticos, de formato cônico, do tipo eppendorf, com volume de 1,5 mL, cujo interior apresentava sólido pulverizado de coloração bege, que preenchia um volume de 1,0 mL de cada um dos tubos. Durante o exame preliminar do material, foram feitas as seguintes observações:
• Todos os tubos apresentavam as mesmas dimensões e foram preenchidos com o mesmo volume, massa e tipo de pó.
• A massa do material apreendido (correspondente à soma da massa dos tubos e do pó contido em todos os tubos) era de 15.000g (quinze mil gramas).
• A massa de 10 tubos, obtida após a remoção completa do pó de cada um deles, era de 10,0g.
Além disso, por meio de técnicas de amostragem e analíticas, determinou-se que o pó, em todos os tubos, apresentava um teor de cocaína de 5,0%.
Provas
- Química OrgânicaCadeias Carbônicas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
- Química OrgânicaPropriedades Químicas dos Compostos Orgânicos
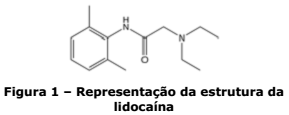
Sobre essa substância, são feitas as seguintes afirmações:
I. Apresenta as funções amina e cetona.
II. Sua fórmula química é: C14H22N2O.
III. Nem todos os átomos dessa molécula estão contidos em um único plano.
IV. Apresenta caráter ácido.
Quais estão corretas?
Provas
Um perito resolveu usar o cloreto de etila (I) como modelo de estrutura química para testar um software de previsão de espectros de Ressonância Magnética Nuclear de 1H. A partir dessa molécula, foram feitas substituições que originaram outros compostos similares (II, III, IV, V e VI), que também foram testados.
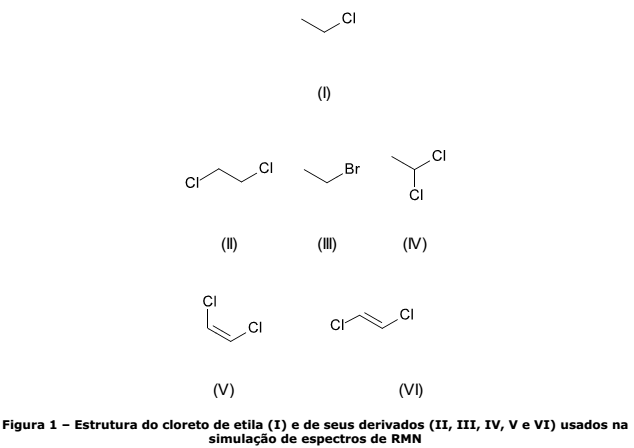
Os testes do software não incluíam sobreposição de espectros de solventes, nem de agentes como o TMS. Considerando as moléculas e as observações teóricas feitas pelo perito, assinale a alternativa INCORRETA.
Provas
Considere os seguintes tipos de materiais vegetais:
• Folhas de coca (Erythroxylum coca), das quais se extraem o alcalóide cocaína (observação: comporta-se como base fraca).
• Folhas de maconha (Cannabis sativa) das quais se obtém diferentes canabinóides, dentre os quais, o delta-9 tetraidrocanabinol (delta-9 THC), molécula de baixa hidrossolubilidade.
Para a extração dos princípios ativos desses materiais vegetais, um laboratório forense dispõe dos seguintes sistemas de solventes para extração:
I. Clorofórmio acrescido de ácido acético glacial (H3C-COOH).
II. Clorofórmio (CHCl3) acrescido de hidróxido de amônio.
III. Clorofórmio puro (CHCl3).
IV. Tolueno (hidrocarboneto aromático de fórmula: C7H8).
V. Solução aquosa 10-5 mol/L de ácido clorídrico.
VI. Solução aquosa 10-5 mol/L de hidróxido de sódio.
VII. Água pura.
Considerando que os sistemas de solventes já foram exaustivamente testados e que não causarão degradação dos princípios ativos e que os protocolos de extração do laboratório preveem o uso sempre da mesma quantidade de material vegetal e de solventes (todos em temperatura ambiente) para todas as metodologias de extração, assinale a alternativa INCORRETA.
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Em um laboratório de análise química, há três tambores plásticos (X, Y e Z) destinados ao descarte de soluções e nos seus rótulos se lê os seguintes dizeres:
• Tambor X: descarte de soluções ácidas.
• Tambor Y: descarte de soluções básicas.
• Tambor Z: descarte de soluções neutras.
Ao perito desse laboratório, foi solicitado que fizesse o descarte de 3 soluções aquosas (1, 2 e 3), cujas características são descritas a seguir:
• Solução 1: cloreto de sódio 0,1 mol/L.
• Solução 2: mistura de 50 mL de ácido clorídrico 0,2 mol/L, com 20 mL de hidróxido de sódio 0,5 mol/L.
• Solução 3: glicose 0,1 mol/L (lembrando que a glicose é poliálcool que apresenta ainda um grupo aldeído (C6H12O6(aq))).
Considerando que o correto descarte tenha sido feito pelo perito, assinale a alternativa correta.
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Em uma ação policial para combate ao tráfico de substâncias psicoativas (“drogas de abuso”), foram apreendidos 10.000 (dez mil) tubos plásticos, de formato cônico, do tipo eppendorf, com volume de 1,5 mL, cujo interior apresentava sólido pulverizado de coloração bege, que preenchia um volume de 1,0 mL de cada um dos tubos. Durante o exame preliminar do material, foram feitas as seguintes observações:
• Todos os tubos apresentavam as mesmas dimensões e foram preenchidos com o mesmo volume, massa e tipo de pó.
• A massa do material apreendido (correspondente à soma da massa dos tubos e do pó contido em todos os tubos) era de 15.000g (quinze mil gramas).
• A massa de 10 tubos, obtida após a remoção completa do pó de cada um deles, era de 10,0g.
Além disso, por meio de técnicas de amostragem e analíticas, determinou-se que o pó, em todos os tubos, apresentava um teor de cocaína de 5,0%.
Provas
- Química OrgânicaCadeias Carbônicas
- Química OrgânicaPropriedades Físicas dos Compostos Orgânicos
- Química OrgânicaReações OrgânicasReações Orgânicas: Substituição, Adição e Eliminação
- Química OrgânicaReações OrgânicasReações Orgânicas: Oxidação, Redução e Polimerização
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Álcoois são de grande versatilidade do ponto de vista sintético, pois podem participar de uma série de reações. Exemplos dessa versatilidade são mostrados nas reações não balanceadas nas quais apenas o produto principal é mostrado:

Sobre essa reação e os compostos nela envolvidos, assinale a alternativa INCORRETA.
Provas
Caderno Container