Foram encontradas 504 questões.
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
No processamento industrial de um ácido carboxílico obteve-se a molécula cuja fórmula estrutural é apresentada a seguir.
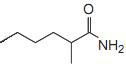
Essa molécula pertence à função orgânica

Essa molécula pertence à função orgânica
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Em um laboratório foi realizado o preparo de uma solução aquosa de H2SO4 diluída. Essa solução foi preparada a partir de uma solução aquosa concentrada do mesmo ácido (com concentração de 98% m/m e densidade de 1,85 g/mL). No preparo da solução, uma alíquota de 20 mL da solução concentrada foi dissolvida em água até completar o volume de 250 mL de solução. A concentração, em mol/L, da solução diluída é igual a
A concentração, em mol/L, da solução diluída é igual a
Dado
massa molar do H2 SO4 = 98 g/mol
A concentração, em mol/L, da solução diluída é igual a
Dado
massa molar do H2 SO4 = 98 g/mol
Provas
Questão presente nas seguintes provas
Os comprimidos efervescentes têm em sua constituição substâncias que, quando colocadas em água, reagem com evolução de gás carbônico. Um experimento comparativo foi realizado separando quatro copos com 200 mL de água, dois deles mantidos a 25 °C, e dois deles, a 5 °C. Num dos copos com água a 25 °C foi adicionado um comprimido efervescente inteiro, enquanto, no outro, se adicionou meio comprimido. Nos copos mantidos a 5 °C, o mesmo foi feito.
Quanto à evolução inicial de gás nos copos, como a reação não tem cinética de ordem zero, observa-se
Quanto à evolução inicial de gás nos copos, como a reação não tem cinética de ordem zero, observa-se
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias Inorgânicas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Um laboratório analisou a água da caixa d’água de uma certa residência que havia sido deixada aberta pelo seu proprietário, recebendo assim a chuva de uma região poluída. Foi recolhida uma amostra de 25 mL, a qual foi neutralizada totalmente por 10 mL de solução 5 x 10-4 mol/L de hidróxido de sódio.
Supondo que essa contaminação da água seja por um monoácido, a concentração desse monoácido, em mol/L, encontrada na água dessa caixa é igual a
Supondo que essa contaminação da água seja por um monoácido, a concentração desse monoácido, em mol/L, encontrada na água dessa caixa é igual a
Provas
Questão presente nas seguintes provas
Considere as estruturas dos hidrocarbonetos representados a seguir.

Sobre esses hidrocarbonetos, tem-se que
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- FundamentosSubstâncias, Misturas e Processos de Separação
- FundamentosTransformações: Estados Físicos e Fenômenos
- Química CinéticaTransformações Químicas
- Química InorgânicaSoluções e Substâncias Inorgânicas
Dentre os fenômenos abaixo, aquele que evidencia ocorrência de reação química com transferência de elétrons de uma espécie a outra é a
Provas
Questão presente nas seguintes provas
O volume que 12,9 g de um gás ocupa é 9,8 L, a 25 °C e 1 atm. 7
Considerando-se que o gás tem comportamento ideal, esse gás é o
Dado
RT = 24,4 atm L-1 mol -1
Considerando-se que o gás tem comportamento ideal, esse gás é o
Dado
RT = 24,4 atm L-1 mol -1
Provas
Questão presente nas seguintes provas
- Química OrgânicaPolímeros
- Química OrgânicaReações OrgânicasReações Orgânicas: Oxidação, Redução e Polimerização
A reação entre hexametilenodiamina (C6 H16 N2 ) e um ácido orgânico, cuja fórmula molecular é C6 H10 O4 , sob condições ideais, dá origem a um polímero do tipo poliamida. Nessa reação ocorre também a eliminação de moléculas de água. Essa poliamida é classificada como um polímero
Provas
Questão presente nas seguintes provas
- Química CinéticaTransformações Químicas
- Química InorgânicaSoluções e Substâncias Inorgânicas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Em um recipiente fechado promove-se o contato do sal bicarbonato de sódio sólido com um vinagre comercial contendo 4,0% de ácido acético. Desse contato ocorre uma transformação química representada pela equação
NaHCO3(s) + HC2 H3 O2(aq) → NaC2 H3O2(aq) + H2 O(l) + CO2(g)
Nessa reação, o
NaHCO3(s) + HC2 H3 O2(aq) → NaC2 H3O2(aq) + H2 O(l) + CO2(g)
Nessa reação, o
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Soluções tampões são soluções que resistem a mudanças no pH, seja pela adição de um ácido ou de uma base. A fim de preparar uma solução tampão, um técnico utilizou solução aquosa de ácido acético a 0,1 mol/L que está 1% ionizada para posterior dissolução do sal de seu ânion.
A concentração dos íons acetato e o pH da solução ácida serão, respectivamente,
A concentração dos íons acetato e o pH da solução ácida serão, respectivamente,
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container