Foram encontradas 429 questões.
223527
Ano: 2018
Disciplina: Administração de Recursos Materiais
Banca: CESGRANRIO
Orgão: Liquigás
Disciplina: Administração de Recursos Materiais
Banca: CESGRANRIO
Orgão: Liquigás
Provas:
A manutenção de estoques implica riscos de investimento
e de possibilidade de obsolescência em diversos pontos
da cadeia de suprimentos.
Esses riscos são maiores para o
Esses riscos são maiores para o
Provas
Questão presente nas seguintes provas
Em uma transformação química que envolve dois reagentes
produzindo um único produto, observa-se que o(a)
Provas
Questão presente nas seguintes provas
Uma mistura gasosa, encerrada em um recipiente de aço,
contém CO2
e N2
. Essa mistura, considerando-se condições ideais, exerce pressão total de 10 atm, sendo a pressão
parcial do N2
quatro vezes maior do que a do CO2
.
Na mistura, a pressão parcial, em atm, do CO2 é
Na mistura, a pressão parcial, em atm, do CO2 é
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
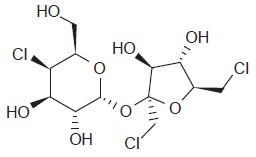
A sucralose é um edulcorante amplamente consumido.
Provas
Questão presente nas seguintes provas
A liberação de calor proveniente da combustão da glicose
(C6
H12O6
) é de 2.600 kJ de energia por cada 1 mol. Um
atleta olímpico precisa de 10.140 kJ por dia, quando em
treinamento prévio a uma grande competição.
Ao expressar essa energia em termos de massa de glicose, o atleta deve ingerir, em gramas, aproximadamente,
Dado M(C) = 12 g mol-1 M (O) = 16 g mol-1 M(H) = 1 g mol-1
Ao expressar essa energia em termos de massa de glicose, o atleta deve ingerir, em gramas, aproximadamente,
Dado M(C) = 12 g mol-1 M (O) = 16 g mol-1 M(H) = 1 g mol-1
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasPropriedades Coligativas: Tonoscopia, Ebulioscopia, Crioscopia e Pressão Osmótica.
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma solução para remoção de esmalte foi preparada,
misturando-se 176,0 g de acetato de etila e 29,0 g de acetona.
Considerando-se a temperatura de 20 ºC, a razão entre a pressão de vapor da acetona pura e a pressão de vapor do removedor de esmalte é, aproximadamente,
Dado Pressão de vapor do acetato de etila: 73 mmHg a 20 ºC Pressão de vapor da acetona: 200 mmHg a 20 ºC M (acetato de etila) = 88,0 g mol-1 M (acetona) = 58,0 g mol-1
Considerando-se a temperatura de 20 ºC, a razão entre a pressão de vapor da acetona pura e a pressão de vapor do removedor de esmalte é, aproximadamente,
Dado Pressão de vapor do acetato de etila: 73 mmHg a 20 ºC Pressão de vapor da acetona: 200 mmHg a 20 ºC M (acetato de etila) = 88,0 g mol-1 M (acetona) = 58,0 g mol-1
Provas
Questão presente nas seguintes provas
A reação de oxirredução que ocorre numa pilha de lítio é representada simplificadamente a seguir:
2 Li(s) + I2(s) → 2 Li+ (aq) + 2 I- (aq)
Dados os potenciais padrões de redução:
• Eº Li+ /Li = -3,05 V
• Eº I2 /I- = +0,53 V
verifica-se que a diferença de potencial padrão dessa pilha, em volts, é
Provas
Questão presente nas seguintes provas
Considere a reação termoquímica abaixo:
C3 H8 (g) + 5 O2 (g) → 3 CO2 (g) + 4 H2 O (g); ∆Hº = -490 kJ mol-1
A queima de uma quantidade de propano produziu 98.000 kJ de calor.
Conclui-se que a massa, em gramas, de propano que reagiu foi
Dado M (C3 H8 ) = 44 g mol-1
C3 H8 (g) + 5 O2 (g) → 3 CO2 (g) + 4 H2 O (g); ∆Hº = -490 kJ mol-1
A queima de uma quantidade de propano produziu 98.000 kJ de calor.
Conclui-se que a massa, em gramas, de propano que reagiu foi
Dado M (C3 H8 ) = 44 g mol-1
Provas
Questão presente nas seguintes provas
Uma solução líquida contém duas substâncias denominadas
I e II. Um volume de 100 microlitros da solução foi
colocado perto da borda inferior (na linha da amostragem)
de uma placa de cromatografia de camada delgada, cuja
fase estácionária tem caráter mais polar. A borda inferior
da placa foi mergulhada em solvente de caráter menos
polar, de forma que este, por capilaridade, percolasse a
fase estacionária. Após 5 minutos, a linha de frente foi
marcada 10,0 cm acima da linha de amostragem.
Sabendo-se que o fator de retenção (RF) da substância I foi de 0,9, que o da substância II foi de 0,6 e que os diâmetros das manchas foram de 0,2 cm, conclui-se que a
Sabendo-se que o fator de retenção (RF) da substância I foi de 0,9, que o da substância II foi de 0,6 e que os diâmetros das manchas foram de 0,2 cm, conclui-se que a
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
- Transformações Químicas e EnergiaEletroquímica
A medição de pH de uma solução aquosa é feita usando-se o eletrodo combinado de membrana de vidro.
Nessa medição, há eletrodo de
Nessa medição, há eletrodo de
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container