Foram encontradas 50 questões.
O hidrogênio é preparado em grande escala por diversos métodos. Qual dos processos abaixo irá produzir hidrogênio muito puro (99,9%)?
Provas
O rótulo de um produto de limpeza informa que a concentração de amônia (NH3) é de 9,5 g/litro. Com o intuito de verificar se a concentração de amônia corresponde à indicada no rótulo, uma amostra de 5,00 ml desse produto foi titulada com ácido clorídrico de concentração 0,100 mol / 2. Para consumir toda a amônia dessa amostra, foram gastos 25,00 ml de ácido.
Com base nas informações fornecidas, qual a concentração da solução, em mol/1, calculado com os dados da titulação?
Provas
Dadas as fórmulas H2, LiF, CO,, CaCl2, em quais substâncias abaixo as ligações entre os átomos são exemplos de ligações químicas covalentes?
Provas
Em um meio ácido e redutor, a reação catódica que ocorre sobre uma superfície de ferro é
Provas
Observe abaixo os calores das seguintes reações a 298 &K e 1 atm.
\( C_2H_{2(g)} + 5/2 O_{2(g)} \rightarrow 2\,\,CO_{2(g)} + H_2O_{(l)} + 310Kcal \)
\( C_2H_{6(g)} + 7/2 O_{2(g)} \rightarrow 2\,\,CO_{2(g)} +3 H_2O_{(l)} + 372Kcal \)
\( H_{2(g)} + 1/2 O_{2(g)} \rightarrow \,\,H_2O_{(l)} + 68 Kcal \)
De acordo com os dados apresentados acima, calcule o calor da reação abaixo a 298 K e 1 atm em valores absolutos, e assinale a opção correta.
\( C_2 H_{2(g)} + 2H_2 \rightarrow C_2H_{6(g)} \)
Provas
A Lei dos Gases Ideais é expressa pela seguinte relação:
PV = nRI, onde P = pressão do gás
V = volume do gás
n = quantidade do gás em mol
R = constante universal dos gases perfeitos
T = temperatura do gás.
se for fixada uma quantidade de gás, a seguinte consideração sobre esta lei é correta:
constante a expressão se transforma na Lei de
Provas
O Brasil possui grande reserva de nióbio. Com relação a este elemento químico, é correto afirmar que os números quânticos principal, azimutal e magnético do elétron mais energético É, respectivamente:
Provas
Observe a pilha a seguir.
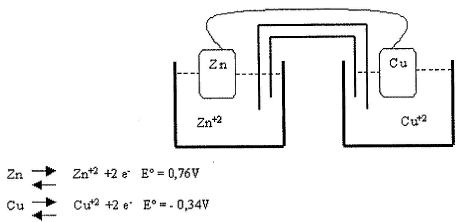
De acordo com a figura acima, pode-se afirmar que
Provas
Em um laboratório existem 3 soluções com rótulos ilegíveis. Sabendo-se que cada um deles possui apenas um único ânion, foram efetuadas as seguintes experiências:
Solução A + solução de Iodo \( \rightarrow \) descora formando solução incolor
Solução A + cloreto de ferroIII \( \rightarrow \) coloração violeta-escuro
Solução B + HCl diluído \( \rightarrow \) mancha escura em papel de filtro embebido com acetato de chumbo colocado na boca do tubo de ensaio
Solução B + AgNO3\( \rightarrow \) precipitado preto
Solução.C + HCl diluído \( \rightarrow \) apresenta efervescência
Solução C + AgNO3 \( \rightarrow \) precipitado branco
Solução C + Call2 \( \rightarrow \) precipitado branco
Assim, pode-se concluir que os ânions presentes nas soluções A, Be C possuem, respectivamente:
Provas
Sabe-se que um certo elemento químico do grupo 2 possui 56 prótons e 81 nêutrons no seu núcleo. Ao efetuar ligação iônica, ele
Provas
Caderno Container