Foram encontradas 50 questões.
Analise as figuras a seguir.
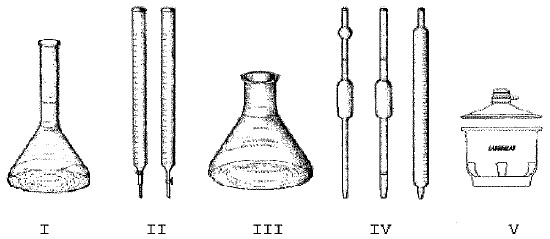
Analisando os materiais de laboratório apresentados nas figuras acima, assinale a opção INCORRETA.
Provas
Analise as afirmativas abaixo, em relação às reações de complexação, e assinale a opção correta.
I- Um íon complexo é composto de um átomo central e de vários ligantes intimamente acoplados a ele.
II - Um fenômeno que ocorre na formação do íon complexo é uma mudança de cor na solução.
III- Quanto menor for o valor da constante de instabilidade (ou de dissociação) menos estável será o complexo.
Provas
A solubilidade molar do iodato de chumbo(II), Pb (IO3 )2 , em , 25ºC, é 4,0x10-5 mol-1 . Qual o valor do produto de solubilidade (Kps) do iodato de chumbo(II)?
Provas
Assinale a opção que apresenta o elemento químico que possui o valor de eletronegatividade mais alto na Tabela Periódica.
Provas
A trinitração do tolueno, considerando as regras comuns de substituição aromática, dá origem, preferencialmente, ao seguinte composto:
Provas
Analise a tabela a seguir.
| Indicador | Faixa de viragem (pH) | Cor em meio ácido | Cor em meio básico |
| I - Fenolftaleína | 8,3-10,0 | incolor | vermelho |
| II -Amarelo de alizarina | 10, 1-12, 1 | amarelo | vermelho alaranjado |
| III- Vermelho de metila | 4,2-6,3 | vermelho | amarelo |
| IV -Timolftaleína | 9,3-10,5 | incolor | azul |
| V -Alaranjado de metila | 2,9-4,6 | vermelho | larania |
Na titulação de um ácido forte com uma base fraca podem ser usados indicadores que possibilitam a determinação do ponto de equivalência. Dentre os indicadores listados na tabela acima, assinale a opção que apresenta aqueles que podem ser utilizados neste tipo de titulação.
Provas
Quando se realiza uma análise instrumental, uma tentativa de se melhorar a exatidão da medida realizada é feita com a utilização de um branco. O branco ideal é formado pelos constituintes da amostra em análise, exceto o de interesse. Porém, devido às dificuldades de sua obtenção, utiliza-se um branco real - formado pelo solvente utilizado na preparação da amostra ou um branco reagente - com o solvente e os reagentes usados na preparação da amostra, dessa forma, procura-se corrigir os chamados erros
Provas
Além da natureza do problema analítico a ser solucionada, outros critérios devem ser observados na seleção de métodos analíticos adequados a cada caso. Assinale a opção que apresenta critérios a serem considerados em todos os métodos de análise.
Provas
Com relação à dureza da água, é INCORRETO afirmar que a
Provas
No composto H2SO4 , conhecido como ácido sulfúrico, há· ligações covalentes e iônicas. Conhecendo-se a definição de cada um desses tipos de ligação, qual é o número de oxidação do átomo de enxôfre neste composto?
Provas
Caderno Container