Foram encontradas 80 questões.
Um elemento químico pertencente ao segundo
período da Tabela Periódica forma compostos estáveis com, no máximo, quatro ligações covalentes,
enquanto seu análogo do terceiro período forma
espécies como PX₅.
A explicação mais adequada para esse comportamento distinto é:
A explicação mais adequada para esse comportamento distinto é:
Provas
Questão presente nas seguintes provas
Considere a afirmação a seguir, frequentemente
encontrada em interpretações equivocadas de fenômenos químicos:
“Uma reação química não ocorre espontaneamente porque é exotérmica.”
À luz das leis empíricas da Termodinâmica, essa afirmação é:
“Uma reação química não ocorre espontaneamente porque é exotérmica.”
À luz das leis empíricas da Termodinâmica, essa afirmação é:
Provas
Questão presente nas seguintes provas
Em um experimento de cinética química, a velocidade inicial de uma reação genérica A + B → produtos
foi medida para diferentes concentrações iniciais dos
reagentes, conforme a tabela:
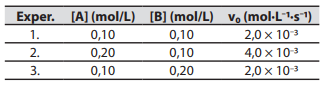
Com base nos dados, a lei de velocidade da reação é:

Com base nos dados, a lei de velocidade da reação é:
Provas
Questão presente nas seguintes provas
Em um laboratório forense, uma reação reversível
é utilizada para identificação de uma substância. O
sistema atinge o equilíbrio químico à temperatura
constante.
Nessa condição:
Nessa condição:
Provas
Questão presente nas seguintes provas
Durante a análise de um artefato incendiário, o
perito avalia a viabilidade energética de uma reação
química envolvida no processo de combustão.
Assinale a alternativa correta considerando os conceitos da termodinâmica química.
Assinale a alternativa correta considerando os conceitos da termodinâmica química.
Provas
Questão presente nas seguintes provas
Durante a análise pericial de um recipiente contendo um gás ideal em Condições Normais de Temperatura e Pressão (CNTP), um perito verifica que a amostra
possui massa igual a 11,0 g e ocupa um volume de 5,6 L.
Considerando essas informações, assinale a alternativa que indica, respectivamente, a quantidade de matéria do gás e sua massa molar.
Considerando essas informações, assinale a alternativa que indica, respectivamente, a quantidade de matéria do gás e sua massa molar.
Provas
Questão presente nas seguintes provas
Em uma investigação pericial, duas reações químicas distintas apresentam valores igualmente negativos de energia livre de Gibbs (ΔG < 0), indicando
que ambas são termodinamicamente espontâneas.
No entanto, observa-se experimentalmente que uma
ocorre rapidamente, enquanto a outra se processa de
forma extremamente lenta à temperatura ambiente.
Essa diferença no comportamento reacional é explicada, principalmente, pela:
Essa diferença no comportamento reacional é explicada, principalmente, pela:
Provas
Questão presente nas seguintes provas
Uma solução aquosa utilizada em um procedimento pericial contém 1 mol de cloreto de sódio completamente dissociado em meio aquoso e 9 mol de
água como solvente.
Considerando a dissociação total do eletrólito e desprezando efeitos de atividade, a fração molar da água nessa solução é de, aproximadamente:
Considerando a dissociação total do eletrólito e desprezando efeitos de atividade, a fração molar da água nessa solução é de, aproximadamente:
Provas
Questão presente nas seguintes provas
Considere o equilíbrio gasoso abaixo, frequentemente discutido em análises envolvendo sistemas
reacionais confinados:
N₂O₄(g) ⇄ 2NO₂(g)
Quando a pressão total do sistema é aumentada, mantendo-se a temperatura constante, o equilíbrio químico será deslocado:
N₂O₄(g) ⇄ 2NO₂(g)
Quando a pressão total do sistema é aumentada, mantendo-se a temperatura constante, o equilíbrio químico será deslocado:
Provas
Questão presente nas seguintes provas
Em análises químicas forenses, a oxidação do íon
oxalato por permanganato de potássio em meio ácido
é frequentemente empregada como método indireto
para a quantificação de matéria orgânica em diferentes matrizes ambientais e biológicas.
A reação global ocorre com redução do manganês de +7 para +2 e oxidação do oxalato a dióxido de carbono, conforme a equação não balanceada:
MnO₄−+C₂O₄2− → Mn₂+ + CO₂
Após o balanceamento correto da equação química em meio ácido, considerando conservação de massa e de carga elétrica, o coeficiente estequiométrico do íon permanganato é:
A reação global ocorre com redução do manganês de +7 para +2 e oxidação do oxalato a dióxido de carbono, conforme a equação não balanceada:
MnO₄−+C₂O₄2− → Mn₂+ + CO₂
Após o balanceamento correto da equação química em meio ácido, considerando conservação de massa e de carga elétrica, o coeficiente estequiométrico do íon permanganato é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container