Foram encontradas 395 questões.
Um gás ideal, ao receber calor de uma fonte térmica, executa um processo, no qual seu volume permanece constante. A pressão final do gás nesse processo é 4 vezes maior do que a pressão inicial. Qual a relação entre a temperatura final e a temperatura inicial do gás nesse processo?
Provas
Questão presente nas seguintes provas
O ponto de orvalho é a temperatura de uma mistura vaporizada a uma dada pressão, na qual ocorre a
Provas
Questão presente nas seguintes provas
- EletromagnetismoElétricaCircuitos Elétricos Especiais: Leis de Kirchhoff e Ponte de Wheatstone
- EletromagnetismoElétricaEletricidade
A forma como um voltímetro deve ser conectado ao circuito no qual se deseja medir a tensão e sua impedância são, respectivamente:
Provas
Questão presente nas seguintes provas
Todo o ar do interior de um recipiente cúbico é retirado, formando vácuo. A aresta do cubo mede 50 cm. Qual a força de compressão, em newtons, que cada face do cubo sofre, devido à pressão atmosférica exterior? Dado: Considere que a pressão atmosférica vale 1,0 x 105
N/m2
Provas
Questão presente nas seguintes provas
Um gás é submetido a um processo térmico no qual recebe, de uma fonte térmica, 40.000 cal de calor, enquanto realiza trabalho no valor de 2,0 x 10 5 j .Qual a variação, em joules, da energia interna do gás nesse processo?
Dado: 1 cal = 4 J
Dado: 1 cal = 4 J
Provas
Questão presente nas seguintes provas

Dado: g = 10 m/s²
Provas
Questão presente nas seguintes provas
Uma indústria possui um conjunto de máquinas-ferramenta que consomem 20 galões de lubrificante/mês. Cada galão é adquirido por R$ 35,00. Os custos mensais de pedido e os custos unitários de manutenção do estoque são, respectivamente, 10% e 20% do valor da compra. O lubrificante é comprado a cada 2 semanas. Os valores, para o estoque médio, para os custos de manutenção do estoque, para os custos de pedido e os custos totais da estocagem, são, respectivamente,
Provas
Questão presente nas seguintes provas
O pH de um sistema tampão, constituído de um ácido fraco e sua base conjugada forte, como o ácido carbônico e o bicarbonato, representado pelo equilíbrio abaixo, se altera muito pouco, quer se introduza um ácido forte ou uma base forte, quer se dilua o sistema. 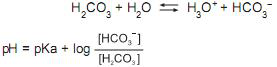
Sobre o equilíbrio de um sistema contendo 100 mL de solução 0,1 mol/L de H 2CO3 e 0,1 mol/L de HCO3– , quando se adiciona(m)
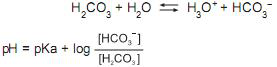
Sobre o equilíbrio de um sistema contendo 100 mL de solução 0,1 mol/L de H 2CO3 e 0,1 mol/L de HCO3– , quando se adiciona(m)
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Tabela de solubilidades, a 25°C, em gramas por 100 mL

O sal diet é uma mistura de cloreto de potássio e cloreto de sódio, contendo quantidade traço de cloreto de lítio. Uma amostra de 4,5 g seca de sal diet foi pesada e analisada para determinar-se a percentagem em massa de cloreto de potássio. Para tal, a mistura de cloretos alcalinos foi tratada com ácido perclórico de modo a converter os sais cloretos em sais percloratos. A amostra foi seca e, em seguida, foi adicionada em 100 mL de acetato de etila, nos quais o potássio se precipitou na forma de KClO4 (ver dados de solubilidade na tabela acima). O sobrenadante foi separado, e o precipitado lavado com acetato de etila, antes de ser seco e pesado na balança analítica. Qual a percentagem, em massa, de KCl na amostra se a massa de KClO4 obtida foi igual a 2,77 g?

O sal diet é uma mistura de cloreto de potássio e cloreto de sódio, contendo quantidade traço de cloreto de lítio. Uma amostra de 4,5 g seca de sal diet foi pesada e analisada para determinar-se a percentagem em massa de cloreto de potássio. Para tal, a mistura de cloretos alcalinos foi tratada com ácido perclórico de modo a converter os sais cloretos em sais percloratos. A amostra foi seca e, em seguida, foi adicionada em 100 mL de acetato de etila, nos quais o potássio se precipitou na forma de KClO4 (ver dados de solubilidade na tabela acima). O sobrenadante foi separado, e o precipitado lavado com acetato de etila, antes de ser seco e pesado na balança analítica. Qual a percentagem, em massa, de KCl na amostra se a massa de KClO4 obtida foi igual a 2,77 g?
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Heterogêneos: Produto de Solubilidade (Kps)
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
O sulfato de cobre (II) pentahidratado, CuSO4
.
5H2
O (massa molar = 249,5 g/mol), é utilizado em piscinas como algicida. Em solução aquosa, a espécie Cu2+ pode precipitar-se na forma de hidróxido de cobre, Cu(OH)2, cujo equilíbrio de solubilidade é mostrado abaixo.
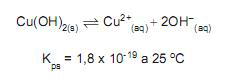
Sendo o valor do pH ideal da água da piscina igual a 6, a quantidade máxima de CuSO4 . 5H2 O em massa, que deve ser adicionada a uma piscina de volume igual a 10.000 L, com água no pH ideal, em kg, é
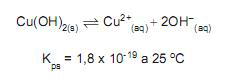
Sendo o valor do pH ideal da água da piscina igual a 6, a quantidade máxima de CuSO4 . 5H2 O em massa, que deve ser adicionada a uma piscina de volume igual a 10.000 L, com água no pH ideal, em kg, é
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container