Foram encontradas 60 questões.
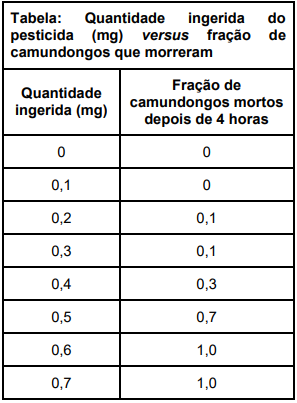
Em um estudo de toxicidade, camundongos
foram expostos a um pesticida que pretende-se
lançar ao mercado, e obteve-se a seguinte tabela
onde mostra-se a quantidade ingerida (mg)
versus fração de camundongos que morreram.
A LD50 aproximada é:

A LD50 aproximada é:
Provas
Questão presente nas seguintes provas
Pela definição da EPA (Environmental Protect
Agency, dos EUA), uma substância perigosa é:
"Uma substância que em razão da sua
quantidade, concentração, características
físicas, químicas ou infecciosas, pode causar
ou contribuir consideravelmente para um
aumento na mortalidade (...)".
No quadro A, são encontradas algumas classificações de resíduos, no quadro B são encontradas algumas substâncias químicas consideradas perigosas.
Quadro A 1. Resíduo inflamável 2. Resíduo corrosivo 3. Resíduo Tóxico 4. Resíduo de origens específicas
Quadro B I. H2SO4 II. Hg III. Lodo de tratamento de água residual de produção de coque IV. C2H5OH
Faça uma associação entre os quadros A e B e assinale a alternativa correta.
No quadro A, são encontradas algumas classificações de resíduos, no quadro B são encontradas algumas substâncias químicas consideradas perigosas.
Quadro A 1. Resíduo inflamável 2. Resíduo corrosivo 3. Resíduo Tóxico 4. Resíduo de origens específicas
Quadro B I. H2SO4 II. Hg III. Lodo de tratamento de água residual de produção de coque IV. C2H5OH
Faça uma associação entre os quadros A e B e assinale a alternativa correta.
Provas
Questão presente nas seguintes provas
Em microbiologia Clínica são utilizados
diferentes meios de cultura que entre suas
classificações podem ser: seletivos ou
diferenciais; sintético ou complexos; sólidos,
semissólidos ou líquidos. Dentre essas
características temos:
I. Meios de culturas sintéticos são aqueles que a composição química é qualitativa e quantitativamente conhecida. II. Os meios seletivos servem para suprimir algum microrganismo indesejado ou favorecer algum de interesse. III. Os meios diferenciais são aqueles que conferem características especiais às colônias. Em situações normais, elas seriam idênticas.
Assinale alternativa correta.
I. Meios de culturas sintéticos são aqueles que a composição química é qualitativa e quantitativamente conhecida. II. Os meios seletivos servem para suprimir algum microrganismo indesejado ou favorecer algum de interesse. III. Os meios diferenciais são aqueles que conferem características especiais às colônias. Em situações normais, elas seriam idênticas.
Assinale alternativa correta.
Provas
Questão presente nas seguintes provas
Um químico preparou uma solução de Ba+2 comconcentração 0,025M. Inicia-se então umatitulação com 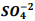 seguindo a reação: BαSO4(s) ⇔
seguindo a reação: BαSO4(s) ⇔ 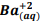 +
+ 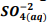 , onde Kps = [ Bα+2] [
, onde Kps = [ Bα+2] [ 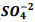 ] = 1, 1 x10−10. Verifica-se que:
] = 1, 1 x10−10. Verifica-se que:
I. A partir da concentração de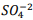 acima de0,025M inicia a precipitação de Ba+2. II. Em concentrações menores que 4,4 x10−9 M jáhouve precipitação de BαSO4.
acima de0,025M inicia a precipitação de Ba+2. II. Em concentrações menores que 4,4 x10−9 M jáhouve precipitação de BαSO4.
Assinale a alternativa correta:
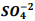 seguindo a reação: BαSO4(s) ⇔
seguindo a reação: BαSO4(s) ⇔ 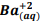 +
+ 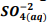 , onde Kps = [ Bα+2] [
, onde Kps = [ Bα+2] [ 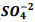 ] = 1, 1 x10−10. Verifica-se que:
] = 1, 1 x10−10. Verifica-se que: I. A partir da concentração de
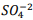 acima de0,025M inicia a precipitação de Ba+2. II. Em concentrações menores que 4,4 x10−9 M jáhouve precipitação de BαSO4.
acima de0,025M inicia a precipitação de Ba+2. II. Em concentrações menores que 4,4 x10−9 M jáhouve precipitação de BαSO4. Assinale a alternativa correta:
Provas
Questão presente nas seguintes provas
Considere a titulação de 100,0 ml do ácido
acético 0,100M com hidróxido de sódio 0,100M:
CH3CO2H(aq) + OH-(aq) ⇔ CH3CO2-(aq) + H2O(l)
Para atingir o ponto de equivalência foram gastos 5,3 x10-6 M de OH- e o pH ficou em 8,72.
Analise as afirmativas a seguir e dê valores Verdadeiro (V) ou Falso (F).
( ) No ponto de equivalência o pH é neutro. ( ) No ponto de equivalência, o pH é ligeiramente básico, porém a partir desse ponto, a adição de mais NaOH torna a solução substancialmente básica.
Assinale a alternativa que apresenta a sequência correta de cima para baixo.
CH3CO2H(aq) + OH-(aq) ⇔ CH3CO2-(aq) + H2O(l)
Para atingir o ponto de equivalência foram gastos 5,3 x10-6 M de OH- e o pH ficou em 8,72.
Analise as afirmativas a seguir e dê valores Verdadeiro (V) ou Falso (F).
( ) No ponto de equivalência o pH é neutro. ( ) No ponto de equivalência, o pH é ligeiramente básico, porém a partir desse ponto, a adição de mais NaOH torna a solução substancialmente básica.
Assinale a alternativa que apresenta a sequência correta de cima para baixo.
Provas
Questão presente nas seguintes provas
O pH de uma solução-tampão de ácido acético
e acetato de sódio é representada por CH3COOH
+ H2O ⇔ CH3COO- + H3O+
. A concentração inicial
de CH3COOH = 0,700M e CH3COO- = 0,600M e a
constante de equilíbrio é 1,8.10-5.
A equação que melhor representa a constante de equilíbrio para esse tampão é:
A equação que melhor representa a constante de equilíbrio para esse tampão é:
Provas
Questão presente nas seguintes provas
Soluções-tampão possuem uma função
importante em sistemas reacionais e
biológicos, mantendo o pH de uma solução em
uma faixa específica para o trabalho. Algumas
informações sobre soluções-tampão são
mostradas nas seguintes afirmativas:
I. Duas substâncias devem ser utilizadas, um ácido capaz de reagir com os íons OH- adicionados e uma base capaz de reagir com os íons H3O+ adicionados. II. Soluções-tampão podem ser preparadas a partir de um par ácido forte e seu sal conjugado. III. A dupla conjugada do sistema tampão do ácido acético é: CH3COOH ⇔ CH3COO-.
Estão corretas as afirmativas:
I. Duas substâncias devem ser utilizadas, um ácido capaz de reagir com os íons OH- adicionados e uma base capaz de reagir com os íons H3O+ adicionados. II. Soluções-tampão podem ser preparadas a partir de um par ácido forte e seu sal conjugado. III. A dupla conjugada do sistema tampão do ácido acético é: CH3COOH ⇔ CH3COO-.
Estão corretas as afirmativas:
Provas
Questão presente nas seguintes provas
Cromatografia é uma técnica muito utilizada em
laboratórios de pesquisas e analíticos com a
intenção de analisar e quantificar substâncias
orgânicas. Os analitos percorrem uma coluna
preenchida com uma fase estacionária (que pode
ser eletricamente neutra ou carregada e saem no
outro orifício em tempos determinados. O que faz
esse analito ficar mais ou menos tempo dentro das
colunas é o quanto esse composto é adsorvido
pelo material de preenchimento da coluna, ou seja,
quanto menor o tempo, menor a interação com a
coluna.
Um par de aminoácido é separado em uma coluna onde a fase estacionária está saturada com água e o solvente transportados é o metanol. Os aminoácidos são:
HOOC-CHNH2-CH2-OH e HOOC-CHNH2-CH3.
Assinale a alternativa que melhor representa o que acontece.
Um par de aminoácido é separado em uma coluna onde a fase estacionária está saturada com água e o solvente transportados é o metanol. Os aminoácidos são:
HOOC-CHNH2-CH2-OH e HOOC-CHNH2-CH3.
Assinale a alternativa que melhor representa o que acontece.
Provas
Questão presente nas seguintes provas
Na reação heterogênea entre o superóxido de
potássio e o gás carbônico, há a liberação de
oxigênio, segundo a reação:
X KO2(s) + Y CO2(g) ⇔ W K2CO3(s) + Z O2(g).
Calcule a massa de KO2 necessária para reagir com 50 l de CO2 a 25°C e 1,0 atm. A massa molar do KO2 é 71,1 g/mol. Considere o volume molar 24,5l/mol.
Assinale a alternativa que contém os valores de X, Y, W e Z e a massa de KO2 consumida na reação.
X KO2(s) + Y CO2(g) ⇔ W K2CO3(s) + Z O2(g).
Calcule a massa de KO2 necessária para reagir com 50 l de CO2 a 25°C e 1,0 atm. A massa molar do KO2 é 71,1 g/mol. Considere o volume molar 24,5l/mol.
Assinale a alternativa que contém os valores de X, Y, W e Z e a massa de KO2 consumida na reação.
Provas
Questão presente nas seguintes provas
Calcule o volume de gás carbônico para que plantas
produzam 1,00 g de glicose à 25°C e 1,0 atm.
Reação: 6CO2(g) + 6H2O(l) ⇔ C6H12O6(g) + 6O2(g).
Considere massa molecular da glicose = 180 g/mol e volume molar = 24,5 l/mol.
Assinale a alternativa que contém a resposta correta.
Reação: 6CO2(g) + 6H2O(l) ⇔ C6H12O6(g) + 6O2(g).
Considere massa molecular da glicose = 180 g/mol e volume molar = 24,5 l/mol.
Assinale a alternativa que contém a resposta correta.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container