Foram encontradas 570 questões.
Dada a equação química
Fe + H2SO4 → Fe2(SO4)3 + H2
a soma de todos os menores coeficientes estequiométricos da equação balanceada pelo método das tentativas é igual a
Provas
Questão presente nas seguintes provas
O gráfico a seguir mostra a estimativa da mudança de
temperatura diante de três diferentes cenários: um considerando
uma faixa intermediária de emissões (SSP2-4,5), um segundo com
o fim de todas as emissões e um terceiro com o fim das emissões
apenas de CO2. Ao considerar o primeiro cenário (SSP2-4.5), a
possibilidade de um aumento de 1,5ºC na temperatura global é
estimada em 42% atualmente, podendo chegar a 66% em 2029.
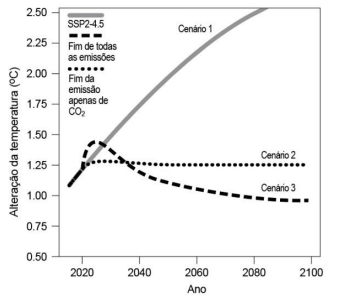
(Adaptado de https://www.nature.com/articles/s41558-022-01372-y)
O problema ambiental, aqui considerado como antropogênico, que seria mitigado com a redução do gás indicado no gráfico seria o

(Adaptado de https://www.nature.com/articles/s41558-022-01372-y)
O problema ambiental, aqui considerado como antropogênico, que seria mitigado com a redução do gás indicado no gráfico seria o
Provas
Questão presente nas seguintes provas
Observe a seguir uma ilustração comumente usada nas aulas de
ciências para representar a organização das partículas de uma
substância nos diferentes estados físicos.
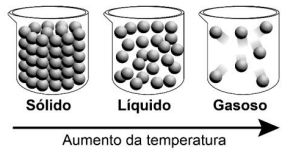
Em relação a este tema, é correto afirmar que

Em relação a este tema, é correto afirmar que
Provas
Questão presente nas seguintes provas
Para o estudo da fotossíntese, uma professora realizou com a
turma o seguinte experimento:
1. Em dois tubos de ensaio, os alunos adicionaram 20mL de água contendo algumas gotas de solução de NaOH. Em seguida, adicionaram 5 gotas de azul de bromotimol em cada tubo. 2. Com um canudo, misturaram a água e o azul de bromotimol. A água dos tubos ficou azul. 3. Usando o canudo, um aluno soprou cuidadosamente em cada tubo, até que a água ficasse amarela. 4. Colocaram um pequeno ramo de elódea em cada tubo e tamparam os tubos com uma rolha. 5. Envolveram totalmente um dos tubos com cartolina preta e colocaram os dois tubos em frente a uma fonte de luz.
A figura a seguir ilustra as etapas do experimento descrito acima.

Transcorridas algumas horas após o início do experimento, deve-se esperar que a água do tubo mantido
1. Em dois tubos de ensaio, os alunos adicionaram 20mL de água contendo algumas gotas de solução de NaOH. Em seguida, adicionaram 5 gotas de azul de bromotimol em cada tubo. 2. Com um canudo, misturaram a água e o azul de bromotimol. A água dos tubos ficou azul. 3. Usando o canudo, um aluno soprou cuidadosamente em cada tubo, até que a água ficasse amarela. 4. Colocaram um pequeno ramo de elódea em cada tubo e tamparam os tubos com uma rolha. 5. Envolveram totalmente um dos tubos com cartolina preta e colocaram os dois tubos em frente a uma fonte de luz.
A figura a seguir ilustra as etapas do experimento descrito acima.

Transcorridas algumas horas após o início do experimento, deve-se esperar que a água do tubo mantido
Provas
Questão presente nas seguintes provas
Uma das dificuldades para a reciclagem das embalagens plásticas
é que, em geral, elas são descartadas misturadas. Como as
embalagens podem ser compostas de diferentes tipos de
plástico, é preciso separá-los de acordo com sua constituição
para que possam ser reciclados adequadamente, sem que as
propriedades físicas e mecânicas sejam alteradas. Assim, em
certas indústrias de reciclagem, depois que as embalagens
plásticas são moídas, seus fragmentos passam por uma banheira
com água para que ocorra a separação dos diferentes tipos de
plástico que os compõem. No caso de garrafas de refrigerante,
fragmentos de politereftalato de etileno (PET) que compõe o
corpo da garrafa afundam, enquanto fragmentos de polietileno
de alta densidade (PEAD), que compõe a tampa, flutuam.
Com relação à técnica de separação descrita e as propriedades dos plásticos, assinale V para a afirmativa verdadeira e F para a falsa.
( ) A separação do politereftalato de etileno (PET) e do polietileno de alta densidade (PEAD) é possível porque são plásticos que possuem densidades, respectivamente, maior e menor que 1,0 g/cm3. ( ) Se na mistura formada pelas partículas de embalagens moídas existir um plástico com densidade maior que a densidade do PET, será possível separá-lo adicionando uma quantidade determinada de sal à agua da banheira. ( ) Considere dois blocos maciços, um composto de plástico PET e o outro, de PEAD. Se os blocos possuem a mesma massa, o bloco composto de PET terá maior volume.
As afirmativas são, respectivamente,
Com relação à técnica de separação descrita e as propriedades dos plásticos, assinale V para a afirmativa verdadeira e F para a falsa.
( ) A separação do politereftalato de etileno (PET) e do polietileno de alta densidade (PEAD) é possível porque são plásticos que possuem densidades, respectivamente, maior e menor que 1,0 g/cm3. ( ) Se na mistura formada pelas partículas de embalagens moídas existir um plástico com densidade maior que a densidade do PET, será possível separá-lo adicionando uma quantidade determinada de sal à agua da banheira. ( ) Considere dois blocos maciços, um composto de plástico PET e o outro, de PEAD. Se os blocos possuem a mesma massa, o bloco composto de PET terá maior volume.
As afirmativas são, respectivamente,
Provas
Questão presente nas seguintes provas
O ensino de Química na educação básica pode ser feito por meio
da construção, do exercício e da discussão de três níveis de
conhecimento: o fenomenológico, o teórico e o representacional.
Compete ao nível representacional
Compete ao nível representacional
Provas
Questão presente nas seguintes provas
“Transfira 3 gotas da solução de nitrato de chumbo para o tubo
de ensaio e adicione 3 gotas da solução de iodeto de potássio.
Observe o que acontece na mistura das soluções.”.
A aula experimental em laboratório de química configura uma atividade cujo objetivo é exercitar a observação e evidenciar a transformação química, seja pela mudança de coloração, formação de precipitados ou liberação de gases.
O trecho foi extraído de uma apostila de aulas experimentais de química. Nesse experimento, o aluno deverá perceber a formação de um precipitado amarelo.
Com o desenvolvimento dessa atividade, o aluno poderá perceber e concluir sobre a possível ocorrência de uma reação
A aula experimental em laboratório de química configura uma atividade cujo objetivo é exercitar a observação e evidenciar a transformação química, seja pela mudança de coloração, formação de precipitados ou liberação de gases.
O trecho foi extraído de uma apostila de aulas experimentais de química. Nesse experimento, o aluno deverá perceber a formação de um precipitado amarelo.
Com o desenvolvimento dessa atividade, o aluno poderá perceber e concluir sobre a possível ocorrência de uma reação
Provas
Questão presente nas seguintes provas
“Um dos maiores defensores da inclusão de história das ciências e
epistemologia no ensino de ciências é Michael Mattews, que
advoga a importância tanto do ensino sobre as ciências quanto
do ensino de ciências. Na sua perspectiva, ensinar sobre ciências
inclui, além dos resultados científicos, a discussão de toda uma
dinâmica da atividade científica: descoberta, justificação,
divulgação e aceitação do conhecimento científico.”
O texto defende a inclusão de história de ciências no currículo em ação.
As opções a seguir apresentam vantagens para o uso da história das ciências, à exceção de uma. Assinale-a.
O texto defende a inclusão de história de ciências no currículo em ação.
As opções a seguir apresentam vantagens para o uso da história das ciências, à exceção de uma. Assinale-a.
Provas
Questão presente nas seguintes provas
“A outra escola de pensamento defendia o método do peso
equivalente. Este media o peso de um elemento segundo a
quantidade relativa que reagia quimicamente com uma única
quantidade de hidrogênio, ou um equivalente calculável.”
STRATHERN, Paul. O Sonho de Mendeleiev - A verdadeira história da Química. 2002. Zahar.
Na tentativa de estabelecer um peso para o oxigênio, descobriu-se que seu peso equivalente era 8, muito embora o oxigênio tivesse peso atômico 16, já que um volume de gás oxigênio pesava 16 vezes mais do que o mesmo volume de hidrogênio.
O peso equivalente do oxigênio era a metade do seu peso atômico porque
STRATHERN, Paul. O Sonho de Mendeleiev - A verdadeira história da Química. 2002. Zahar.
Na tentativa de estabelecer um peso para o oxigênio, descobriu-se que seu peso equivalente era 8, muito embora o oxigênio tivesse peso atômico 16, já que um volume de gás oxigênio pesava 16 vezes mais do que o mesmo volume de hidrogênio.
O peso equivalente do oxigênio era a metade do seu peso atômico porque
Provas
Questão presente nas seguintes provas
“Aceitando a ideia de Boyle de que gases consistem de partículas
minúsculas, [Dalton] logo descobriu uma propriedade
fundamental dos gases, até hoje conhecida como Lei de Dalton.”
STRATHERN, Paul. O Sonho de Mendeleiev - A verdadeira história da Química. 2002. Zahar.
Assinale a opção que apresenta corretamente a Lei de Dalton.
STRATHERN, Paul. O Sonho de Mendeleiev - A verdadeira história da Química. 2002. Zahar.
Assinale a opção que apresenta corretamente a Lei de Dalton.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container