Foram encontradas 60 questões.
A Cipermetrina é uma substância do grupo dos piretróides e possui classificação toxicológica nível II (altamente tóxica). É fotoestável, não se degradando com a luz solar. Atua como um potente inseticida, por contato ou ingestão, contra alvos biológicos que causam consideráveis danos a culturas como algodão, café, milho e soja.
A fórmula que representa a estrutura química da cipermetrina é mostrada a seguir.
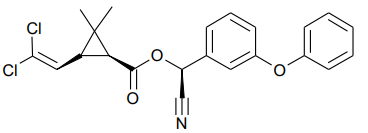
Nessa estrutura, é possível identificar os grupos funcionais
Provas
Questão presente nas seguintes provas
A energia de ionização (EI) é uma propriedade periódica quemostra tendência inversa ao raio atômico, diminuindo da direitapara a esquerda ao longo do período.
Entretanto, observa-se que, contrário à regra, os valores daprimeira energia de ionização dos átomos nitrogênio (Z = 7) eoxigênio (Z = 8) mostram EI(O) < EI(N):
• EI(N) = 1402 kJ mol-1 • EI(O) = 1314 kJ mol-1
Assinale a opção que justifica corretamente a relação entre osvalores de EI do nitrogênio e do oxigênio.
Entretanto, observa-se que, contrário à regra, os valores daprimeira energia de ionização dos átomos nitrogênio (Z = 7) eoxigênio (Z = 8) mostram EI(O) < EI(N):
• EI(N) = 1402 kJ mol-1 • EI(O) = 1314 kJ mol-1
Assinale a opção que justifica corretamente a relação entre osvalores de EI do nitrogênio e do oxigênio.
Provas
Questão presente nas seguintes provas
Bohr desenvolveu seu modelo atômico adotando duas premissas:
1. A quantização do momento angular. 2. O equilíbrio mecânico atingido pela igualdade dos módulos das forças elétrica (de atração do elétron ao núcleo) e centrípeta (do movimento circular do elétron em torno do núcleo).
Dessa forma, ele desenvolveu uma expressão para a energia que depende de um número quântico, n, que indica o nível de energia eletrônica e determina o raio.
A esse respeito, assinale V para a afirmativa verdadeira e F para a falsa.
( ) O modelo atômico de Bohr permitiu descrever com sucesso o raio do movimento circular do elétron em torno do núcleo de hidrogênio no estado fundamental. ( ) O modelo atômico de Bohr permitiu descrever com sucesso a diferença de energia entre dois níveis eletrônicos do átomo de hidrogênio. ( ) O modelo atômico de Bohr permitiu descrever com sucesso o comprimento de onda associado a excitações eletrônicas em átomos de qualquer número atômico.
As afirmativas são, respectivamente,
1. A quantização do momento angular. 2. O equilíbrio mecânico atingido pela igualdade dos módulos das forças elétrica (de atração do elétron ao núcleo) e centrípeta (do movimento circular do elétron em torno do núcleo).
Dessa forma, ele desenvolveu uma expressão para a energia que depende de um número quântico, n, que indica o nível de energia eletrônica e determina o raio.
A esse respeito, assinale V para a afirmativa verdadeira e F para a falsa.
( ) O modelo atômico de Bohr permitiu descrever com sucesso o raio do movimento circular do elétron em torno do núcleo de hidrogênio no estado fundamental. ( ) O modelo atômico de Bohr permitiu descrever com sucesso a diferença de energia entre dois níveis eletrônicos do átomo de hidrogênio. ( ) O modelo atômico de Bohr permitiu descrever com sucesso o comprimento de onda associado a excitações eletrônicas em átomos de qualquer número atômico.
As afirmativas são, respectivamente,
Provas
Questão presente nas seguintes provas
Ácido crotônico é um composto insaturado de cadeia normal.
Ele é sólido, de ponto de fusão 71,6ºC, e, em soluções aquosas,
comporta-se como um ácido fraco, com Ka = 2x010–5.
A fórmula química que representa sua estrutura é apresentada abaixo:
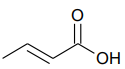
Uma solução aquosa de ácido crotônico foi preparada pela dissolução de 2,15g do ácido em água, sendo o volume final igual a 500mL.
[Dados: massas molares (em g.mol-1). C: 12; H: 1; O: 16.]
O pH dessa solução é igual a
A fórmula química que representa sua estrutura é apresentada abaixo:

Uma solução aquosa de ácido crotônico foi preparada pela dissolução de 2,15g do ácido em água, sendo o volume final igual a 500mL.
[Dados: massas molares (em g.mol-1). C: 12; H: 1; O: 16.]
O pH dessa solução é igual a
Provas
Questão presente nas seguintes provas
Os compostos hidroxiacetona (1-hidroxi-propan-2-ona), etanoato
de metila e ácido propanoico foram recentemente identificados
no espaço interestelar. Eles estão inseridos numa classe
denominada “compostos orgânicos complexos” e suas rotas de
síntese nesse meio despertam grande interesse científico.
Dedica-se grande esforço também à compreensão do papel
exercido por tais compostos orgânicos complexos na síntese
abiótica de biomoléculas também encontradas nas mesmas
regiões.
A esse respeito, assinale V para a afirmativa verdadeira e F para a falsa.
( ) Hidroxiacetona, etanoato de metila e ácido propanoico são isômeros. ( ) Hidroxiacetona, etanoato de metila e ácido propanoico apresentam grupos polares em suas estruturas. ( ) Pontos de ebulição dos compostos seguem a ordem: etanoato de metila > ácido propanoico ≈ hidroxiacetona.
As afirmativas são, respectivamente,
A esse respeito, assinale V para a afirmativa verdadeira e F para a falsa.
( ) Hidroxiacetona, etanoato de metila e ácido propanoico são isômeros. ( ) Hidroxiacetona, etanoato de metila e ácido propanoico apresentam grupos polares em suas estruturas. ( ) Pontos de ebulição dos compostos seguem a ordem: etanoato de metila > ácido propanoico ≈ hidroxiacetona.
As afirmativas são, respectivamente,
Provas
Questão presente nas seguintes provas
Diborano (B2H6) é um gás incolor com odor repulsivamente doce.Mistura-se facilmente com o ar formando uma mistura explosiva,pois sofre ignição espontaneamente em ar úmido à temperaturaambiente.
Considere os dados termoquímicos:
B2H6(g) + 3 O2(g) → B2O3(s) + 3 H2O(g) ΔHº= -1941 kJ mol–1 2 B(s) + 3/2 O2(g) → B2O3(s) ΔHº= -2368 kJ mol–1 H2(g) + 1/2 O2(g) → H2O(g) ΔHº= -241,8 kJ mol–1
A entalpia padrão de formação do diborano (em kJ mol–1) é
Considere os dados termoquímicos:
B2H6(g) + 3 O2(g) → B2O3(s) + 3 H2O(g) ΔHº= -1941 kJ mol–1 2 B(s) + 3/2 O2(g) → B2O3(s) ΔHº= -2368 kJ mol–1 H2(g) + 1/2 O2(g) → H2O(g) ΔHº= -241,8 kJ mol–1
A entalpia padrão de formação do diborano (em kJ mol–1) é
Provas
Questão presente nas seguintes provas
Deseja-se construir um sistema eletroquímico contendo um
catodo de cobre (no qual o metal estará imerso em uma solução
aquosa de nitrato de cobre) e um anodo de alumínio (no qual o
metal estará imerso em solução aquosa de sulfato de alumínio).
Os dois eletrodos estarão conectados por uma ponte salina,
contendo solução aquosa de nitrato de potássio e, externamente,
por um fio de cobre condutor.
[Dados. Potenciais de redução padrão:
E0Al3+|Al = -1,66 V; E0Cu2+|Cu = +0,34 V.]
Nessas condições, analise as afirmativas a seguir a respeito desse sistema eletroquímico:
I. Será uma pilha, pois a reação esperada é espontânea. II. A diferença de potencial esperada é 7,32V. III. Será uma reação espontânea se um potencial externo de 2,00V for aplicado ao sistema.
Está correto o que se afirma em
[Dados. Potenciais de redução padrão:
E0Al3+|Al = -1,66 V; E0Cu2+|Cu = +0,34 V.]
Nessas condições, analise as afirmativas a seguir a respeito desse sistema eletroquímico:
I. Será uma pilha, pois a reação esperada é espontânea. II. A diferença de potencial esperada é 7,32V. III. Será uma reação espontânea se um potencial externo de 2,00V for aplicado ao sistema.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
Dois recipientes contêm metano e amônia, respectivamente,
ambos com volume de 10L, e estão sob mesma temperatura
(425K) e pressão (0,85 bar).
[Dados: massas molares (em g.mol-1). Metano: 16; Amônia: 17.]
Nesse caso, é correto afirmar que os recipientes contêm
[Dados: massas molares (em g.mol-1). Metano: 16; Amônia: 17.]
Nesse caso, é correto afirmar que os recipientes contêm
Provas
Questão presente nas seguintes provas
A análise elementar tem por objetivo identificar e quantificar
elementos químicos como carbono, hidrogênio, nitrogênio e
enxofre com excelente precisão em compostos presentes em
amostras puras líquidas ou sólidas. Os resultados da análise
elementar permitem identificar a fórmula mínima do composto
químico.
A análise elementar de uma amostra revelou a seguinte composição: 58,5% de carbono, 4,1% de hidrogênio e 11,4 % de nitrogênio.
[Dados: massas molares (em g.mol-1): C: 12; H: 1; N: 14; O: 16.]
A fórmula mínima do composto na amostra é
A análise elementar de uma amostra revelou a seguinte composição: 58,5% de carbono, 4,1% de hidrogênio e 11,4 % de nitrogênio.
[Dados: massas molares (em g.mol-1): C: 12; H: 1; N: 14; O: 16.]
A fórmula mínima do composto na amostra é
Provas
Questão presente nas seguintes provas
O professor deve promover práticas pedagógicas diferenciadas,
reflexivas, colaborativas e dialógicas que, necessariamente,
utilizem TIC, para que as crianças e os jovens vivenciem situações
de possíveis usos das TIC, sempre com base em seus hábitos,
crenças e atitudes, de maneira que se apropriem delas nas mais
variadas situações de vida na sociedade.
De acordo com a afirmativa, assinale a opção que indica o objeto de conhecimento ligado ao terceiro eixo do currículo de Tecnologia para Aprendizagem.
De acordo com a afirmativa, assinale a opção que indica o objeto de conhecimento ligado ao terceiro eixo do currículo de Tecnologia para Aprendizagem.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container