Foram encontradas 140 questões.
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
- Sistemas de EquilíbrioSistemas Homogêneos: Constantes: Kc e Kp. Deslocamento do Equilíbrio: Fatores
A amônia é um gás incolor à temperatura ambiente e possui um odor
extremamente forte. Seu caráter polar é a principal razão para a sua solubilidade em
água, sendo que em ambientes aquáticos, o nitrogênio amoniacal compreende as
formas do íon amônio (NH4+) e da amônia (NH3) dissolvidos, de maneira que a
proporção entre elas depende da temperatura, salinidade e, principalmente, do pH
do meio.
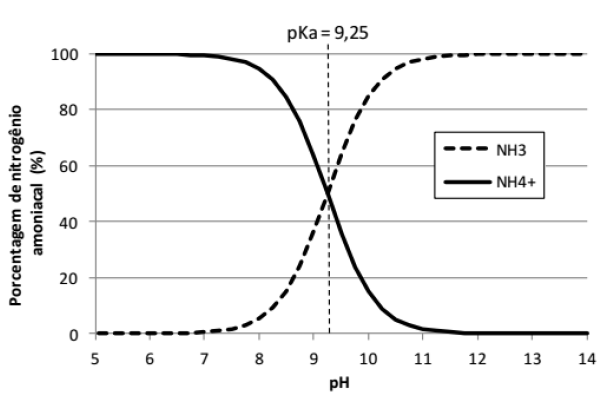
De acordo com o gráfico acima e os conhecimentos sobre equilíbrio químico. Assinale a alternativa CORRETA:

De acordo com o gráfico acima e os conhecimentos sobre equilíbrio químico. Assinale a alternativa CORRETA:
Provas
Questão presente nas seguintes provas
As técnicas eletroanalíticas se baseiam em processos de ________onde as espécies
eletroativas do meio oferecem resposta à aplicação de um _______para o monitoramento
da corrente elétrica ou valor do potencial em comparação ao potencial de um eletrodo de
referência. A ________e a _______são bastante utilizadas em análises de espécies
eletroativas orgânicas e inorgânicas e na determinação seletiva de íons orgânicos e
inorgânicos em solução, respectivamente. Assinale a alternativa que corresponde as
palavras CORRETAS para cada respectivo espaço vazio.
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Considere a reação a seguir:
NaOH + H2SO4 → Na2SO4 + H2O
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaVelocidade de Reação, Energia de Ativação e Catalisadores
O Sulfato de amônio é um composto inorgânico utilizado na agricultura como
fertilizante. Este sal é obtido pela reação entre a amônia e o ácido sulfúrico, de
acordo com a reação abaixo.
NH3 + H2SO4 → (NH4)2SO4
Se a obtenção deste sal for obtida através da lavagem do gás amônia com uma solução de ácido sulfúrico, dado que a concentração de amônia é de 34.000 mg/L, qual seria a concentração de ácido sulfúrico em mol/L necessária para se obter 100% de rendimento? (Dados: massas molares: H= 1,0 g/mol, N= 14 g/mol, O= 16 g/mol, S= 32 g/mol)
NH3 + H2SO4 → (NH4)2SO4
Se a obtenção deste sal for obtida através da lavagem do gás amônia com uma solução de ácido sulfúrico, dado que a concentração de amônia é de 34.000 mg/L, qual seria a concentração de ácido sulfúrico em mol/L necessária para se obter 100% de rendimento? (Dados: massas molares: H= 1,0 g/mol, N= 14 g/mol, O= 16 g/mol, S= 32 g/mol)
Provas
Questão presente nas seguintes provas
Sabendo que o hidróxido de alumínio é o composto gelatinoso que aglutina
impurezas presentes na água, ao tentar diminuir seu efeito, reage-se 1 mol do
composto com 1 mol de ácido sulfúrico. Assinale a alternativa que corresponde
CORRETAMENTE ao produto salino originado.
Provas
Questão presente nas seguintes provas
Grande parte dos estudos em Química são destinados a química da separação.
Diversas técnicas foram desenvolvidas ao longo dos anos com o objetivo de
concentrar analitos, separar interferentes, isolar compostos de interesse
econômico e até mesmo tratar água e efluentes. Com base em seus conhecimentos
em técnicas de separação, assinale a alternativa INCORRETA:
Provas
Questão presente nas seguintes provas
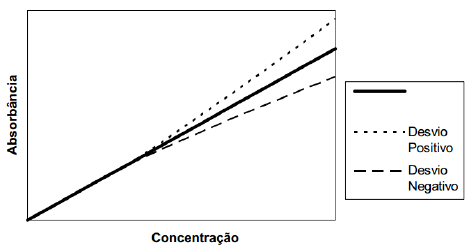
Os desvios por limitação da Lei de Lambert-Beer são aqueles que as interações
do analito com o solvente e demais solutos variam com o aumento da
concentração. Observe o gráfico abaixo e assinale quais afirmativas são
VERDADEIRAS.
 I. Em soluções concentradas do analito ou outros solutos, as interações soluto-soluto
alteram a estrutura do analito e também modificam a sua absortividade.
II. Ao ocorrer um desvio na Lei de Lambert-Beer ainda pode-se trabalhar com a curva de
calibração, embora ela não seja uma reta.
III. Como os desvios normalmente ocorrem em concentrações muito baixas, uma das
soluções mais comuns é a pré-concentração.
IV. Os desvios são positivos e negativos conforme as alterações aumentem ou diminuam
a absorvidade.
V. Os desvios podem ser químicos ou causados pela instrumentação, entretanto, neste
último, o desvio é praticamente nulo, devido a equipamentos de alta tecnologia.
I. Em soluções concentradas do analito ou outros solutos, as interações soluto-soluto
alteram a estrutura do analito e também modificam a sua absortividade.
II. Ao ocorrer um desvio na Lei de Lambert-Beer ainda pode-se trabalhar com a curva de
calibração, embora ela não seja uma reta.
III. Como os desvios normalmente ocorrem em concentrações muito baixas, uma das
soluções mais comuns é a pré-concentração.
IV. Os desvios são positivos e negativos conforme as alterações aumentem ou diminuam
a absorvidade.
V. Os desvios podem ser químicos ou causados pela instrumentação, entretanto, neste
último, o desvio é praticamente nulo, devido a equipamentos de alta tecnologia.
 I. Em soluções concentradas do analito ou outros solutos, as interações soluto-soluto
alteram a estrutura do analito e também modificam a sua absortividade.
II. Ao ocorrer um desvio na Lei de Lambert-Beer ainda pode-se trabalhar com a curva de
calibração, embora ela não seja uma reta.
III. Como os desvios normalmente ocorrem em concentrações muito baixas, uma das
soluções mais comuns é a pré-concentração.
IV. Os desvios são positivos e negativos conforme as alterações aumentem ou diminuam
a absorvidade.
V. Os desvios podem ser químicos ou causados pela instrumentação, entretanto, neste
último, o desvio é praticamente nulo, devido a equipamentos de alta tecnologia.
I. Em soluções concentradas do analito ou outros solutos, as interações soluto-soluto
alteram a estrutura do analito e também modificam a sua absortividade.
II. Ao ocorrer um desvio na Lei de Lambert-Beer ainda pode-se trabalhar com a curva de
calibração, embora ela não seja uma reta.
III. Como os desvios normalmente ocorrem em concentrações muito baixas, uma das
soluções mais comuns é a pré-concentração.
IV. Os desvios são positivos e negativos conforme as alterações aumentem ou diminuam
a absorvidade.
V. Os desvios podem ser químicos ou causados pela instrumentação, entretanto, neste
último, o desvio é praticamente nulo, devido a equipamentos de alta tecnologia. Provas
Questão presente nas seguintes provas
O controle de qualidade da água é realizado durante e após a etapa de tratamento
e tem como objetivo avaliar a eficácia do tratamento e verificar se os parâmetros de
potabilidade estão na faixa estabelecida pela legislação. Todas as alternativas
sobre estes parâmetros estão corretas, EXCETO:
Provas
Questão presente nas seguintes provas
A técnica de precipitação é amplamente utilizada na química analítica. Os
métodos gravimétricos são quantitativos e se baseiam em medidas de massa.
Sobre a gravimetria, todas as alternativas estão corretas, EXCETO:
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Soluções de soda cáustica são constantemente utilizadas para ajuste de pH e
para neutralizar soluções ácidas. Uma solução de hidróxido de sódio (NaOH) foi
preparada dissolvendo-se 200 g de NaOH em 1000 g de água. Determine qual é a
concentração em mol/L desta solução. (Dados: densidade da água = 1,0 g/cm3
;
massas molares: H= 1,0 g/mol, Na= 23 g/mol, O= 16 g/mol; 1 cm3 = 0,001 dm3
).
Assinale a alternativa CORRETA.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container