Foram encontradas 120 questões.
2865901
Ano: 2022
Disciplina: Legislação Estadual e Distrital
Banca: CESPE / CEBRASPE
Orgão: SEDUC-AL
Disciplina: Legislação Estadual e Distrital
Banca: CESPE / CEBRASPE
Orgão: SEDUC-AL
Provas:
Com relação ao Plano de Cargo e Carreira do Magistério Público
Estadual e ao Código de Ética Funcional do Servidor Público
Civil do Estado de Alagoas, julgue o item subsequente.
Provas
Questão presente nas seguintes provas
2865900
Ano: 2022
Disciplina: Legislação Estadual e Distrital
Banca: CESPE / CEBRASPE
Orgão: SEDUC-AL
Disciplina: Legislação Estadual e Distrital
Banca: CESPE / CEBRASPE
Orgão: SEDUC-AL
Provas:
Com relação ao Plano de Cargo e Carreira do Magistério Público
Estadual e ao Código de Ética Funcional do Servidor Público
Civil do Estado de Alagoas, julgue o item subsequente.
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
Uma transformação química milenar é a produção do etanol a
partir da fermentação de alimentos. Nesse processo, a levedura e
outros microrganismos fermentam a glicose (C6H12O6) em etanol
(C2H5OH) e CO2. Com relação à história da química e ao mundo
e suas transformações, julgue o item subsequente,
considerando 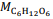 = 180 g/mol e
= 180 g/mol e 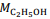 = 46 g/mol.
= 46 g/mol.
A química distanciou-se da alquimia a partir dos ensaios de Robert Boyle, um dos primeiros pesquisadores a dar forma científica ao atomismo, opondo-se a Aristóteles e Paracelso.
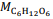 = 180 g/mol e
= 180 g/mol e 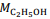 = 46 g/mol.
= 46 g/mol. A química distanciou-se da alquimia a partir dos ensaios de Robert Boyle, um dos primeiros pesquisadores a dar forma científica ao atomismo, opondo-se a Aristóteles e Paracelso.
Provas
Questão presente nas seguintes provas
Com relação a ligações químicas, geometria molecular e teoria da
ligação de valência, julgue o item que se segue.
Nos compostos formados por cátions e ânions muito polarizáveis, o caráter da ligação química é fortemente covalente.
Nos compostos formados por cátions e ânions muito polarizáveis, o caráter da ligação química é fortemente covalente.
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias Inorgânicas
- Técnicas de LaboratórioEquipamentos e Técnicas Básicas
Considere os seguintes exemplos de exercício e problema.
1. Exercício – Calcule a concentração, em mol/L, de íon cloro
em uma solução formada a partir da dissolução de 2,0 g de NaCl
em 1 L de água.
2. Problema – Qual é a concentração de íons cloro na água de
torneira?
A próxima tabela ressalta aspectos que caracterizam um exercício
e um problema.

Recomenda-se o uso da técnica de neutralização em uma aula experimental cujo objetivo seja padronizar a concentração de soluções diluídas ácidas ou básicas.
Provas
Questão presente nas seguintes provas
2167326
Ano: 2022
Disciplina: Legislação Estadual e Distrital
Banca: CESPE / CEBRASPE
Orgão: SEDUC-AL
Disciplina: Legislação Estadual e Distrital
Banca: CESPE / CEBRASPE
Orgão: SEDUC-AL
Provas:
Considerando as disposições do Regime Jurídico Único dos
Servidores Públicos Civis do Estado de Alagoas, das Autarquias
e das Fundações Públicas Estaduais e as disposições do Estatuto
do Magistério Público do Estado de Alagoas, julgue o item que
se segue.
Provas
Questão presente nas seguintes provas
Uma transformação química milenar é a produção do etanol a
partir da fermentação de alimentos. Nesse processo, a levedura e
outros microrganismos fermentam a glicose (C6H12O6) em etanol
(C2H5OH) e CO2. Com relação à história da química e ao mundo
e suas transformações, julgue o item subsequente,
considerando 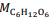 = 180 g/mol e
= 180 g/mol e 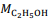 = 46 g/mol.
= 46 g/mol.
De acordo com os experimentos de Faraday, a quantidade de produto formado ou de reagente consumido em uma reação eletrolítica é estequiometricamente proporcional à diferença de potencial aplicada entre os eletrodos da célula eletrolítica.
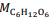 = 180 g/mol e
= 180 g/mol e 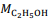 = 46 g/mol.
= 46 g/mol. De acordo com os experimentos de Faraday, a quantidade de produto formado ou de reagente consumido em uma reação eletrolítica é estequiometricamente proporcional à diferença de potencial aplicada entre os eletrodos da célula eletrolítica.
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química OrgânicaGlicídios, Lipídios, Aminoácidos e Proteínas.
Uma transformação química milenar é a produção do etanol a
partir da fermentação de alimentos. Nesse processo, a levedura e
outros microrganismos fermentam a glicose (C6H12O6) em etanol
(C2H5OH) e CO2. Com relação à história da química e ao mundo
e suas transformações, julgue o item subsequente,
considerando 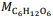 = 180 g/mol e
= 180 g/mol e 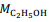 = 46 g/mol.
= 46 g/mol.
De acordo com a reação descrita, para a obtenção de 1,0 kg de etanol, são necessários mais de 2,0 kg de glicose.
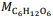 = 180 g/mol e
= 180 g/mol e 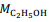 = 46 g/mol.
= 46 g/mol. De acordo com a reação descrita, para a obtenção de 1,0 kg de etanol, são necessários mais de 2,0 kg de glicose.
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
Com relação a ligações químicas, eletronegatividade, repulsão de
pares eletrônicos e geometria molecular, julgue o item a seguir.
O ângulo de ligação entre átomos de hidrogênio é maior em uma molécula de amônia que em uma molécula de água.
O ângulo de ligação entre átomos de hidrogênio é maior em uma molécula de amônia que em uma molécula de água.
Provas
Questão presente nas seguintes provas
Com relação a ligações químicas, geometria molecular e teoria da
ligação de valência, julgue o item que se segue.
De acordo com a teoria de ligação de valência, a molécula de água é constituída por quatro orbitais híbridos do tipo sp3 arranjados de forma tetraédrica em torno do oxigênio, de maneira que dois orbitais participam das ligações simples O–H e outros dois acomodam os pares de elétrons não ligantes.
De acordo com a teoria de ligação de valência, a molécula de água é constituída por quatro orbitais híbridos do tipo sp3 arranjados de forma tetraédrica em torno do oxigênio, de maneira que dois orbitais participam das ligações simples O–H e outros dois acomodam os pares de elétrons não ligantes.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container