Foram encontradas 50 questões.
Quando uma reação química ocorre entre dois átomos, os seus elétrons de valência são rearranjados de tal forma que uma força resultante atrativa, a ligação química, passa a existir entre esses átomos. São características de ligação iônica e covalente, respectivamente:
Provas
Sinta-se um químico responsável por um laboratório de Química que deseja preparar 500 mL de uma solução de hidróxido de sódio, NaOH, de concentração 3 mol/L. Qual a quantidade de massa de NaOH que deverá ser pesada e seguidamente dissolvida em água suficiente para completar 500 mL dessa solução?
(Dados: H = 1,00g/mol; Na = 23,00g/mol; O = 16,00g/mol)
Provas
O conceito de concentração é útil em muitos contextos. Por exemplo, o Rio de Janeiro tem cerca de 12 milhões e 800 mil habitantes e área superficial de 46.600 km2, aproximadamente; logo, a concentração média de habitantes é de cerca de 275 habitantes por quilômetro quadrado. Em química, a quantidade de soluto dissolvido num determinado volume de solução pode ser calculada da mesma forma e se denomina concentração da solução. Com base nessas informações, qual a concentração molar da solução preparada de NaCl, quando se usa 116g dessa substância dissolvida em 1000 mL de solução?
(Dados: Na = 23,00g/mol; Cl = 35,00g/mol)
Provas
Os termos “oxidação” e “redução” vêm de reações que foram conhecidas por séculos. Civilizações antigas aprenderam como transformar óxidos e sulfetos metálicos em metais, isto é, como reduzir os minérios em metais. Um exemplo de reações de oxidação-redução, é o óxido de ferro (III) reagindo com o monóxido de carbono, como mostrado na equação abaixo:
Fe2O3 (s) + 3 CO (g) → 2 Fe (s) + 3 CO2 (g)
Nesta reação, podemos afirmar CORRETAMENTE que:
Provas
Ácidos e bases são duas classes muito importantes de compostos e têm várias propriedades em comum. Por exemplo, soluções de ácidos ou bases podem mudar as cores de pigmentos vegetais de modos específicos. Uma base pode neutralizar o efeito de um ácido, e um ácido pode neutralizar o efeito de uma base. Segundo Arrhenius, são propriedades dos ácidos e bases, respectivamente:
Provas
O ferro reage com o oxigênio formando o óxido de ferro, Fe2O3, como mostrado na equação química abaixo:
Fe (s) + O2 (g) → Fe2O3 (s)
Os coeficientes mínimos e inteiros da equação química acima, quando balanceada, deverão ser, respectivamente:
Provas
Os elementos são dispostos na tabela periódica de modo que elementos com propriedades físicas e químicas semelhantes ficam em colunas verticais, chamadas grupos. A tabela que se usa comumente tem os grupos numerados de 1 a 8, com cada número seguido pela letra A ou B. Com este sistema, os químicos frequentemente designam os elementos dos grupos A como os elementos representativos e os dos grupos B como os elementos de transição. As fileiras horizontais da tabela são os períodos, que são numerados a partir de 1, para o período que contém somente H e He. Por exemplo, o sódio, Na, está no grupo 1A e é o primeiro elemento do terceiro período. O mercúrio, Hg, está no grupo 2B e no sexto período. De acordo com os procedimentos utilizados para localização dos elementos químicos na Tabela Periódica, podemos afirmar corretamente que o elemento químico Telúrio, 52Te128, se encontra no grupo e período, respectivamente:
Provas
Segundo as experiências de Thomson, Rutherford e outros cientistas conduziram ao modelo atual do átomo. Neste modelo, todos os átomos são constituídos de três partículas fundamentais: prótons, nêutrons e elétrons. Com base nesses conhecimentos, nos deparamos com as seguintes afirmativas:
I. Os prótons e os nêutrons se localizam num núcleo muito pequeno, significando que o núcleo concentra toda a carga positiva e quase toda a massa do átomo.
II. Os elétrons, com carga negativa, envolvem o núcleo e ocupam a menor parte do volume de um átomo.
III. Como o átomo não tem carga elétrica líquida, o número de elétrons fora do núcleo é igual ao número de prótons no interior do núcleo.
IV. Existem nêutrons no núcleo de todos os átomos (normalmente num número no mínimo igual ao número de prótons), exceto para o átomo de hidrogênio, que tem somente um único próton em seu núcleo.
Acerca das afirmativas acima são CORRETAS, apenas:
Provas
Em 1803, John Dalton (1766-1844) reviveu intensamente a ideia dos átomos. Dalton correlacionou a ideia da existência de elementos que não podem ser decompostos quimicamente, à ideia dos átomos, que são indivisíveis. Os compostos, que podem ser divididos em duas ou mais substâncias novas, têm que conter duas ou mais espécies diferentes de átomos. Dalton foi além, afirmando que cada espécie de átomo tem suas propriedades específicas, especialmente uma massa característica. Essa ideia permitiu que a sua teoria explicasse quantitativamente as massas dos diferentes elementos que se combinavam quimicamente para formar compostos. Dentre os postulados de Dalton, podemos destacar CORRETAMENTE que:
Provas
Observe o hidrocarboneto mostrado abaixo:
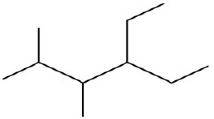
Segundo a IUPAC, União Internacional de Química Pura e Aplicada, a nomenclatura oficial para o composto acima é:
Provas
Caderno Container