Foram encontradas 50 questões.
Os compostos de coordenação, K4[Fe(CN)6] e [Ni(NH3)6]Br2 recebem, respectivamente, os seguintes nomes CORRETAMENTE:
(Dados: K+; Fe2+; CN-; Ni2+; NH3; Br-)
Provas
Com relação aos estudos dos complexos, a nomenclatura oficial para o composto de coordenação, [Fe(CN)2(NH3)2(H2O)2]+, será:
(Dados: Fe3+; CN-; NH3; H2O)
Provas
Os compostos I e II, mostrados abaixo, são isômeros de:
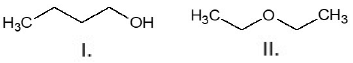
Provas
Aminas são substâncias orgânicas que apresentam um ou mais radicais ligados ao Nitrogênio e são muito utilizadas na produção de outros compostos orgânicos. Aminas são compostos orgânicos nitrogenados que derivam da substância amônia (NH3) pela substituição de um ou mais hidrogênios por radicais orgânicos. São exemplos de compostos orgânicos nitrogenados:
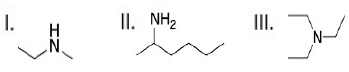
Sobre os compostos orgânicos nitrogenados acima, pode-se afirmar CORRETAMENTE que:
Provas
Os compostos, mostrados abaixo, pertencem a classe dos álcoois:
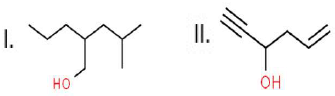
As nomenclaturas para os compostos I e II, respectivamente, segundo a IUPAC, são:
Provas
O produto obtido pela oxidação de um álcool depende da estrutura do álcool. A oxidação de um álcool primário ocorre em duas etapas. Ele é inicialmente oxidado a um composto X, e então, numa segunda etapa, a um composto Y, como mostrado na equação abaixo:

Os produtos X e Y obtidos pela oxidação do álcool acima, respectivamente, são
Provas
Geralmente, os compostos carbonilados são classificados em subcategorias. Esta classificação é feita com base nos grupos ligados ao carbono da carbonila. São exemplos de compostos carbonilados.
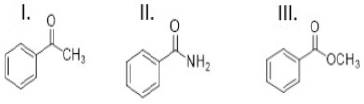
Os compostos I, II e III acima apresentam, respectivamente, os grupos funcionais:
Provas
Para descrever as ligações no metano e em outras moléculas, Linus Pauling propôs a teoria da hibridização dos orbitais. Ele propôs que orbitais atômicos s, p e/ou d de um determinado átomo pudessem se misturar para criar um novo conjunto de orbitais, denominado orbitais híbridos. No caso do metano, CH4, cada ligação C-H é formada então pela superposição de um orbital híbrido do carbono com um orbital 1s do hidrogênio. Cada um dos orbitais híbridos do carbono é denominado:
(Dados: 1H1; 6C12)
Provas
Baseado nos conhecimentos adquiridos sobre repulsão de pares de elétrons na camada de valência, RPECV, podemos garantir que o NH3, possui geometria de pares de elétrons e geometria molecular, respectivamente:
(Dados: 1H1; 7N14)
Provas
O modelo de repulsão de pares de elétrons na camada de valência (sigla RPECV, sigla inglesa VSEPR), imaginado por Ronald J. Gillespie (1924-) e Ronald S. Nyholm (1917-1971), é um método confiável de se preverem as formas de moléculas covalentes e de íons poliatômicos. De acordo com esses autores, podemos afirmar CORRETAMENTE que os compostos PF5 e SF4 possuem, respectivamente, geometria molecular:
(Dados: 9F19; 16S32)
Provas
Caderno Container