Foram encontradas 80 questões.
Mesmo que um modelo atômico consiga explicar muitos fenômenos ele não explica tudo o que acontece, e pode ser substituído. Em se tratando de modelos atômicos analise as proposições abaixo:
I. O modelo de Dalton foi um resgate da primitiva teoria atômica de Epicuro que viveu entre 341 a.C. e 270 a.C.
II. Rutherford postulou que o átomo era uma esfera maciça de carga positiva com cargas negativas incrustadas na superfície.
III. O modelo de Bohr repousava na mecânica clássica e explicava perfeitamente a existência de órbitas estacionárias.
IV. O modelo atual foi concebido com as contribuições de De Broglie, Heisenberg e Schrödinger.
V. O número quântico spin foi introduzido por Wolfgang Pauli para explicar a descoberta da duplicação das raias espectrais.
Está correto o que se afirma somente em
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasPropriedades Coligativas: Tonoscopia, Ebulioscopia, Crioscopia e Pressão Osmótica.
Provas
Provas
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química OrgânicaIsomeria Plana e Espacial
- Química OrgânicaReações OrgânicasReações Orgânicas: Oxidação, Redução e Polimerização
Provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química CinéticaTransformações Químicas
Provas
- Química OrgânicaCadeias Carbônicas
- Química OrgânicaReações OrgânicasReações Orgânicas: Substituição, Adição e Eliminação
Provas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
É comum as estruturas dos compostos orgânicos apresentarem 2, 3 ou até 4 funções orgânicas. Observe a seguinte estrutura:
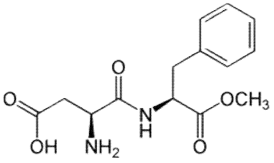
As funções orgânicas representadas na estrutura acima são:
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Um estudante misturou 50 mL de solução aquosa de ácido sulfúrico 0,10 mol/L com 50 mL de solução aquosa de hidróxido de sódio 0,40 mol/L e introduziu algumas gotas de fenolftaleina. O processo pode ser representado pela equação não balanceada:
H2SO4(aq) + NaOH(aq) → Na2SO4(aq) + H2O(l)
Ao término da reação, pode-se concluir acertadamente queProvas
A bateria de carro é um gerador de energiarelativamente barato, tem uma vida útil longa e umarecarga fácil. As semirreações dos eletrodos queconstituem as seis células da bateria convencionalnão selada, são:
Pb(s) + H2SO4(aq) →
PbSO4(s) + 2 H + + 2e- e0 = 0,36 Volts
PbO2(s) + H2SO4(aq) + 2e- + 2H+ →
PbSO4(s) + 2 H2O(l) e0 = 1,69 Volts
Considerando o enunciado acima, é correto afirmar que
Provas
Caderno Container