Foram encontradas 70 questões.
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Quais são as espécies predominantes nas soluções
aquosas descritas abaixo?
Solução I: solução aquosa de HCl (ácido forte)
Solução II: solução aquosa de NaOH (base forte)
Solução III: solução aquosa de HCN (ácido fraco)
Provas
Questão presente nas seguintes provas
A velocidade da reação: N2 + 3 H2 → 2 NH3 pode
ser calculada pela expressão (k é a constante de
velocidade): (x e y são constantes experimentais)
Provas
Questão presente nas seguintes provas
As reações de adição a alcenos:
I. São reações eletrofílicas, onde a ligação dupla se
comporta como uma base, já que participa com seus
elétrons nas reações.
II. Seguem, em geral, a orientação de Markovnikov, mas
adição de peróxidos pode mudar a sua estereoquímica,
sobretudo na reação com cloro.
III. Seguem sempre um mecanismo em uma etapa, onde
não há a formação de intermediários.
IV. Devido à alta reatividade dos alcenos, não necessitam
de catálise.
V. Não apresentam rearranjos.
Assinale a alternativa correta:
Assinale a alternativa correta:
Provas
Questão presente nas seguintes provas
Sobre equilíbrio químico, considere as afirmativas a
seguir e assinale a alternativa correta:
I. As reações não vão até o fim. Elas continuam até que a composição da mistura reacional corresponda ao mínimo de entalpia. Essa composição é descrita por uma constante de equilíbrio característica da reação que depende da temperatura, dentre outros fatores. II. Para controlar o rendimento de uma reação, precisamos entender a base termodinâmica do equilíbrio e como a posição atual de equilíbrio é afetada por condições como a temperatura e a pressão, por exemplo. III. O equilíbrio químico é o estágio da reação química em que não existe mais tendência a mudar a composição da mistura da reação, isto é, as concentrações ou pressões parciais dos reagentes e produtos. Como os equilíbrios físicos, todos os equilíbrios químicos são dinâmicos, com a reação direta e inversa ocorrendo com a mesma velocidade. IV. A termodinâmica descreve quantitativamente o equilíbrio, o que nos possibilita controlar a direção e o rendimento das reações. V. A composição de uma mistura de reação no equilíbrio é descrita pela constante de equilíbrio, que é dependente do produto das atividades dos produtos (elevadas a potências iguais aos coeficientes estequiométricos da equação química balanceada da reação) dividido pelo produto das atividades dos reagentes (elevadas a potências iguais a seus coeficientes estequiométricos).
Assinale a alternativa correta:
I. As reações não vão até o fim. Elas continuam até que a composição da mistura reacional corresponda ao mínimo de entalpia. Essa composição é descrita por uma constante de equilíbrio característica da reação que depende da temperatura, dentre outros fatores. II. Para controlar o rendimento de uma reação, precisamos entender a base termodinâmica do equilíbrio e como a posição atual de equilíbrio é afetada por condições como a temperatura e a pressão, por exemplo. III. O equilíbrio químico é o estágio da reação química em que não existe mais tendência a mudar a composição da mistura da reação, isto é, as concentrações ou pressões parciais dos reagentes e produtos. Como os equilíbrios físicos, todos os equilíbrios químicos são dinâmicos, com a reação direta e inversa ocorrendo com a mesma velocidade. IV. A termodinâmica descreve quantitativamente o equilíbrio, o que nos possibilita controlar a direção e o rendimento das reações. V. A composição de uma mistura de reação no equilíbrio é descrita pela constante de equilíbrio, que é dependente do produto das atividades dos produtos (elevadas a potências iguais aos coeficientes estequiométricos da equação química balanceada da reação) dividido pelo produto das atividades dos reagentes (elevadas a potências iguais a seus coeficientes estequiométricos).
Assinale a alternativa correta:
Provas
Questão presente nas seguintes provas
O ciclo do carbono está intimamente relacionado com
os seres vivos que vivem sobre a superfície terrestre.
Existem vários tipos de compostos de carbono nas
diversas etapas que compõem o ciclo. Esses compostos
podem ser líquidos, sólidos e gasosos. Muitos deles
são sintetizados pelos organismos vivos, com números
de oxidação variando de +4 a -4. Contudo, o transporte
de carbono entre os vários compartimentos (atmosfera,
hidrosfera e litosfera) é feito, principalmente, pelo
carbono com número de oxidação +4 na forma de gás
carbônico, carbonato ou bicarbonato.
Sobre o ciclo do carbono, analise as afirmativas que
seguem e assinale a alternativa correta:
I. No ciclo do carbono o gás carbônico na forma de gás é absorvido pelos vegetais durante a fotossíntese para formar a massa vegetal. II. Já os seres humanos e todos os demais seres vivos, ao respirarem, tanto aeróbica como anaerobicamente, liberam gás carbônico e energia, que pode ser aproveitada de diversas formas, inclusive por outros organismos. III. As reações de dissolução do gás carbônico em água são reações de equilíbrio, em fase líquida aquosa. Essas reações em equilíbrio podem participar de mecanismos de transporte de gás carbônico em meios aquosos tão diferentes como os que existem nos oceanos e do transporte de CO2 entre células e pulmões feito pelo sangue. IV. Os mesmos equilíbrios interagindo com íons metálicos podem resultar na formação de esqueletos e carapaças de organismos como conchas, casca de ovos ou na formação e dissolução de rochas e sedimentos. V. O ser humano interfere globalmente no ciclo do carbono adicionando quantidades significativas de gás carbônico na atmosfera, quando utiliza qualquer combustível contendo carbono proveniente de fonte não renovável.
Assinale a alternativa correta:
I. No ciclo do carbono o gás carbônico na forma de gás é absorvido pelos vegetais durante a fotossíntese para formar a massa vegetal. II. Já os seres humanos e todos os demais seres vivos, ao respirarem, tanto aeróbica como anaerobicamente, liberam gás carbônico e energia, que pode ser aproveitada de diversas formas, inclusive por outros organismos. III. As reações de dissolução do gás carbônico em água são reações de equilíbrio, em fase líquida aquosa. Essas reações em equilíbrio podem participar de mecanismos de transporte de gás carbônico em meios aquosos tão diferentes como os que existem nos oceanos e do transporte de CO2 entre células e pulmões feito pelo sangue. IV. Os mesmos equilíbrios interagindo com íons metálicos podem resultar na formação de esqueletos e carapaças de organismos como conchas, casca de ovos ou na formação e dissolução de rochas e sedimentos. V. O ser humano interfere globalmente no ciclo do carbono adicionando quantidades significativas de gás carbônico na atmosfera, quando utiliza qualquer combustível contendo carbono proveniente de fonte não renovável.
Assinale a alternativa correta:
Provas
Questão presente nas seguintes provas
Sobre a teoria atômica, considere as seguintes
afirmações e assinale a alternativa correta: I. Dalton chegou à conclusão da existência de átomos
com base em observações químicas macroscópicas e
não teve evidências diretas da existência de átomos.
II. Os experimentos de Thomson sobre o comportamento
dos raios catódicos em campos magnéticos e elétricos
proporcionaram a descoberta dos elétrons e permitiram
que sua razão carga-massa fosse medida.
III. Os estudos de Rutherford mostraram que o átomo tinha
um núcleo denso, carregado positivamente.
IV. De Broglie, Heisenberg, Born, Bohr e Planck foram
cientistas que colaboraram para a teoria quântica
moderna.
V. A dualidade onda-partícula, o princípio da incerteza, as
funções de onda, a equação de Schrödinger, o princípio
da exclusão de Pauli são contribuições recentes para a
teoria atômica.
Assinale a alternativa correta:
Assinale a alternativa correta:
Provas
Questão presente nas seguintes provas
Considere a reação C4H9Br(aq) + OH-
(aq) → C4H9 OH(aq)
+ Br- (aq) e o fato de que em determinado experimento
quando a concentração de 2-bromo-2-metilpropano, C4H9Br, foi dobrada, a velocidade da reação aumentou
por um fator de 2 e que quando as concentrações
de C4H9Br e OH-
foram dobradas simultaneamente, o
aumento da velocidade foi o mesmo, um fator de 2.
Após analisar as afirmativas a seguir, assinale a
alternativa correta.
I. Um solvente polar aprótico favoreceria a reação.
II. O mecanismo de reação corresponde a uma substituição
nucleofílica bimolecular.
III. Nesse tipo de reação não há a formação de intermediário.
IV. Não é possível a formação de isômeros como produtos
nessa reação.
V. A reação é de 1ª
ordem em relação a C4H9Br, ordem 0
em relação a OH- e ordem global 1.
Assinale a alternativa correta:
Assinale a alternativa correta:
Provas
Questão presente nas seguintes provas
A reação: (CH3 )3CCl + OH-
→ (CH3)3COH + Cl-
foi estudada
em solução aquosa e o mecanismo proposto é:
(CH3)3CCl → (CCH3)3C+ + Cl-
(etapa lenta, constante de
velocidade = k1)
(CH3)3C+ + OH- → (CH3)3COH (etapa rápida, constante
de velocidade = k2)
Para esse processo podemos afirmar que:
Provas
Questão presente nas seguintes provas
O diagrama abaixo representa a variação de energia
durante a reação: A ⇆ B. Assinale a alternativa que
corresponde à sequência correta para preenchimento
das lacunas: 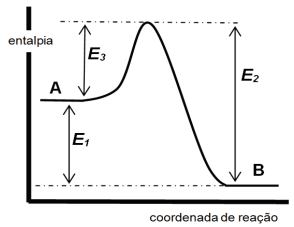 ( ) corresponde à entalpia da reação direta
( ) corresponde à energia de ativação da reação direta
( ) corresponde à entalpia da reação inversa
( ) corresponde à energia de ativação da reação inversa
( ) corresponde à entalpia da reação direta
( ) corresponde à energia de ativação da reação direta
( ) corresponde à entalpia da reação inversa
( ) corresponde à energia de ativação da reação inversa
Assinale a alternativa correta:
 ( ) corresponde à entalpia da reação direta
( ) corresponde à energia de ativação da reação direta
( ) corresponde à entalpia da reação inversa
( ) corresponde à energia de ativação da reação inversa
( ) corresponde à entalpia da reação direta
( ) corresponde à energia de ativação da reação direta
( ) corresponde à entalpia da reação inversa
( ) corresponde à energia de ativação da reação inversa
Assinale a alternativa correta:
Provas
Questão presente nas seguintes provas
Utilize os dados abaixo para responder a questão 37.

Escreva as semi-reações de cátodo e ânodo e a equação balanceada para os sistemas representados a seguir. Em cada caso faça um esquema da célula galvânica, calcule o valor de ΔE° e determine se corresponde a uma pilha ou eletrólise. Na sequência, assinale a alternativa correta.
Sistemas:
I. Pt(s) | Fe2+(aq), Fe3+(aq) | | Ag+(aq) | Ag(s)
II. Pt(s) | Cl- (aq) | Cl2(g) | | H+(aq) | H2(g) | C(gr)
III. V(s) | V2+(aq) | | U3+(aq) | U(s)
IV. Hg(l) | Cl- (aq) | Hg2Cl2(s) | | Sn4+(aq), Sn2+(aq) | Pt(s)
Assinale a alternativa correta:
:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container