Foram encontradas 70 questões.
Considere a tabela abaixo para responder a questão 38.
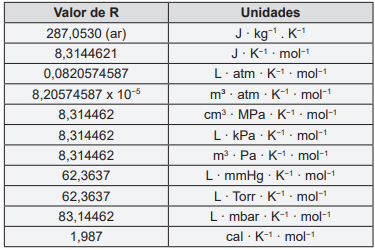
Massas atômicas (u): C = 12,01, O = 16,00, H = 1,01
Analise as seguintes afirmativas e a seguir assinale a alternativa correta:
I. Um tanque de oxigênio armazenado fora de um edifício tem uma pressão de 20,00 atm às 6:00 h da manhã, quando a temperatura está em torno de 10°C. A pressão no tanque às 18:00 h quando a temperatura chega a 30°C é 21,41 atm.
II. Um motor de automóvel mal ajustado pode liberar, em marcha lenta, até 1,00 mol de monóxido de carbono por minuto. A 27°C, o volume desse gás, a 1 atm de pressão que pode ser liberado por minuto é 24,61 L.
III. O óleo produzido a partir de folhas de eucalipto contém o composto volátil eucaliptol. Esse composto tem densidade 0,320 g L-1 a 190°C e 60,0 mmHg. A massa molar do eucaliptol gasoso é 153,89 g mol-1.
IV. O volume de gás carbônico (a 25°C e 1 atm) necessário para que uma planta produza 1,00 g de glicose (C6H12O6) por fotossíntese é 815 mL.
V. A composição do ar seco, em volume, é: 78% de nitrogênio, 21% de oxigênio e 1% de argônio. As pressões parciais desses gases no ar a uma pressão atmosférica de 1 atm são respectivamente, p(N2) = 0,78 atm, p(O2) = 0,21 atm e p(Ar) = 0,01 atm.
Assinale a alternativa correta:
Provas
- Sistemas de EquilíbrioSistemas Heterogêneos: Produto de Solubilidade (Kps)
- Sistemas de EquilíbrioSistemas Homogêneos: Constantes: Kc e Kp. Deslocamento do Equilíbrio: Fatores
Provas
- Química OrgânicaPropriedades Químicas dos Compostos Orgânicos
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Provas
- Química OrgânicaGlicídios, Lipídios, Aminoácidos e Proteínas.
- Química OrgânicaIsomeria Plana e Espacial
*Grupo farmacofórico é o conjunto de características eletrônicas e estéricas que caracterizam um ou mais grupos funcionais ou subunidades estruturais, necessários ao melhor reconhecimento molecular pelo receptor e, portanto, para o efeito farmacológico desejado
Assinale a alternativa correta:
Provas
- FundamentosPropriedades das Substâncias
- FundamentosTransformações: Estados Físicos e Fenômenos
- Química OrgânicaPropriedades Físicas dos Compostos Orgânicos
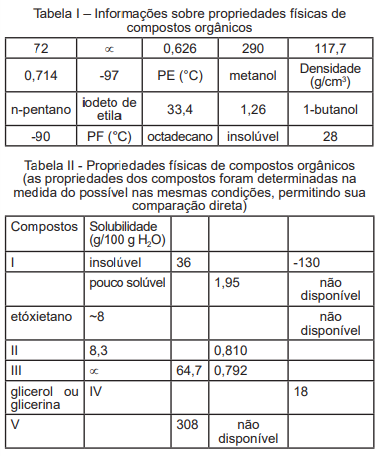 I. Sabendo-se que o composto I tem densidade de
0,626 g/cm3
, a menor densidade da lista de compostos
apresentados, ele certamente representa o n-pentano,
pois tal composto possui também baixo ponto de
ebulição e é insolúvel em água.
II. O composto II representa o n-butanol e seu ponto de
fusão é -97°C.
III. O composto III representa o metanol e sua mais alta
solubilidade em relação ao n-butanol está relacionada a
sua maior interação por ligação de hidrogênio, já que a
molécula é menor.
IV. A glicerina ou glicerol (também conhecida como 1, 2, 3-
propanotriol) tem ponto de ebulição muito alto, 290°C,
devido aos grupos hidroxila, mesmo motivo que deixa
este composto extremamente solúvel em água. Assim
sendo, IV representa o símbolo do infinito.
V. O composto V é sólido à temperatura ambiente de 25°C. Assinale a alternativa correta:
I. Sabendo-se que o composto I tem densidade de
0,626 g/cm3
, a menor densidade da lista de compostos
apresentados, ele certamente representa o n-pentano,
pois tal composto possui também baixo ponto de
ebulição e é insolúvel em água.
II. O composto II representa o n-butanol e seu ponto de
fusão é -97°C.
III. O composto III representa o metanol e sua mais alta
solubilidade em relação ao n-butanol está relacionada a
sua maior interação por ligação de hidrogênio, já que a
molécula é menor.
IV. A glicerina ou glicerol (também conhecida como 1, 2, 3-
propanotriol) tem ponto de ebulição muito alto, 290°C,
devido aos grupos hidroxila, mesmo motivo que deixa
este composto extremamente solúvel em água. Assim
sendo, IV representa o símbolo do infinito.
V. O composto V é sólido à temperatura ambiente de 25°C. Assinale a alternativa correta:Provas
- Química OrgânicaCadeias Carbônicas
- Química OrgânicaHidrocarbonetos
- Química OrgânicaPropriedades Físicas dos Compostos Orgânicos
Provas
Assinale a alternativa correta:
Provas
- Química OrgânicaIsomeria Plana e Espacial
- Química OrgânicaPropriedades Físicas dos Compostos Orgânicos
- Química OrgânicaPropriedades Químicas dos Compostos Orgânicos
Provas
I. São favorecidas por solventes polares próticos. II. Podem resultar em misturas de isômeros ópticos. III. Podem apresentar como produtos secundário alcenos. IV. Podem ser mono ou bimoleculares. V. Podem apresentar rearranjos.
Assinale a alternativa correta:
Provas
Assinale a alternativa correta:
Provas
Caderno Container