Foram encontradas 50 questões.
Uma célula galvânica é montada com um eletrodo consistindo de uma lâmina de zinco metálico imersa em solução aquosa 1,0 mol.L-1 de sulfato de zinco. O outro eletrodo é o de hidrogênio, com pressão parcial do gás igual a 1 bar e concentração de íons H3 O+ igual a 0,01 mol.L-1 , a 25°C. A força eletromotriz desta célula, em volts, é aproximadamente igual a:
Dados:
Zn 2+(aq) + 2è → Zn(s) E0 = - 0,76V
Dados:
Zn 2+(aq) + 2è → Zn(s) E0 = - 0,76V
2H+(aq) + 2è → H 2(g)E0 = 0,00V
Provas
Questão presente nas seguintes provas
Clorobenzeno (C6 H5 Cl) e bromobenzeno (C6 H5 Br) formam soluções ideais. A 100°C, a pressão de vapor do bromobenzeno é de 137 mmHg e a do clorobenzeno é de 285 mmHg. Considere uma solução contendo 30,0% em massa de bromobenzeno em clorobenzeno a esta temperatura. A pressão de vapor da solução, em mmHg, é aproximadamente igual a:
Dados: massas molares (g.mol -1 ),
H=1, C=12, Cl=35,5, Br=80
Dados: massas molares (g.mol -1 ),
H=1, C=12, Cl=35,5, Br=80
Provas
Questão presente nas seguintes provas
As Leis da Termodinâmica explicam as variações de energia e a tendência de ocorrência dos processos de modo espontâneo, sendo essenciais para a compreensão da Química. Considerando, por exemplo, um processo que é exotérmico, em relação à espontaneidade, à variação de entropia (ΔS) e à temperatura, pode-se afirmar que:
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
- Química OrgânicaTipos de Reagentes e Mecanismos das Reações Orgânicas
Um químico orgânico recebeu em seu laboratório uma amostra de um líquido para ser identi?cada. Os primeiros testes (cromatogra?a em camada delgada, ponto de ebulição) mostraram tratar-se de uma substância pura. A amostra apresentou resultado negativo nas reações com permanganato de potássio (um agente oxidante forte) e com o reagente de Tollens (espelho de prata). No entanto, apresentou resultado positivo nos testes com iodofórmio e com 2,4-dinitrofenilhidrazina. A partir dessas informações, o tipo de substância que pode ser o líquido analisado é:
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
- Transformações Químicas e EnergiaTermoquímica
O ácido benzoico tem entalpia padrão de combustão igual a -3227 kJ.mol -1 . Para calibrar um calorímetro, foram usados 2,27 g deste ácido, aumentando em 5,0°C a temperatura do calorímetro. Em seguida, com o calorímetro a 25°C, promoveu-se a queima de 1,6 g de acetileno (etino) e a temperatura subiu para 31,7°C. A entalpia padrão de combustão do acetileno, em kJ.mol -1 , é aproximadamente igual a:
Dados: Massas molares (g.mol -1 ), H= 1, C=12, O=16
Dados: Massas molares (g.mol -1 ), H= 1, C=12, O=16
Provas
Questão presente nas seguintes provas
A possibilidade de estabelecimento de ligação entre dois átomos pode ser definida em termos de um parâmetro denominado ordem de ligação (O.L), que pode ser determinada a partir do número de elétrons em orbitais ligantes e antiligantes em diagramas de energia dos orbitais, usando-se a Teoria dos Orbitais Moleculares (TOM). Considerando o parâmetro acima citado, a associação correta entre a molécula e sua ordem de ligação está presente em:
Provas
Questão presente nas seguintes provas
A atividade biológica de compostos quirais pode variar muito de um enantiômero para outro. O caso mais célebre ocorreu com a talidomida, que causou defeitos congênitos (teratogênese) em fetos de grávidas que fizeram uso de medicamentos contendo misturas de seus isômeros ópticos, cujas estruturas estão indicadas a seguir:
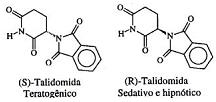
Considere um medicamento que continha um excesso enantiomérico de 50%, em relação ao isômero (R). Pode-se afirmar, então, que a composição percentual da mistura era igual a:
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma amostra de 0,265 g de um antibiótico em pó foi dissolvida em HCl e completou-se o volume até 100,00 mL de solução. Uma alíquota de 25,00 mL foi transferida para um balão, seguida da adição de 25,00 mL de solução aquosa 0,018 mol.L–1 de KBrO3. Um excesso de KBr foi adicionado para formar Br2, segundo a equação a seguir: BrO3– + 5Br – + 6H+ → 3Br2 + 3H2O
O bromo formado reage com toda a sulfanilamida presente no antibiótico e, após um tempo, é adicionado excesso de KI, para reagir com o excesso de bromo, formando I2. Finalmente, o iodo formado é titulado, consumindo 13,00 mL de uma solução aquosa 0,12 mol.L–1 de tiossulfato de sódio. As demais equações químicas são:
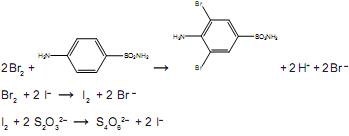
A porcentagem de sulfanilamida presente na amostra do antibiótico em pó é aproximadamente igual a:
Dado: Massa molar da sulfanilamida= 172 g. mol -1
Provas
Questão presente nas seguintes provas
Ernest Rutherford (1871-1937) foi quem descobriu que, se um núcleo radioativo se desintegra emitindo uma partícula α ou β, o núcleo resultante é, em regra, também radioativo e, mais cedo ou mais tarde, acaba expulsando alguma partícula para converter- se em outro núcleo, e assim por diante, até terminar num núcleo estável, isto é, não radioativo. Considere o nuclídeo urânio-238 que, após uma série de emissões, transforma-se no chumbo-206. A quantidade de partículas alfa e beta emitidas nesta série radioativa é, respectivamente, igual a:
Provas
Questão presente nas seguintes provas
O álcool benzílico (ou fenilmetanol) é um álcool aromático líquido. É utilizado como componente de fragrâncias e aromas, como preservante para produtos oftálmicos, injetáveis e orais, sendo também usado como solvente e como um produto químico intermediário para reações orgânicas. A reação do álcool benzílico com uma solução aquosa básica de permanganato de potássio produz um composto A que, após purificação, reage com excesso de etanol, sob catálise ácida, formando um produto orgânico B, também de aplicação industrial, cujo nome é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container