Foram encontradas 50 questões.
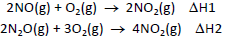
A variação de entalpia da reação N2O(g) + 1/2O2 (g) → 2NO(g) pode ser determinada como
Provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
O cloreto de tionila, composto inorgânico com a fórmula SOC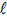 2 ,
é um reagente químico muito usado em reações de cloração. É
um líquido incolor, destilável à temperatura ambiente que
decompõe-se acima de 140ºC. É um composto de S(IV) formado
por ligações químicas de natureza covalente.
2 ,
é um reagente químico muito usado em reações de cloração. É
um líquido incolor, destilável à temperatura ambiente que
decompõe-se acima de 140ºC. É um composto de S(IV) formado
por ligações químicas de natureza covalente.
Assinale a opção que melhor representa a estrutura geométrica de equilíbrio do cloreto de tionila.
Provas
Provas
Provas
Provas
- Gases
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
Em um laboratório foi montada uma aparelhagem para recolhimento do gás oxigênio produzido na reação de decomposição do clorato de potássio, como ilustra a figura a seguir.
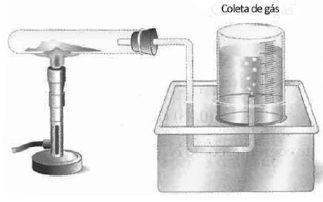
A reação observada pode ser representada pela equação:
2 KClO3 → 2 KCl+ 3 O2
Uma amostra de clorato de potássio foi parcialmente decomposta sendo a pressão do gás recolhido de 0,8 atm e seu volume de 180 mL na temperatura de 27ºC. Considerando o comportamento ideal do gás, a massa de clorato de potássio que sofreu decomposição foi de, aproximadamente,
Dados: Massa Molar: KClO3 = 122,5 g.mol-1
Constante real dos gases R= 0,082atm.L.mol-1 .K-1
Provas
Uma técnica usada em laboratórios químicos é a determinação das fórmulas empíricas (mínimas) pela análise por combustão. Nesse processo, queima-se uma amostra em um tubo por onde passa um fluxo abundante de oxigênio, sendo todo o hidrogênio do composto convertido em água e todo o carbono convertido em dióxido de carbono.
O equipamento utilizado é representado pela figura a seguir.
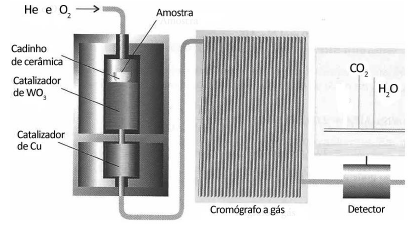
Na análise por combustão de 6,0 g de um hidrocarboneto recém-sintetizado foi determinada a massa de 17,6 g de dióxido de carbono e 10,8 g de água.
A fórmula empírica desse composto é:
Dados: Massas Molares: H = 1g.mol-1 C = 12g.mol-1 O=16g.mol-1
Provas
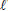 )
) Esta reação, descoberta pelo químico francês Paul Sabatier, tem sido estudada para remover CO2 de atmosferas artificiais como em espaçonaves. Considerando que um indivíduo libere para o ambiente 0,6 kg de dióxido de carbono por dia, e que 80% desse gás será removido pelo processo de Sabatier, a massa de metano produzida por dia é de Dados: Massas Molares: H = 1g.mol-1 C = 12g.mol-1 O=16g.mol-1
Provas
O posicionamento dos metaloides entre os metais e os não-metais é o nosso primeiro exemplo das tendências na variação das propriedades quando nos deslocamos na tabela periódica. Frequentemente veremos que, à medida que mudamos de posição em um período ou em um grupo, as propriedades físicas e químicas variam de modo mais ou menos regular. Há poucas variações abruptas nas características dos elementos quando nos deslocamos horizontalmente ao longo de um período ou verticalmente através de um grupo.
(Brady, J.; Senese, F. Química a matéria e suas transformações Vol 1, 5ª Ed. Rio de janeiro: LTC. 2009)
Com relação aos raios dos átomos, analise as afirmativas a seguir.
I. O raio do ferro é menor que o raio do potássio.
II. O raio do paládio é maior que o raio do níquel.
III. O raio do manganês e maior que o raio do estrôncio
Está correto o que se afirma em
Provas
Provas
Caderno Container