Foram encontradas 65 questões.
A isomeria é um fenômeno no qual compostos orgânicos
apresentam a mesma fórmula molecular, mas diferentes
disposições de seus átomos, resultando em propriedades físicas e
químicas distintas. O tipo de isomeria que um composto orgânico
apresenta depende diretamente de sua estrutura molecular e do
arranjo dos seus átomos ou grupos funcionais.
Com base na estrutura dos compostos orgânicos e seus tipos de isomeria, é correto afirmar que
Com base na estrutura dos compostos orgânicos e seus tipos de isomeria, é correto afirmar que
Provas
Questão presente nas seguintes provas
Sobre as funções orgânicas e suas respectivas estruturas
moleculares, as alternativas a seguir:
I. Os éteres possuem um átomo de oxigênio entre dois grupos alquila ou arila.
II. Os ácidos carboxílicos apresentam o grupo funcional -OH ligado diretamente a um carbono com ligação dupla com oxigênio.
III. As cetonas possuem o grupo funcional carbonila (C=O) localizado no final da cadeia carbônica.
IV. As aminas contêm um grupo amino (-NH₂), sendo compostos básicos.
V. Os alcenos possuem pelo menos uma ligação tripla entre carbonos em sua estrutura.
Estão corretas as afirmativas
I. Os éteres possuem um átomo de oxigênio entre dois grupos alquila ou arila.
II. Os ácidos carboxílicos apresentam o grupo funcional -OH ligado diretamente a um carbono com ligação dupla com oxigênio.
III. As cetonas possuem o grupo funcional carbonila (C=O) localizado no final da cadeia carbônica.
IV. As aminas contêm um grupo amino (-NH₂), sendo compostos básicos.
V. Os alcenos possuem pelo menos uma ligação tripla entre carbonos em sua estrutura.
Estão corretas as afirmativas
Provas
Questão presente nas seguintes provas
Ácido acetilsalicílico é um anti-inflamatório não esteroide indicado
para dor de dente, dor de cabeça, febre, artrite reumatoide,
artrose ou para reduzir o risco de infarto agudo do miocárdio e do
AVC, pois tem ação anti-inflamatória, antitérmica, analgésica e
anticoagulante. Sua fórmula estrutural é:
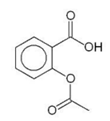
As funções orgânicas presentes nesse composto são

As funções orgânicas presentes nesse composto são
Provas
Questão presente nas seguintes provas
A separação de dois líquidos miscíveis, como etanol e água, pode
ser feita por destilação, que se baseia nas diferenças de ponto de
ebulição dos líquidos. A mistura é aquecida e o componente com
menor ponto de ebulição evapora primeiro, sendo condensado em
outro recipiente. Para separar líquidos com pontos de ebulição
próximos, utiliza-se a destilação fracionada, que envolve uma
coluna de fracionamento para melhorar a separação. A eficiência
do processo depende de fatores como a diferença de temperatura
de ebulição e a pressão aplicada.
Na separação de dois líquidos miscíveis por destilação fracionada, a eficiência da separação quantitativa depende
Na separação de dois líquidos miscíveis por destilação fracionada, a eficiência da separação quantitativa depende
Provas
Questão presente nas seguintes provas
Uma massa fixa de um gás ideal passa pelo ciclo ABCD, como
mostrado na Figura abaixo, dentro de um pistão (cilindro com
êmbolo). A temperatura no ponto A é igual a 750 K.
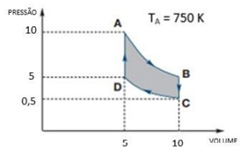
Com relação às diferentes etapas do ciclo, avalie as afirmativas a seguir:
I. A etapa de A para B se caracteriza por uma expansão isocórica.
II. A etapa de B para C se caracteriza por uma compressão adiabática.
III. A etapa de C para D se caracteriza por uma expansão isotérmica.
IV. A etapa de D para A se caracteriza por uma compressão isocórica.
Está correto o que se afirma em

Com relação às diferentes etapas do ciclo, avalie as afirmativas a seguir:
I. A etapa de A para B se caracteriza por uma expansão isocórica.
II. A etapa de B para C se caracteriza por uma compressão adiabática.
III. A etapa de C para D se caracteriza por uma expansão isotérmica.
IV. A etapa de D para A se caracteriza por uma compressão isocórica.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
A tabela periódica dos elementos organiza os elementos químicos
de acordo com suas propriedades atômicas e características
periódicas. Uma dessas propriedades é a eletronegatividade, que
mede a tendência de um átomo em atrair elétrons em uma ligação
química. Considerando a posição de elementos na tabela periódica
e as tendências periódicas, podemos fazer comparações entre
suas eletronegatividades e prever seu comportamento químico.
Com base na tendência da eletronegatividade na tabela periódica, assinale a afirmativa correta acerca da comparação entre as eletronegatividades dos elementos indicados.
Com base na tendência da eletronegatividade na tabela periódica, assinale a afirmativa correta acerca da comparação entre as eletronegatividades dos elementos indicados.
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
As propriedades físicas e químicas das substâncias são fortemente
influenciadas pela polaridade de suas ligações químicas e pelas
interações intermoleculares resultantes. Compreender essas
interações é fundamental para explicar fenômenos como
solubilidade, ponto de ebulição e viscosidade das substâncias.
Considerando essas informações, é correto afirmar que
Considerando essas informações, é correto afirmar que
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A solubilidade dos compostos inorgânicos em água varia
consideravelmente e é um parâmetro crucial para prever a
quantidade máxima de uma substância que pode ser dissolvida
em uma determinada quantidade de água. Dessa forma, o
entendimento da solubilidade de compostos como cloretos,
nitratos e sulfatos torna-se essencial para a manipulação e o uso
correto desses materiais.
A tabela abaixo apresenta as solubilidades de alguns compostos inorgânicos a 25 °C, em gramas por 100 mL de água:
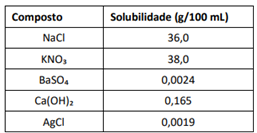
Com base na tabela, a quantidade máxima de soluto (em gramas) que poderia ser dissolvida em 250 mL de água a 25ºC para formar uma solução saturada é
A tabela abaixo apresenta as solubilidades de alguns compostos inorgânicos a 25 °C, em gramas por 100 mL de água:

Com base na tabela, a quantidade máxima de soluto (em gramas) que poderia ser dissolvida em 250 mL de água a 25ºC para formar uma solução saturada é
Provas
Questão presente nas seguintes provas
A pirita (FeS₂) é um minério importante para a obtenção de ferro
e enxofre em processos industriais. Suponha que 500 g de um
minério de pirita com 96% de pureza seja utilizado para a produção
de dióxido de enxofre (SO₂), gás liberado durante a queima da
pirita em presença de oxigênio, conforme a equação não
balanceada a seguir:
FeS2(s)+O2(g)⟶Fe2O3(s)+SO2(g)
Sabendo que a massa molar da pirita (FeS₂) é 120 g/mol, a massa de SO₂ produzida a partir da queima total do minério utilizado é de
FeS2(s)+O2(g)⟶Fe2O3(s)+SO2(g)
Sabendo que a massa molar da pirita (FeS₂) é 120 g/mol, a massa de SO₂ produzida a partir da queima total do minério utilizado é de
Provas
Questão presente nas seguintes provas
Sistemas químicos com reações em fase gasosa são muito comuns
em processos industriais e naturais. Nesses sistemas, os reagentes
e produtos estão na forma de gases, e suas propriedades são
descritas por equações de estado, como a equação do gás ideal.
Essa equação é útil para descrever sistemas que estejam operando
a pressões moderadas e a altas temperaturas.
Considerar a reação de síntese da amônia em fase gasosa, representada pela equação química:
N₂(g) + 3H₂(g) ⇌ 2NH₃(g)
Se inicialmente forem colocados 2 mols de N₂ e 6 mols de H₂ em um reator fechado de volume fixo de 10 L e a uma temperatura de 300 K e, após o equilíbrio ser atingido, restar 1 mol de N₂, a pressão total do sistema, assumindo comportamento ideal dos gases será de
[Dado: constante universal dos gases (R)=0,082 (atm.L)/(mol.K)]
Considerar a reação de síntese da amônia em fase gasosa, representada pela equação química:
N₂(g) + 3H₂(g) ⇌ 2NH₃(g)
Se inicialmente forem colocados 2 mols de N₂ e 6 mols de H₂ em um reator fechado de volume fixo de 10 L e a uma temperatura de 300 K e, após o equilíbrio ser atingido, restar 1 mol de N₂, a pressão total do sistema, assumindo comportamento ideal dos gases será de
[Dado: constante universal dos gases (R)=0,082 (atm.L)/(mol.K)]
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container