Foram encontradas 65 questões.
A eletroquímica é responsável por entender processos de oxidação
e redução que ocorrem em dispositivos como pilhas e baterias,
onde energia química é convertida em energia elétrica. Um dos
seus princípios fundamentais é o potencial eletroquímico, que
determina a tendência de uma substância em perder ou ganhar
elétrons. Esse estudo permite aplicações em diversas áreas, como
produção de energia, galvanoplastia e proteção contra corrosão.
Em uma célula eletroquímica, o potencial padrão de redução do
cátodo é +0,34V e o do ânodo é −0,76V. Se a célula operar a
25°C, sua diferença de potencial padrão (E0) e a reação
espontânea que ocorre nessa condição são, respectivamente,
iguais a:
Provas
Questão presente nas seguintes provas
A Tabela abaixo apresenta dados de concentração de íons hidrogênio [H+ ] de algumas soluções:
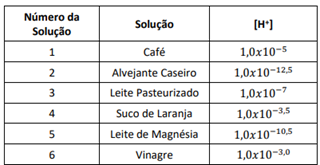
Com base na Tabela, considere as seguintes afirmações:
I. O vinagre é cem vezes mais ácido que o café.
II. A [H+ ] na solução 4 é igual à [OH- ] na solução 2.
III. A solução 4 é dez vezes mais básica que a solução 5.
IV. Na tabela há três soluções ácidas e 2 soluções básicas.
Está correto o que se afirma em:
Provas
Questão presente nas seguintes provas
Um sistema termodinâmico passa por uma reação química a uma
temperatura constante de 300 K. Sabe-se que a variação de
entalpia (ΔH) é de 50 kJ/mol e a variação de entropia (ΔS) é de 0,1
kJ/(mol·K).
Com base nessas informações assinale a afirmativa correta acerca da espontaneidade do processo e da variação de energia livre de Gibbs ΔG.
Com base nessas informações assinale a afirmativa correta acerca da espontaneidade do processo e da variação de energia livre de Gibbs ΔG.
Provas
Questão presente nas seguintes provas
A reação de transformação da glicose em ácido lático, é
representada por:
C6H12O6 → 2C3H6O3 glicose ácido lático
Essa reação apresenta uma variação de entalpia, a 25 °C, igual a −21 kcal/(mol de glicose) e a reação de combustão total de ácido lático apresenta uma entalpia padrão de combustão igual a −326 kcal/(mol de ácido lático)
A partir dessas informações, a entalpia padrão de combustão da glicose em kcal/(mol de glicose) é
C6H12O6 → 2C3H6O3 glicose ácido lático
Essa reação apresenta uma variação de entalpia, a 25 °C, igual a −21 kcal/(mol de glicose) e a reação de combustão total de ácido lático apresenta uma entalpia padrão de combustão igual a −326 kcal/(mol de ácido lático)
A partir dessas informações, a entalpia padrão de combustão da glicose em kcal/(mol de glicose) é
Provas
Questão presente nas seguintes provas
A energia nuclear é produzida em reatores por meio da fissão de
átomos pesados, como o urânio-235, que, ao se dividir, libera
grande quantidade de energia em forma de calor. Esse calor é
transformado em eletricidade, mas o uso dessa tecnologia exige
rigorosos controles de segurança para evitar acidentes e o
gerenciamento dos resíduos radioativos gerados, que podem ser
nocivos para o ambiente e a saúde humana.
Com relação à radioatividade e ao uso de energia nuclear, assinale a afirmativa correta.
Com relação à radioatividade e ao uso de energia nuclear, assinale a afirmativa correta.
Provas
Questão presente nas seguintes provas
Com base nas estruturas de moléculas complexas de fármacos,
analise as sentenças abaixo e assinale (V) para as verdadeiras e (F)
para as falsas:
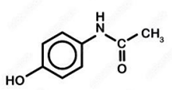
( ) O paracetamol (C₈H₉NO₂) possui uma função amida e um grupo hidroxila.
Paracetamol
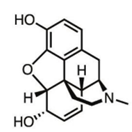
( ) A morfina (C₁₇H₁₉NO₃) contém grupos amina e álcool, o que contribui para sua ação no sistema nervoso.
Morfina
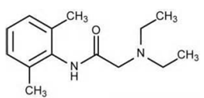
( ) A lidocaína (C₁₄H₂₂N₂O) é um anestésico local que apresenta em sua estrutura uma função éster.
Lidocaína
As afirmativas são, respectivamente,
( ) O paracetamol (C₈H₉NO₂) possui uma função amida e um grupo hidroxila.
Paracetamol

( ) A morfina (C₁₇H₁₉NO₃) contém grupos amina e álcool, o que contribui para sua ação no sistema nervoso.
Morfina

( ) A lidocaína (C₁₄H₂₂N₂O) é um anestésico local que apresenta em sua estrutura uma função éster.
Lidocaína

As afirmativas são, respectivamente,
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Diluição, mistura de soluções, análise volumétrica e gravimétrica e
propriedades coligativas são conceitos centrais para o estudo e
aplicação das soluções. A diluição envolve a redução da
concentração de uma solução, enquanto a mistura pode alterar
propriedades ou concentração final. A análise volumétrica
determina a concentração de uma substância em solução por
titulação, e a gravimétrica se baseia na medição de massa. Já as
propriedades coligativas dependem apenas do número de
partículas dissolvidas, influenciando fenômenos como pressão
osmótica e ponto de ebulição.
Uma solução de NaCl (não volátil) é preparada dissolvendo-se 5,85 g do sal em 500 mL de água pura a 25°C. Considere a massa molar de NaCl = 58,5 g/(mol NaCl) e a densidade da água = 1,00 g/mL. Sobre as propriedades e características dessa solução, é correto afirmar que
Uma solução de NaCl (não volátil) é preparada dissolvendo-se 5,85 g do sal em 500 mL de água pura a 25°C. Considere a massa molar de NaCl = 58,5 g/(mol NaCl) e a densidade da água = 1,00 g/mL. Sobre as propriedades e características dessa solução, é correto afirmar que
Provas
Questão presente nas seguintes provas
O ouro é encontrado livre na natureza (ouro nativo). O ouro puro
normalmente é denominado ouro 24 quilates (100% puro). Essa
terminologia tem origem muito antiga. Uma joia feita de ouro 18
quilates contém 75% de ouro em massa, enquanto os 25%
restantes são compostos por prata e cobre. Sabendo que um anel
de ouro 18 quilates pesa 12 gramas.
Considerando a massa atômica do ouro aproximadamente igual a 200 u, o número de átomos de ouro presente no anel é
Considerando a massa atômica do ouro aproximadamente igual a 200 u, o número de átomos de ouro presente no anel é
Provas
Questão presente nas seguintes provas
As funções orgânicas são classificações que agrupam compostos
com propriedades químicas semelhantes, devido à presença de
grupos funcionais específicos. Esses grupos são responsáveis pelas
características e reatividade das moléculas.
A esse respeito, avalie cada afirmativa a seguir e assinale (V) para as verdadeiras e (F) para as falsas:
( ) Os ácidos carboxílicos apresentam o grupo funcional -OH ligado diretamente a um carbono com ligação dupla com oxigênio.
( ) As cetonas possuem o grupo funcional carbonila (C=O) localizado no final da cadeia carbônica.
( ) As aminas contêm um grupo amino (-NH₂), sendo compostos básicos.
As afirmativas são, respectivamente,
A esse respeito, avalie cada afirmativa a seguir e assinale (V) para as verdadeiras e (F) para as falsas:
( ) Os ácidos carboxílicos apresentam o grupo funcional -OH ligado diretamente a um carbono com ligação dupla com oxigênio.
( ) As cetonas possuem o grupo funcional carbonila (C=O) localizado no final da cadeia carbônica.
( ) As aminas contêm um grupo amino (-NH₂), sendo compostos básicos.
As afirmativas são, respectivamente,
Provas
Questão presente nas seguintes provas
O acetileno (C₂H₂) é amplamente utilizado em maçaricos de
oxiacetileno devido à sua capacidade de liberar grandes
quantidades de calor durante sua combustão. A reação de
combustão completa do acetileno em oxigênio puro pode ser
representada pela seguinte equação não balanceada:
C2H2(g) + O2(g)⟶ CO2(g)+ H2O(g)
Sabendo que a combustão de 1 mol de acetileno libera aproximadamente 1300 kJ de energia, a quantidade de calor liberada na combustão completa de 52 g de acetileno é de aproximadamente
C2H2(g) + O2(g)⟶ CO2(g)+ H2O(g)
Sabendo que a combustão de 1 mol de acetileno libera aproximadamente 1300 kJ de energia, a quantidade de calor liberada na combustão completa de 52 g de acetileno é de aproximadamente
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container