Foram encontradas 550 questões.
Observe a lista de itens que compõem uma Sala de Recursos Multifuncionais.
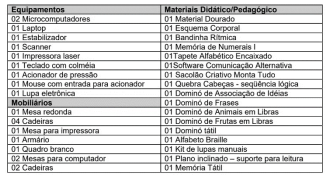
De acordo com a planilha apresentada, as afirmativas a seguir indicam corretamente recursos disponíveis e seus usos, à exceção de uma. Assinale-a.
Provas
Questão presente nas seguintes provas
Ao longo do século XX, a indústria farmacêutica produziu uma
série de novas drogas. Na década de 1960, por exemplo, químicos
norte-americanos sintetizaram o flurbiprofeno, um anti-inflamatório não-esteroide usado em casos de artrite e de dor de
dentes. Uma amostra de 6,1mg de flurbiprofeno foi analisada e
revelou a presença de 4,5 mg de carbono e, ainda, que a massa
molar do composto é 244g . mol–1
.
O número de átomos de carbono presentes na fórmula molecular do flurbiprofeno é igual a
O número de átomos de carbono presentes na fórmula molecular do flurbiprofeno é igual a
Provas
Questão presente nas seguintes provas
A metilamina (CH3NH2) é importante matéria-prima na indústria
química. Esse composto é um gás incolor, com forte odor, sendo
comumente comercializado na forma de solução aquosa. Em
água, o seguinte equilíbrio químico se estabelece
CH3NH2(aq) + H2O(l) ⇆ CH3NH3+ (aq) + OH–(aq)
Sabe-se que o valor da constante de ionização da metilamina (Kb) é igual a 3,6 x 10-4 e que seu grau de ionização é inferior a 5%. Assim, uma solução aquosa de metilamina que seja comercializada com concentração 0,10mol.L-1 deve apresentar pH igual a
(Dados: log 2 = 0,30 e log 3 = 0,50)
CH3NH2(aq) + H2O(l) ⇆ CH3NH3+ (aq) + OH–(aq)
Sabe-se que o valor da constante de ionização da metilamina (Kb) é igual a 3,6 x 10-4 e que seu grau de ionização é inferior a 5%. Assim, uma solução aquosa de metilamina que seja comercializada com concentração 0,10mol.L-1 deve apresentar pH igual a
(Dados: log 2 = 0,30 e log 3 = 0,50)
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O zinco é um elemento químico necessário ao organismo humano
em pequenas quantidades. No entanto, sua ingestão excessiva,
por água ou outros alimentos/suplementos, pode causar graves
distúrbios.
A resolução 420/2009 do CONAMA estipula que o limite de zinco
para águas subterrâneas seja de 1050ppb.
Considere que a análise de 2,5g de água de um poço artesiano
tenha revelado a presença de 5,5 microgramas de zinco. O teor de zinco nessa água é, de forma aproximada, equivalente
Provas
Questão presente nas seguintes provas
A Tabela Periódica é um dos mais importantes instrumentos da
Química. Nela os elementos estão dispostos em grupos de acordo
com suas principais características. Considere as informações a
seguir, relativas a um determinado grupo de elementos da Tabela
Periódica.
I. possuem baixos ponto de fusão, ponto de ebulição e densidade. II. reagem violentamente com água, gerando como produtos uma base e gás hidrogênio. III. perdem elétrons com facilidade, tendendo a formar íons monovalentes.
Possuem essas características os elementos químicos pertencentes ao grupo
I. possuem baixos ponto de fusão, ponto de ebulição e densidade. II. reagem violentamente com água, gerando como produtos uma base e gás hidrogênio. III. perdem elétrons com facilidade, tendendo a formar íons monovalentes.
Possuem essas características os elementos químicos pertencentes ao grupo
Provas
Questão presente nas seguintes provas
Uma amostra inicial de 110,4 g contém uma mistura de KClO3,
KHCO3 e K2CO3. De modo a determinar sua composição
centesimal, tal amostra foi aquecida até a decomposição
completa, originando as seguintes transformações.
• 2KClO3 (s) → 2 KCl (s) + 3 O2 (g) • 2 KHCO3 (s) → K2O (s) + H2O (g) + 2 CO2 (g) • K2CO3 (s) → K2O (s) + CO2 (g)
Nas condições reacionais empregadas, o rendimento foi de 100% e produziu 1,80 g de água, 19,2 g de gás oxigênio e 22,0 g de gás carbônico.
Os percentuais aproximados de KClO3, KHCO3 e K2CO3 na amostra inicial são, respectivamente, iguais a
• 2KClO3 (s) → 2 KCl (s) + 3 O2 (g) • 2 KHCO3 (s) → K2O (s) + H2O (g) + 2 CO2 (g) • K2CO3 (s) → K2O (s) + CO2 (g)
Nas condições reacionais empregadas, o rendimento foi de 100% e produziu 1,80 g de água, 19,2 g de gás oxigênio e 22,0 g de gás carbônico.
Os percentuais aproximados de KClO3, KHCO3 e K2CO3 na amostra inicial são, respectivamente, iguais a
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Iônico: Conceitos, Diluição de Ostwald, Efeito do Íon Comum
A força de um ácido está diretamente ligada a sua capacidade de
sofrer ionização. Essa força pode ser determinada
experimentalmente e expressa a partir do valor da constante de
ionização ácida (Ka).
Observe a tabela a seguir que contém os valores de pKa para cinco ácidos inorgânicos distintos.
ÁCIDO pKa carbônico 6,37 hipocloroso 7,53 hipobromoso 8,69 bórico 9,14 cianídrico 9,31
O ácido mais forte é o
Observe a tabela a seguir que contém os valores de pKa para cinco ácidos inorgânicos distintos.
ÁCIDO pKa carbônico 6,37 hipocloroso 7,53 hipobromoso 8,69 bórico 9,14 cianídrico 9,31
O ácido mais forte é o
Provas
Questão presente nas seguintes provas
Quando uma ligação química se forma, os átomos rearrumam
seus elétrons de modo a atingirem a configuração eletrônica de
um gás nobre. A esse princípio, o químico norte-americano G. N.
Lewis deu o nome de Regra do Octeto. No entanto, hoje sabemos
que diversos compostos não obedecem a esse princípio.
Um exemplo de composto que viola esse princípio é o
Provas
Questão presente nas seguintes provas
Um experimento de cinética química bastante conhecido é
chamado de “reação relógio”. Nele, os íons persulfato reagem
com íons iodeto conforme a reação balanceada a seguir.
S2O8 2 – (aq) + 3 I – (aq) → 2 SO4 2 – (aq) + I3 – (aq)
A tabela a seguir contém dados experimentais sobre a reação em condições específicas de temperatura e pressão.
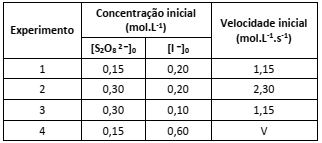
A partir das informações apresentadas é possível prever que a velocidade (V) do Experimento 4 será
S2O8 2 – (aq) + 3 I – (aq) → 2 SO4 2 – (aq) + I3 – (aq)
A tabela a seguir contém dados experimentais sobre a reação em condições específicas de temperatura e pressão.

A partir das informações apresentadas é possível prever que a velocidade (V) do Experimento 4 será
Provas
Questão presente nas seguintes provas
Desde o início do século XX ficou claro que a mecânica clássica
não seria capaz de explicar a estrutura interna dos átomos. Novas
leis precisaram ser desenvolvidas e ficaram conhecidas como
mecânica quântica.
A partir dessas novas leis foi possível determinar a(o)
A partir dessas novas leis foi possível determinar a(o)
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container