Foram encontradas 40 questões.
Considere que o estudo cinético da reação entre X(g) e Y(g) foi realizado em um sistema fechado, mantendo-se constante os valores de volume e temperatura. Os resultados obtidos no experimento estão representados na tabela a seguir:
| [X] (mol L–1) | [Y] (mol L–1) | Velocidade (mol L–1 h–1) |
| 1 x 10–3 | 1 x 10–3 | 5 x 10–5 |
| 1 x 10–3 | 2 x 10–3 | 10 x 10–5 |
| 2 x 10–3 | 2 x 10–3 | 40 x 10–5 |
A partir dos resultados obtidos, assinale, a seguir, a Lei da Velocidade (v) para a reação X(g) + Y(g) !$ \rightarrow !$ XY(g).
Provas
Considere os grupos substituintes derivados de hidrocarbonetos:
| I. | 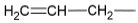 | II. | 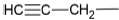 |
| II. | 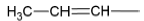 | IV. | 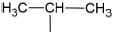 |
Assinale, a seguir, o número que representa o grupo univalente alil(a).
Provas
Considere as substâncias químicas e suas respectivas ocorrências no cotidiano:
I. Ácido acético: principal componente do vinagre.
II. Salicilato de metila (éster metílico do ácido salicílico): ações analgésica e anti-inflamatória.
III. Glicerina: propriedades emolientes, lubrificantes e umectantes.
IV. Álcool etílico: prevenção do contágio com o Coronavírus, combustível em automóveis e limpeza doméstica.
Assinale a associação correta das substâncias químicas e as suas fórmulas estruturais.
Provas
Em função da isomeria geométrica, os ácidos maleico e fumárico apresentam propriedades químicas distintas. Enquanto a molécula do ácido maleico sofre reação de desidratação e produz o anidrido maleico, a molécula do ácido fumárico não é capaz de realizar desidratação intramolecular nas mesmas condições. Sendo assim, o reconhecimento de isomeria geométrica em compostos orgânicos é de grande relevância na área de síntese orgânica para o desenvolvimento de novos produtos. Assinale, a seguir, o composto que NÃO apresenta isomeria geométrica:
Provas
Em determinados sistemas, o aumento da temperatura promove o aumento na velocidade das reações químicas pela alteração de alguns fatores. São considerados fatores que podem ser alterados pelo aumento da temperatura, EXCETO:
Provas
Observe as equações químicas a seguir:
I. CaO + H2O !$ \rightarrow !$ Ca(OH)2
II. SO2 + H2O !$ \rightarrow !$ H2SO3
III. Rb2O + 2HCl !$ \rightarrow !$ 2RbCl + H2O
IV. CO2 + 2NaOH !$ \rightarrow !$ Na2CO3 + H2O
Assinale a afirmativa INCORRETA.
Provas
Considere a equação química a seguir:
!$ a\,Pb(NO_3)_{2(aq)} +b Kl_{(aq)} \rightarrow Pbl_{2(s)}+ d KNO_{3(aq)} !$
É correto afirmar que:
Provas
A existência de compostos é o ponto central da ciência da química e, ao perceber como as ligações se formam, podemos compreender como os químicos projetam novos materiais. Pesquisas envolvendo sangue artificial, novos fármacos, produtos químicos para a agricultura e os polímeros utilizados para fazer artefatos, como discos compactos, telefones celulares e fibras sintéticas, se baseiam na percepção de como os átomos se ligam. Sobre as ligações químicas, analise as afirmativas a seguir.
I. Os sólidos iônicos são frágeis porque as atrações e repulsões são fortes.
II. Os raios covalentes devem ser somados, quando se deseja estimar os comprimentos de ligação em moléculas.
III. A ligação química dos compostos formados por cátions e ânions muito polarizáveis tem forte caráter covalente.
Está correto o que se afirma em
Provas
A oxirredução está presente em diversos processos de interesse para a indústria e a sociedade. As pilhas e as baterias, tão utilizadas em dispositivos eletrônicos, geram energia elétrica por meio do processo de oxirredução. Muitos metais são obtidos na forma pura por meio de reações de oxirredução. A oxirredução também tem grande importância na bioquímica, sendo empregada para explicar, inclusive, o envelhecimento do ser humano. Em relação às reações de oxirredução, marque V para as afirmativas verdadeiras e F para as falsas.
( ) O magnésio metálico reage com ácido clorídrico para formar cloreto de magnésio e gás hidrogênio.
( ) As reações de combustão são consideradas reações redox, porque o oxigênio elementar é convertido em compostos de oxigênio.
( ) Uma solução de cloreto de ferro (II) não oxida o magnésio metálico.
( ) A soma dos coeficientes estequiométricos da reação entre alumínio com ácido bromídrico é 10.
A sequência está correta em
Provas
A eletroquímica é o estudo da interação entre a eletricidade e as reações químicas. A transferência de elétrons de uma espécie para outra é um dos processos fundamentais que permitem a vida, a fotossíntese, as células a combustível e a purificação de metais. Compreender como os elétrons são transferidos nos permite determinar modos de usar as reações químicas para gerar eletricidade e usá-la para produzir reações químicas. Sobre as pilhas, é INCORRETO afirmar que:
Provas
Caderno Container