Foram encontradas 40 questões.
A situação hipotética contextualiza a questão. Leia-a atentamente.
Determinado grupo de pesquisa desenvolveu um novo composto antineoplásico, codificado como XY-100. A síntese do fármaco
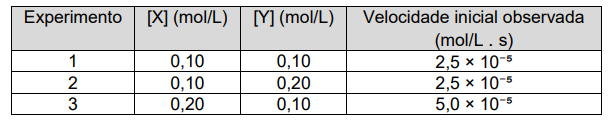
ocorre a partir dos reagentes X e Y, por meio de uma reação cujo comportamento cinético foi estudado e apresentado na tabela:
Dados de concentrações e velocidades iniciais coletadas para a síntese de XY-100:
Provas
Questão presente nas seguintes provas
A situação hipotética contextualiza a questão. Leia-a atentamente.
Determinado grupo de pesquisa desenvolveu um novo composto antineoplásico, codificado como XY-100. A síntese do fármaco
ocorre a partir dos reagentes X e Y, por meio de uma reação cujo comportamento cinético foi estudado e apresentado na tabela:
Dados de concentrações e velocidades iniciais coletadas para a síntese de XY-100:

Provas
Questão presente nas seguintes provas
A situação hipotética contextualiza a questão. Leia-a atentamente.
Determinado grupo de pesquisa desenvolveu um novo composto antineoplásico, codificado como XY-100. A síntese do fármaco
ocorre a partir dos reagentes X e Y, por meio de uma reação cujo comportamento cinético foi estudado e apresentado na tabela:
Dados de concentrações e velocidades iniciais coletadas para a síntese de XY-100:

Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Após preparar uma solução saturada de Mg(OH)2 e permitir que o equilíbrio químico fosse alcançado, o professor de química
mediu o pH da solução e registrou um valor de 9. Tendo em vista que toda a concentração de íons magnésio resulta
exclusivamente da dissociação da base, assinale, a seguir, a concentração aproximada de Mg2+ na solução.
Provas
Questão presente nas seguintes provas
Considere que o professor de química preparou uma solução tampão de acetato de sódio e ácido acético para uma aula sobre
equilíbrio químico ácido-base. Sabe-se que o pKa do ácido acético é 4,8 (Ka = 1,7 x 10-5) e que as concentrações usadas do sal
e do ácido foram de 3,0 mol/L e 0,3 mol/L, respectivamente. É correto afirmar o pH da solução preparada pelo professor é
de, aproximadamente:
Provas
Questão presente nas seguintes provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química CinéticaTransformações Químicas
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
A classificação periódica é uma forma de organização dos elementos químicos de modo a evidenciar algumas semelhanças em
suas propriedades físicas ou químicas. Vários estudiosos tentaram criar um sistema de classificação dos elementos. Os critérios
utilizados para a organização dos elementos foram estabelecidos ao longo do tempo. Sobre a tabela periódica, é INCORRETO
afirmar que:
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
No laboratório de química, o professor fez uma prática com os alunos. O objetivo da experiência era testar a condutividade
elétrica de diferentes compostos. No primeiro momento, colocou sobre a bancada sete recipientes identificados. Eram diferentes soluções que seriam analisadas. O professor pediu que, antes do teste de condutividade elétrica dos compostos, os
alunos prevessem quais soluções iriam acender a lâmpada e quais dos compostos não iriam acender. E dos que acendesse a
lâmpada, qual acenderia com maior intensidade.

De acordo com a resposta dos estudantes, analise as afirmativas a seguir.
I. Dentre as soluções dos três ácidos analisados, o ácido sulfúrico acende a lâmpada com maior intensidade.
II. Somente as soluções de sacarose e naftaleno não acendem a lâmpada.
III.Somente as soluções de sulfato de cálcio, etanol, ácido sulfúrico, ácido sulfídrico e ácido hipocloroso acendem a lâmpada.
Está correto o que se afirma em

De acordo com a resposta dos estudantes, analise as afirmativas a seguir.
I. Dentre as soluções dos três ácidos analisados, o ácido sulfúrico acende a lâmpada com maior intensidade.
II. Somente as soluções de sacarose e naftaleno não acendem a lâmpada.
III.Somente as soluções de sulfato de cálcio, etanol, ácido sulfúrico, ácido sulfídrico e ácido hipocloroso acendem a lâmpada.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
- Química CinéticaVelocidade de Reação, Energia de Ativação e Catalisadores
- Química OrgânicaGlicídios, Lipídios, Aminoácidos e Proteínas.
O colesterol é um composto normalmente produzido no fígado e que tem um papel importante em vários aspectos do
metabolismo dos organismos animais, sendo precursor de vários hormônios. Faz parte da produção de hormônios, vitamina
D e ácidos biliares que atuam na digestão e na absorção das gorduras no intestino. Porém, em taxas elevadas, o colesterol
aumenta o risco de complicações como diabetes e doenças cardiovasculares como infarto e derrame:
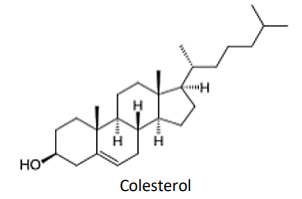
Quantos gramas de água são produzidos na oxidação de 6 g de colesterol?

Quantos gramas de água são produzidos na oxidação de 6 g de colesterol?
Provas
Questão presente nas seguintes provas
Em sua aula de química, o professor almejou aplicar um desafio para os estudantes. Pediu para que os alunos se reunissem
em quatro grupos e, para cada grupo, entregou a folha com o desafio descrito:
Desafio:
Com a fórmula C5H8 podem ser formados quantos alquinos? E com a fórmula C3H7NO podem ser formadas quantas amidas?
Após o professor marcar um tempo para que os estudantes pudessem responder o desafio, ele recolheu as respostas. Como teria dois tempos na turma, resolveu comentar as respostas dadas pelos grupos:

Qual dos grupos acertou o desafio proposto pelo professor?
Desafio:
Com a fórmula C5H8 podem ser formados quantos alquinos? E com a fórmula C3H7NO podem ser formadas quantas amidas?
Após o professor marcar um tempo para que os estudantes pudessem responder o desafio, ele recolheu as respostas. Como teria dois tempos na turma, resolveu comentar as respostas dadas pelos grupos:

Qual dos grupos acertou o desafio proposto pelo professor?
Provas
Questão presente nas seguintes provas
Em sua aula de química, o professor explicava para os estudantes sobre as propriedades dos compostos orgânicos. Ao terminar a explicação, ele passou na lousa uma atividade. Uma aluna conseguiu desenvolver rapidamente o exercício e pediu para
o professor se ela podia responder o que tinha feito. O professor, então, pediu para ela descrever na lousa suas respostas.
Ao escrever na lousa suas respostas, o professor percebeu que ela cometeu erro(s).
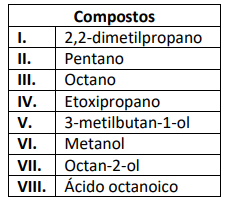
1.Dentre os pares de compostos listados a seguir, indique qual deve apresentar maior temperatura de ebulição:
a) I e II.
b) IV e V.
c) III e VI.
2.Dentre os pares de compostos listados a seguir, indique qual deve ser mais solúvel em água:
a) VI e VII.
b) VII e VIII.
c) I e IV.
Resposta da aluna:
1.
a) I.
b) V.
c) VI.
2.
a) VI.
b) VIII.
c) IV.
Quantos erros a estudante cometeu?

1.Dentre os pares de compostos listados a seguir, indique qual deve apresentar maior temperatura de ebulição:
a) I e II.
b) IV e V.
c) III e VI.
2.Dentre os pares de compostos listados a seguir, indique qual deve ser mais solúvel em água:
a) VI e VII.
b) VII e VIII.
c) I e IV.
Resposta da aluna:
1.
a) I.
b) V.
c) VI.
2.
a) VI.
b) VIII.
c) IV.
Quantos erros a estudante cometeu?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container