Foram encontradas 632 questões.
Mário Beni é um renomado especialista em turismo que contribuiu significativamente para a compreensão dos sistemas
turísticos. Em suas teorias, ele aborda o conceito de “sistemas de turismo” e como esses sistemas interagem e se organizam
para proporcionar experiências turísticas. Segundo Beni, um sistema de turismo é composto por vários elementos que interagem e se influenciam mutuamente, formando um todo integrado. Assinale a afirmativa correta considerando as teorias de
Mário Beni sobre sistemas de turismo.
Provas
Questão presente nas seguintes provas
Para muitas pessoas, a palavra sal está associada apenas ao “sal de cozinha” e, por isso, que relacionam o sal com à cor
branca. No entanto, os sais podem ser encontrados em diferentes cores e apresentam muitas funções. Sobre esses compostos, analise as afirmativas a seguir.
I. É muito utilizado na fabricação de fertilizantes (adubos) e conhecido como salitre do Chile.
II. Comumente utilizado no tratamento de água de piscina, na fabricação de sabões, remédios, corantes, entre outros. É conhecido como soda ou barrilha.
As alternativas I e II descrevem os seguintes tipos de sais, respectivamente:
I. É muito utilizado na fabricação de fertilizantes (adubos) e conhecido como salitre do Chile.
II. Comumente utilizado no tratamento de água de piscina, na fabricação de sabões, remédios, corantes, entre outros. É conhecido como soda ou barrilha.
As alternativas I e II descrevem os seguintes tipos de sais, respectivamente:
Provas
Questão presente nas seguintes provas
Muitos ácidos são utilizados nas indústrias, em geral, vendidos no comércio e formados naturalmente no meio ambiente.
Existe um tipo que, em condições ambientais, é incolor, e se caracteriza por corroer vidros, quando está em solução aquosa.
É muito utilizado na indústria para gravações em vidros dos carros. Esse ácido é conhecido por:
Provas
Questão presente nas seguintes provas
Uma célula eletroquímica é um dispositivo que utiliza reações de óxido-redução para produzir a interconversão de energia
química e elétrica. Existem dois tipos de células eletroquímicas: as células galvânicas, nas quais energia química é convertida
em energia elétrica, e as células eletrolíticas, nas quais energia elétrica é convertida em energia química. Considere uma
célula eletroquímica baseada na seguinte reação:
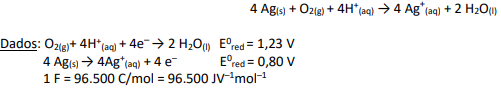
O valor da variação de energia livre, ∆G0 e a espontaneidade da reação é:
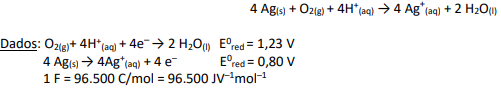
O valor da variação de energia livre, ∆G0 e a espontaneidade da reação é:
Provas
Questão presente nas seguintes provas
Em um laboratório foram feitas cinco experiências para a reação do brometo de t-butila (CH3)3CBr com o íon hidróxido, a
55ºC. Os dados das cinco experiências foram coletados. De acordo com as experiências 1, 2 e 3, em cada uma delas a
concentração de OH– é a mesma e a concentração de (CH3)3CBr é variada. Quando a concentração de (CH3)3CBr é dobrada, a
velocidade dobra e quando a concentração de (CH3)3CBr é triplicada, a velocidade triplica. Nas experiências 1, 4 e 5, a
concentração de (CH3)3CBr é a mesma e a variação da concentração de OH– não provoca nenhum efeito sobre a velocidade.
(CH3)3CBr + OH– → (CH3)3COH + Br–
Considerando os dados apresentados, a lei de velocidade para a reação é:
(CH3)3CBr + OH– → (CH3)3COH + Br–
Considerando os dados apresentados, a lei de velocidade para a reação é:
Provas
Questão presente nas seguintes provas
A área da química, que está preocupada com as velocidades ou grau de velocidade das reações, é chamada cinética química.
A cinética química se relaciona, por exemplo, com a rapidez com que um medicamento é capaz de agir, com o fato de a
formação e a depreciação do ozônio na atmosfera superior estarem em equilíbrio, bem como os problemas industriais, como
o desenvolvimento de catalisadores para a síntese de novos materiais. Sobre a velocidade que as reações químicas são feitas,
analise as afirmativas a seguir.
I. A velocidade de uma reação depende da concentração, mas a constante de velocidade não depende dela.
II. Quanto mais baixa for a energia de ativação, mais lenta a reação.
III. Se a velocidade de aparecimento de O2(g), 2 O3(g) → 3 O2(g), é 9 x 10–4 mol/L em determinado instante, a velocidade de desaparecimento do O3(g) é 18 x 10–4 mol/L.
Está correto o que se afirma em
I. A velocidade de uma reação depende da concentração, mas a constante de velocidade não depende dela.
II. Quanto mais baixa for a energia de ativação, mais lenta a reação.
III. Se a velocidade de aparecimento de O2(g), 2 O3(g) → 3 O2(g), é 9 x 10–4 mol/L em determinado instante, a velocidade de desaparecimento do O3(g) é 18 x 10–4 mol/L.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
As reações de oxirredução estão entre as reações químicas mais comuns e importantes. Elas estão envolvidas em uma grande
variedade de processos importantes, incluindo a ferrugem do ferro, a fabricação e ação de alvejantes e a respiração dos
animais. A transferência de elétrons que ocorre durante as reações de oxirredução pode também ser usada para produzir
energia na forma de eletricidade. Em outras instâncias usamos a energia para fazer determinados processos não espontâneos
ocorrerem. Sobre as reações de oxirredução, analise as afirmativas a seguir.
I. Na reação química As2S3 + HNO3 + H2O → H3AsO4 + H2SO4 + NO, o nitrogênio sofre redução.
II. Na reação Cl2(g) + NaOH(aq) → NaCl(aq) + NaClO(aq) + H2O(l), o cloro sofre, ao mesmo tempo, oxidação e redução, tratando-se, nesse caso, de uma reação de auto-oxirredução.
III. Na equação química MnO4- + Fe2+(aq) + H+ (aq) → Mn2+(aq) + H2O + Fe3+(aq), a soma dos menores valores inteiros dos coeficientes estequiométricos é 24.
Está correto o que se afirma em
I. Na reação química As2S3 + HNO3 + H2O → H3AsO4 + H2SO4 + NO, o nitrogênio sofre redução.
II. Na reação Cl2(g) + NaOH(aq) → NaCl(aq) + NaClO(aq) + H2O(l), o cloro sofre, ao mesmo tempo, oxidação e redução, tratando-se, nesse caso, de uma reação de auto-oxirredução.
III. Na equação química MnO4- + Fe2+(aq) + H+ (aq) → Mn2+(aq) + H2O + Fe3+(aq), a soma dos menores valores inteiros dos coeficientes estequiométricos é 24.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
A célula eletrolítica é a célula eletroquímica na qual ocorre a eletrólise. O arranjo dos componentes das células eletrolíticas
é diferente do arranjo da célula galvânica. Em geral, os dois eletrodos ficam no mesmo compartimento, só existe um tipo de
eletrólito e as concentrações e pressões estão longe das condições-padrão. Em princípio, qualquer pilha (célula) pode ser
convertida em célula eletrolítica aplicando-se uma tensão externa oponente superior à tensão produzida pela pilha. Sobre
eletrólise, analise as afirmativas a seguir.
I. Na eletrólise do sulfato de sódio, a água é mais facilmente oxidada no ânodo do que o SO4- e no catodo as moléculas de água são reduzidas mais facilmente que os íons sódio.
II. Na eletrólise do cloreto de sódio fundido, pode-se obter Cl2(g) no ânodo.
III. Na eletrólise de uma solução aquosa de NaF, o F– será reduzido.
Está correto o que se afirma em
I. Na eletrólise do sulfato de sódio, a água é mais facilmente oxidada no ânodo do que o SO4- e no catodo as moléculas de água são reduzidas mais facilmente que os íons sódio.
II. Na eletrólise do cloreto de sódio fundido, pode-se obter Cl2(g) no ânodo.
III. Na eletrólise de uma solução aquosa de NaF, o F– será reduzido.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
O ferro é, em geral, coberto com um revestimento de pintura ou outro metal, como estanho ou zinco, para proteger sua
superfície contra corrosão. Cobrir a superfície com pintura ou estanho é uma maneira simples de prevenir o oxigênio e a
água de atingir a superfície do ferro. Se o revestimento é quebrado e o ferro é exposto ao oxigênio e à água, a corrosão
começará. O ferro galvanizado, que é o ferro revestido como uma fina camada de zinco, usa o princípio da eletroquímica
para proteger o ferro da corrosão. Os potenciais-padrão de redução para o ferro e o zinco são:
Fe2+(aq) + 2 e– → Fe(s) Eº = – 0,44 V
Zn2+(aq) + 2 e– → Zn(s) Eº = – 0,76 V
Com base nos dados de potencial-padrão de redução das semirreações, marque V para as afirmativas verdadeiras e F para as falsas.
( ) O zinco é mais facilmente oxidado e serve como ânodo.
( ) O ferro funciona como cátodo.
( ) O potencial desta pilha é 1,2 V.
( ) O ∆Eº < 0 caracteriza o funcionamento espontâneo da pilha.
A sequência está correta em
Fe2+(aq) + 2 e– → Fe(s) Eº = – 0,44 V
Zn2+(aq) + 2 e– → Zn(s) Eº = – 0,76 V
Com base nos dados de potencial-padrão de redução das semirreações, marque V para as afirmativas verdadeiras e F para as falsas.
( ) O zinco é mais facilmente oxidado e serve como ânodo.
( ) O ferro funciona como cátodo.
( ) O potencial desta pilha é 1,2 V.
( ) O ∆Eº < 0 caracteriza o funcionamento espontâneo da pilha.
A sequência está correta em
Provas
Questão presente nas seguintes provas
Um catalisador é uma substância que aumenta a velocidade de uma reação química sem ser consumida durante a reação.
Os catalisadores biológicos aumentam a rapidez das reações bioquímicas. Um exemplo de catalisador biológico são as
enzimas: proteínas que participam de processos biológicos aumentam a rapidez das reações e não são consumidas durante
o processo. A ptialina ou amilase salivar, por exemplo, é uma enzima presente na saliva que aumenta a rapidez de quebra
do amido presente nos alimentos em moléculas menores. A função de um catalisador a um sistema químico em equilíbrio é
aumentar:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container