Foram encontradas 632 questões.
As velocidades das reações químicas podem ser extremamente lentas ou extremamente rápidas. O estudo dos fatores que
influenciam as velocidades das reações tem aplicações práticas óbvias. Além disso, esse estudo fornece informações valiosas
de como as reações químicas ocorrem na realidade:

De acordo com o gráfico, analise as afirmativas a seguir.
I. Existe um intermediário B na reação A → C.
II. A reação total é exotérmica.
III. A etapa B → C é mais rápida.
Está correto o que se afirma em

De acordo com o gráfico, analise as afirmativas a seguir.
I. Existe um intermediário B na reação A → C.
II. A reação total é exotérmica.
III. A etapa B → C é mais rápida.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
A química é, por sua própria natureza, preocupada com a mudança. As reações químicas convertem substâncias com propriedades bem definidas em outros materiais com propriedades diferentes. Muitos estudos sobre reações químicas dizem respeito
à formação de novas substâncias a partir de determinado conjunto de reagentes. Entretanto, é igualmente importante entender
com que rapidez as reações ocorrem. As velocidades de reações se estendem sobre uma faixa enorme, a partir das que se
completam em frações de segundos, como explosões, aquelas que levam milhares ou até milhões de anos, como a formação dos
diamantes e outros minerais na crosta terrestre. Sobre o mecanismo de reação de duas etapas são feitas as seguintes afirmativas:
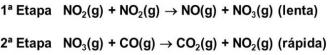
I. O intermediário NO3(g) é produzido lentamente na etapa 1 e é imediatamente consumido na etapa 2.
II. A lei de velocidade da reação é V = K [NO2]2 .
III. A etapa 2 é muito mais rápida que a etapa 1, isto é K2>>K 1.
Está correto o que se afirma em
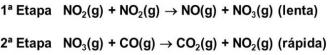
I. O intermediário NO3(g) é produzido lentamente na etapa 1 e é imediatamente consumido na etapa 2.
II. A lei de velocidade da reação é V = K [NO2]2 .
III. A etapa 2 é muito mais rápida que a etapa 1, isto é K2>>K 1.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Iônico: Conceitos, Diluição de Ostwald, Efeito do Íon Comum
O processo de Fritz tornou-se a principal fonte mundial de nitrogênio fixado. Tal processo permitiu aos cientistas sintetizar
fertilizantes que aumentaram a produção de grãos, salvando em consequência milhões de pessoas da inanição. Haber
desenvolveu um processo para sintetizar amônia diretamente a partir de nitrogênio e hidrogênio. 886 K, a constante de
equilíbrio para a reação N2(g) + 3 H2(g) ⇌ 2NH3(g) é 0,226. Como a reação prosseguirá em direção ao equilíbrio, se as pressões
parciais forem PN2 = 0,52 atm; PH2 = 0,27 atm; e, PNH3 = 0,84 atm?
Provas
Questão presente nas seguintes provas
No desenvolvimento de seu processo para produzir amônia, a partir de N2 e H2, Haber buscou os fatores que poderiam ser
variados para aumentar o rendimento de NH3. Usando os valores da constante de equilíbrio a várias temperaturas, ele calculou as quantidades de NH3 formadas no equilíbrio sob várias condições. Observou que a porcentagem de NH3 presente no
equilíbrio diminui com o aumento da temperatura e aumenta com o aumento da pressão. Esses efeitos podem ser entendidos em termos de um princípio apresentado por um químico industrial francês – Henri-Louis Le Châtelier. Sobre o princípio
de Le Châtelier, marque V para as afirmativas verdadeiras e F para as afirmativas falsas.
( ) Para a reação PCl5(g) ⇌ PCl3(g) + Cl2(g) ∆H0= 87,9 kJ, o equilíbrio se deslocará para direita quando a temperatura for diminuída.
( ) Para a reação N2O4(g) ⇌ 2NO2(g), o equilíbrio se deslocará para direita com o aumento da pressão total pela adição de N2(g).
( ) A remoção de H2O, 4 NH3(g) + 3O2(g) ⇌ 2 N2(g) + 6H2O(g), reduz Q abaixo de K, com formação de produtos à custa dos reagentes.
( ) Na reação 2 SO2(g) + O2(g) ⇌ 2 SO3(g), o equilíbrio se desloca no sentido de formação do produto, com o aumento da concentração de SO2(g).
A sequência está correta em
( ) Para a reação PCl5(g) ⇌ PCl3(g) + Cl2(g) ∆H0= 87,9 kJ, o equilíbrio se deslocará para direita quando a temperatura for diminuída.
( ) Para a reação N2O4(g) ⇌ 2NO2(g), o equilíbrio se deslocará para direita com o aumento da pressão total pela adição de N2(g).
( ) A remoção de H2O, 4 NH3(g) + 3O2(g) ⇌ 2 N2(g) + 6H2O(g), reduz Q abaixo de K, com formação de produtos à custa dos reagentes.
( ) Na reação 2 SO2(g) + O2(g) ⇌ 2 SO3(g), o equilíbrio se desloca no sentido de formação do produto, com o aumento da concentração de SO2(g).
A sequência está correta em
Provas
Questão presente nas seguintes provas
A expectativa da eclosão da Primeira Guerra Mundial gerou uma desesperada busca por compostos de nitrogênio, visto que os
nitratos, normalmente usados na agricultura, estavam sendo usados na fabricação de explosivos. Os cientistas de ambos os lados
do conflito estavam tentando insistentemente encontrar maneiras de fixar o nitrogênio. O químico alemão Fritz Haber encontrou
uma forma econômica de utilizar o nitrogênio do ar e prover, desse modo, uma fonte abundante de compostos para a agricultura
e para os armamentos. Uma dificuldade que Haber se deparou foi que as reações empregadas para produzir compostos a partir
de nitrogênio não vão até o fim e parecem parar após consumir uma certa quantidade de reagentes. Neste ponto, a mistura
atinge o equilíbrio químico. Para conseguir a máxima conversão de nitrogênio em seus compostos, Haber deveria compreender
como uma reação se aproxima do equilíbrio para, então, alcança-lo. Sobre equilíbrio químico, é INCORRETO afirmar que:
Provas
Questão presente nas seguintes provas
Em um laboratório de química orgânica, um químico conduziu uma reação de bromação com uma molécula de propeno,
utilizando bromo molecular (Br₂) em um solvente inerte. Ao final do experimento, o profissional observa a formação de um
único produto majoritário, que é caracterizado como 1,2-dibromopropano. Esse tipo de reação química é classificada como:
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Foram preparadas seis soluções aquosas de um sal específico, identificadas de I a VI, em diferentes temperaturas, com
distintas quantidades de sal dissolvidas em 100 g de água. Em alguns casos, o sal não se dissolveu por completo, deixando
um corpo de fundo. O gráfico a seguir exibe a curva de solubilidade do sal em função da temperatura. Os seis pontos
correspondem aos sistemas preparados:
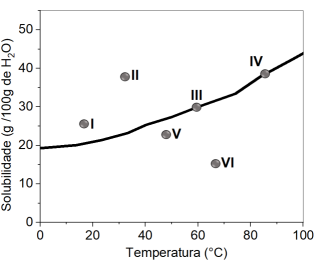
A partir da análise do perfil de solubilidade do sal, é correto afirmar que ocorre a formação de precipitado apenas nos seguintes sistemas:

A partir da análise do perfil de solubilidade do sal, é correto afirmar que ocorre a formação de precipitado apenas nos seguintes sistemas:
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um químico sintetizou uma substância com atividade terapêutica e investigou sua solubilidade. A seguir, é exibida a curva
de solubilidade do fármaco, indicando a quantidade de princípio ativo dissolvida em 100 g de água em diferentes temperaturas:
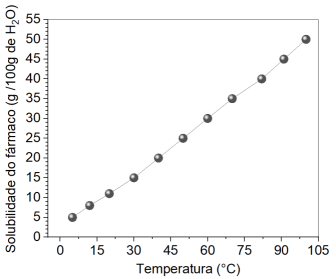
Se o químico optar por trabalhar com 40 g de água a 60°C, a quantidade máxima da substância que será dissolvida é:

Se o químico optar por trabalhar com 40 g de água a 60°C, a quantidade máxima da substância que será dissolvida é:
Provas
Questão presente nas seguintes provas
No Brasil, a concentração máxima permitida de cloro residual livre na água potável é de 5 mg por litro de água. Ao expressar
essa concentração em ppm, o valor a ser obtido é:
Provas
Questão presente nas seguintes provas
No laboratório de pesquisa, um aluno de iniciação científica investiga a reação entre magnésio metálico e oxigênio gasoso
para formar óxido de magnésio. Durante o experimento, ele pesa cuidadosamente uma fita de magnésio, queima-a em
atmosfera de oxigênio puro e, após a reação, determina a massa do óxido de magnésio formado. Se 3 mols de magnésio
metálico reagem com oxigênio e formam 120,0 g de óxido de magnésio, o número de mols de oxigênio que reagiram é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container