Foram encontradas 50 questões.
A viscosidade de um líquido é a resistência ao escoamento sendo uma indicação da intensidade das forças atrativas entre as moléculas. Interações intermoleculares fortes proporcionam maior resistência ao escoamento.
Considerando as substâncias: glicerol (propano-1,2,3-triol), água, tetracloreto de carbono, benzeno e éter dietílico, assinale a opção que indica a que possui maior viscosidade.
Provas
A água pura é um mau condutor de eletricidade porque consiste em moléculas eletricamente neutras que não são capazes de transportar cargas elétricas. Contudo a dissolução de determinadas substâncias denominadas eletrólitos produzem soluções condutoras de eletricidade devido à presença de partículas eletricamente carregadas.
Os eletrólitos podem ser classificados em fortes ou fracos dependendo da porcentagem de partículas eletricamente carregadas que se encontram em solução.
Assinale a opção que indica a substância considerada um eletrólito fraco.
Provas
Na reação de oxidação de um determinado álcool fi utilizados 100 mL de uma solução aquosa de permanganat potássio de concentração 30% em massa e densidade 1,10g.mL-1. O número de mols de permanganato de potássio utilizado reação foi, aproximadamente, de
Dados: Massa molar: O = 16g.mol-1 K=39g.mol-1 Mn = 55g.mol-1
Provas
Em um béquer de 250 mL foi colocada uma determinada massa de ácido oxálico anidro (C2H2O4), previamente pesada. O ácido em questão foi dissolvido em 100 mL de água destilada e, com auxilio de um funil simples, essa solução foi transferida quantitativamente para um balão volumétrico de 250,00 mL.
O volume da solução foi completado com água destilada até a marca da aferição do balão que, posteriormente, foi tampado e agitado para completa homogeneização. Com esse procedimento foi preparada uma solução de ácido oxálico de concentração 0,20 mol.L-1.
A massa, em gramas, de ácido oxálico utilizada nessa solução foi de Dados: Massa molar: H = 1g.mol-1 C = 12g.mol-1 O= 16g.mol-1
Provas
Para limpeza de resinas de biocromatografia é utilizado etanol 70% nem sempre disponível no almoxarifado. A partir do etanol 96°GL pode-se, por diluição, preparar a solução desejada.
Assinale a opção que indica o volume de etanol 96°GL necessário para o preparo de 1 litro de etanol 70%.
Provas
Segundo o conceito de Brönsted, ácidos fortes como HNO3 e HCℓO4 reagem completamente com a água produzindo íons H3O+, enquanto as reações de ácidos como HNO₂ e CH3CO₂H com a água, ocorrem com pouca formação de íons H3O+.
Os ácidos fracos citados são, respectivamente, denominados
Provas
O hidróxido de ouro (Ill) é utilizado na eletrodeposição de ouro sobre outros metais podendo ser obtido pela reação:
2KAuC!$ \ell !$a (aq) + 3Na2CO3(aq) + 3 H2O,) →
2Au(OH)3(aq) + 6NaC!$ \ell !$(ag) + 2 KC!$ \ell !$(aq) + 3 CO2(g).
No preparo de um suprimento de 62 gramas de Au(OH):, um químico de uma unidade de eletrodeposição industrial misturou os reagentes utilizando excesso de água. Considerando um rendimento de 100%, a massa de Na2CO3 necessária nesse processo é, aproximadamente, Dados: Massas molares: Na2CO3 =106g.mol-1 Au(OH)3 = 248g.mol-1
Provas
A testosterona é o principal hormônio sexual masculino e foi isolada pela primeira vez representada a seguir em 1935. Sua estrutura está representada a seguir
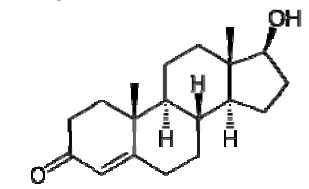
A massa molar, em g.mol-1, dessa substância é
Dados Massa molar do H = 1g.mol-¹ C= 12g.mol-¹ C= 16g.mol-¹
Provas
Os compostos químicos contendo mercúrio são classificados, do ponto de vista toxicológico, em dois grupos principais: compostos orgânicos e compostos inorgânicos, onde se inclui também o mercúrio atômico ou elementar. Sintomas e sinais clássicos, relacionados à ação tóxica no sistema nervoso central, estão normalmente associados à exposição ao mercúrio elementar.
O valor de referência para adultos e índices biológicos de exposição (ou índices biológicos máximos permitidos) para mercúrio excretado na urina é 5µg de Hg/gC (µg/g de creatinina urinária).
Esse valor de referência expresso em mol de Hg/g de creatinina urinária corresponde a:
Dados: Massa molar do Hg = 200g.mol–1 1 µg =10–6g
Provas
Um incêndio pode ser definido como a propagação do fogo capaz de provocar danos à integridade física dos indivíduos e do patrimônio. De acordo com a natureza do combustível, os incêndios enquadram-se em classes:
Classe A | Incêndios em sólidos como madeira, papel e tecidos. |
Classe B | Ocorre em líquidos e gases inflamáveis como gasolina e etano. |
Classe C | Incêndios em equipamentos e instalações elétricas energizadas. |
Classe D | Caracteriza-se por fogo em metais pirofóricos, como alumínio e magnésio. |
O agente extintor mais apropriado para cada tipo de incêndio depende do material que está em combustão. A esse respeito, analise as afirmativas a seguir.
l. O extintor de água pode ser utilizado em incêndios das classes A,B e D.
II. O extintor de espuma mecânica é indicado principalmente para a classe C.
III. O extintor de CO2 pode ser utilizado em incêndios das classes B e C.
IV. O extintor a base de sal de cloreto de sódio é o mais indicado em incêndios da classe D
Assinale:
Provas
Caderno Container