Foram encontradas 45 questões.
- Interações com Tecnologia, Sociedade e Meio Ambiente
- Sistemas de EquilíbrioSistemas Homogêneos: Constantes: Kc e Kp. Deslocamento do Equilíbrio: Fatores
Devido à grande emissão de gases lançados na atmosfera, nas regiões mais populosas é evidente a ocorrência da chuva ácida. Na sua precipitação, um dos ácidos responsáveis pela acidez é o sulfúrico. Um equilíbrio envolvido na formação desse ácido na água da chuva está representado pela equação:
2SO2(g) + O2(g) ⇌ 2SO3(g)
Considere que são colocados 6 mol de SO2, 5 mol de O2 e 4 mol de SO3 num recipiente fechado de 5,0 L para reagirem até o sistema atingir o equilíbrio a dada temperatura. A variação do número de mol dos gases participantes está registrada no gráfico.
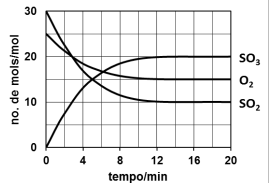
Nestas condições, a constante de equilíbrio, KC, é igual a:
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Transformações Químicas e EnergiaTermoquímica
Provas

Assinale a alternativa que correlaciona, corretamente, as colunas.
Provas
Existem muitos motivos para estudar a velocidade de uma reação, do ponto de vista prático, o conhecimento das velocidades de reações é útil na concepção de medicamentos, no controle da poluição e no processamento de alimentos, bem como nas aplicações de setores produtivos em geral. Então para exemplificar, considere que a velocidade de uma reação entre os compostos A e B segue a lei de velocidade, v = k [A] 2 [B] . Com base nos dados da tabela abaixo, determine a velocidade do Experimento 2 observada a mesma temperatura do Experimento 1.
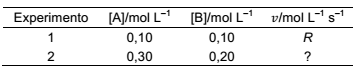
Provas
Responder numerando corretamente a questão da coluna da direita, que descreve a finalidade do uso de EPIs e outros cuidados pessoais que devem ser observados para proteção individual, de acordo com a coluna da esquerda, que apresenta a classificação dos mesmos:
1. Cabelos preferencialmente mantidos presos ou sob gorros
2. Guarda-pó
3. Luvas de procedimentos
4. Óculos
5. Restrições ao uso de joias ou similares
6. Sapatos fechados
( ) Evitar danos nos materiais nobres mediante processo oxidação
( ) Evitar o contato com material biológico ou químico durante a manipulação de materiais e uso de equipamentos
( ) Proteção dos olhos contra respingos e resíduos de vidros ou outros materiais
( ) Proteção dos pés quanto a impactos e derramamentos de líquidos corrosivos
( ) Proteção quanto à manipulação de reagentes diversos
( ) Proteção quanto à manipulação de reagentes, equipamentos e procedimentos laboratoriais
A alternativa que contém a sequência correta dos números da coluna da direita, de cima para baixo, é:
Provas
Qualquer laboratório, principalmente de Química, pode se tornar em um local muito perigoso, quando se usa inadequadamente materiais e equipamentos. Nesse contexto, é importante o conhecimento de boas práticas de laboratório. Com relação a essas práticas, identifique se são verdadeiras (V) ou falsas (F) as seguintes afirmativas:
( ) No encerramento do expediente, não se deve deixar equipamentos elétricos ligados nas tomadas, sob hipótese alguma.
( ) Para exercer as atividades de laboratório é obrigatório o uso de guarda-pó, sapatos fechados e cabelos presos.
( ) Na bancada ou nos bancos, quando for o caso, pode-se colocar livros, sacolas, ferramentas etc.
( ) É proibido fumar no laboratório. Somente será permitido fumar na capela, onde a saúde dos usuários não será exposta a risco.
( ) Deve-se sempre manter os acessos desimpedidos,e o interior do laboratório limpo e organizado.
Assinale a alternativa que apresenta a sequência CORRETA, de cima para baixo:
Provas
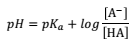
em que, o HA é o ácido e A– é a base conjugada.
Com base no exposto, identifique as afirmativas verdadeiras.
I. O pH da solução será igual ao pKa se a [A– ] for igual a [HA]
II. O pH tende a aumentar se a concentração a [A– ] for maior que [HA]
III. O pH tende a diminuir se a concentração a [A– ] for maior que [HA]
IV.O pH tende a aumentar se a concentração a [A– ] for menor que [HA]
V. O pH tende a diminuir se a concentração a [A– ] for menor que [HA]
Assinale a alternativa correta:
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Provas
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Provas
Caderno Container