Foram encontradas 50 questões.
Considere uma solução tampão preparada com 0,20 mol L−1
de amônia (NH3) e 0,20 mol L−1 de
cloreto de amônio (NH4Cl). Qual é o pH aproximado sabendo-se que a constante Kb é 2,0 × 10−5?
Provas
Questão presente nas seguintes provas
Considerando o equilíbrio de soluções aquosas, qual é o efeito da adição de acetato de sódio
(CH3COONa) a uma solução de ácido acético?
Provas
Questão presente nas seguintes provas
Qual das reações de soluções aquosas resultará em um composto pouco solúvel, ou na formação de
um precipitado?
Provas
Questão presente nas seguintes provas
Assinale a alternativa correta.
I. No ensino de Química, o conhecimento científico é fundamental para o professor transmitir conceitos e princípios químicos de forma precisa e atualizada.
II. As principais habilidades didáticas incluem: planejamento de aulas, comunicação eficaz, uso de recursos didáticos, avaliação e feedback, e capacidade de adaptar o ensino às necessidades dos alunos.
III. O conhecimento científico pode ser integrado à prática pedagógica por meio de atividades experimentais, discussões de casos, resolução de problemas, uso de tecnologias e recursos visuais.
IV. A experimentação não é fundamental no ensino de Química, pois os alunos não são capazes de compreender conceitos e princípios observando fenômenos químicos.
I. No ensino de Química, o conhecimento científico é fundamental para o professor transmitir conceitos e princípios químicos de forma precisa e atualizada.
II. As principais habilidades didáticas incluem: planejamento de aulas, comunicação eficaz, uso de recursos didáticos, avaliação e feedback, e capacidade de adaptar o ensino às necessidades dos alunos.
III. O conhecimento científico pode ser integrado à prática pedagógica por meio de atividades experimentais, discussões de casos, resolução de problemas, uso de tecnologias e recursos visuais.
IV. A experimentação não é fundamental no ensino de Química, pois os alunos não são capazes de compreender conceitos e princípios observando fenômenos químicos.
Provas
Questão presente nas seguintes provas
Assinale a alternativa correta.
I.Dmitri Mendeleev desenvolveu a tabela periódica moderna em 1869 contendo 63 elementos químicos.
II.A tabela de Mendeleev era organizada de acordo com a ordem alfabética dos nomes dos elementos.
III.Henry Moseley reorganizou a tabela periódica de acordo com o número atômico dos elementos.
IV.Os gases nobres foram descobertos e incorporados à tabela periódica entre 1892 e 1902.
I.Dmitri Mendeleev desenvolveu a tabela periódica moderna em 1869 contendo 63 elementos químicos.
II.A tabela de Mendeleev era organizada de acordo com a ordem alfabética dos nomes dos elementos.
III.Henry Moseley reorganizou a tabela periódica de acordo com o número atômico dos elementos.
IV.Os gases nobres foram descobertos e incorporados à tabela periódica entre 1892 e 1902.
Provas
Questão presente nas seguintes provas
Atualmente, a Tabela Periódica é organizada por:
Provas
Questão presente nas seguintes provas
Uma solução é preparada por dissolução de 3,42 g de sacarose em 100 g de água. Para a solução,
calcule a molalidade da solução.
Dado: massa molar da sacarose = 342 g mol–1
Dado: massa molar da sacarose = 342 g mol–1
Provas
Questão presente nas seguintes provas
Uma peça de ferro, com massa inicial de 9,70 g foi submetida a um processo de galvanização por
redução de íons Zn²⁺. A eletrólise ocorreu durante 1000 s, sob a passagem de 300 mA, em solução
contendo íons Zn²⁺. Ao final do processo, a massa da peça passou a 9,65 g. Qual é o rendimento
desta reação?
Dados: massa molar do zinco = 65,4 g mol–1; F = 96500 C mol–1
Dados: massa molar do zinco = 65,4 g mol–1; F = 96500 C mol–1
Provas
Questão presente nas seguintes provas
Qual é a massa de cobre sólido que pode ser obtida se uma solução contendo íons Cu2+ for
eletrolisada a 96,5 mA por 1000 s?
Dados: massa molar do cobre = 63,5 g mol–1; F = 96500 C mol–1
Dados: massa molar do cobre = 63,5 g mol–1; F = 96500 C mol–1
Provas
Questão presente nas seguintes provas
Uma reação química apresenta a seguinte equação de velocidade:
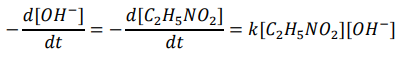
Experimentos a 0 °C com concentrações iniciais dos dois reagentes iguais a 0,01 mol L−1 forneceram um valor de 100 s para o tempo de meia-vida da reação. Qual é o valor da constante de velocidade a 0 °C?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container