Foram encontradas 65 questões.
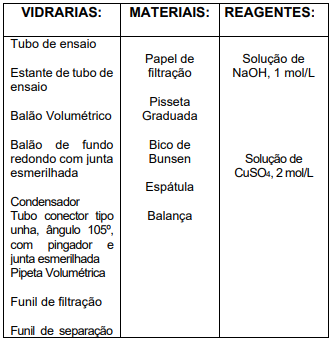
No preparo de uma aula prática de Química
Inorgânica, a professora precisou da seguinte lista
de materiais para seu procedimento experimental:
A proposta de aula é o estudo de reações químicas. A seguir, as reações propostas:
Os valores dos números de oxidação dos metais, nos produtos da primeira reação, e a classificação da segunda reação são, respectivamente

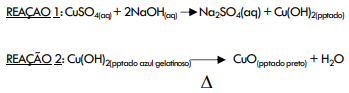
A proposta de aula é o estudo de reações químicas. A seguir, as reações propostas:

Os valores dos números de oxidação dos metais, nos produtos da primeira reação, e a classificação da segunda reação são, respectivamente
Provas
Questão presente nas seguintes provas
Uma das técnicas de separação mais
antigas e importantes na química é a
cromatografia. Existem diversos tipos de técnicas
cromatográficas, uma delas é cromatografia em
camada delgada (CCD) ou cromatografia em
camada fina (CCF), que poder ser utilizada para
separar misturas sobre uma tira de papel
(celulose), placa de vidro ou folha de alumínio.
Nesses dois últimos casos, as placas são cobertas
por uma camada bem fina de sílica-gel (SiO2) ou
alumina (Al2O3), a fase estacionária.
Após o spot ou aplicação do analito sobre a fase estacionária, esta é colocada para correr em uma cuba cromatográfica, a qual contém a fase móvel, uma mistura de solventes que irá carrear, por capilaridade, as substâncias presentes no analito, separando-as por diferença de polaridade.
A identificação das substâncias é feita calculando-se o fator de retenção, que corresponde à razão entre a distância percorrida por cada mancha e a distância percorrida pela fase móvel.
Analise as figuras a seguir, de uma amostra X e três substâncias padrões (Y, Z e W), antes e após a corrida cromatográfica:
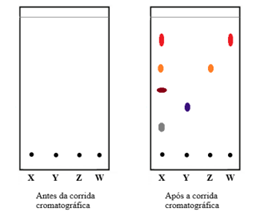
Analisando a corrida cromatográfica, identifique a opção correta:
Após o spot ou aplicação do analito sobre a fase estacionária, esta é colocada para correr em uma cuba cromatográfica, a qual contém a fase móvel, uma mistura de solventes que irá carrear, por capilaridade, as substâncias presentes no analito, separando-as por diferença de polaridade.
A identificação das substâncias é feita calculando-se o fator de retenção, que corresponde à razão entre a distância percorrida por cada mancha e a distância percorrida pela fase móvel.
Analise as figuras a seguir, de uma amostra X e três substâncias padrões (Y, Z e W), antes e após a corrida cromatográfica:

Analisando a corrida cromatográfica, identifique a opção correta:
Provas
Questão presente nas seguintes provas
Uma profissional em química, em sua
pesquisa investigativa de bancada, utilizou o
reagente 2,4-dinitro-fenil hidrazina para analisar
sua amostra orgânica, um líquido incolor de odor
intenso. Como resultado verificou a formação de
um precipitado laranja. Dando continuidade aos
testes de análise funcional, resolveu utilizar o
reagente de Tollens, e não verificou a formação do
espelho de prata.
Para concluir sua investigação, resolveu fazer uma análise de espectroscopia no Infravermelho (FTIR), obtendo-se o espectro a seguir:
A função orgânica da amostra analisada pela analista é
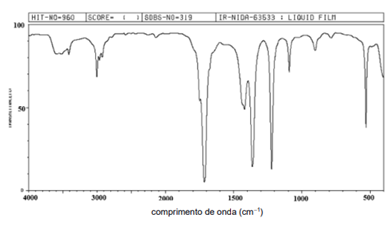
Para concluir sua investigação, resolveu fazer uma análise de espectroscopia no Infravermelho (FTIR), obtendo-se o espectro a seguir:

A função orgânica da amostra analisada pela analista é
Provas
Questão presente nas seguintes provas
Em análise orgânica, a marcha da
solubilidade é uma ferramenta muito importante
para a determinação da classe de compostos
orgânicos. Na investigação de uma amostra X, foi
testada sua solubilidade, e verificou-se que ela foi
solúvel em água e em éter etílico.
Com base nos seus conhecimentos de solubilidade, polaridade e a marcha de solubilidade, a estrutura mais provável para ser a amostra X é
Com base nos seus conhecimentos de solubilidade, polaridade e a marcha de solubilidade, a estrutura mais provável para ser a amostra X é
Provas
Questão presente nas seguintes provas
Decerto você já ouviu o seguinte enunciado:
“Na natureza, nada se cria, nada se perde, tudo se
transforma”, que se refere à Lei da Conservação
das Massas. Segundo esta Lei, em um ambiente
fechado, a massa total no início de uma reação
química é igual à massa total ao final desta, ou
seja, a massa se conserva porque não ocorre
criação nem destruição de átomos. Os átomos são
conservados, e se rearranjam. Os agregados
atômicos dos reagentes são desfeitos e novos
agregados atômicos são formados nos produtos".
Esta lei foi publicada pela primeira vez pelo russo
Mikhail Lomonosov, em 1760. Entretanto, sua
publicação não teve repercussão pela Europa. A
propagação desta lei só se deu pelo francês
Antoine Lavoisier, sendo hoje conhecida como Lei
de Lavoisier.
Analise a reação descrita a seguir, da produção de sulfeto ferroso, um sal presente na composição de diversos minerais, e de grande interesse comercial na indústria:
8 Fe (s) + 1 S8 (s) → 8 FeS (s)
Em um reator fechado, foram adicionados 5,60 kg de ferro metálico (Fe) e 4,0 kg de enxofre (S8). O valor da massa de sulfeto de ferro obtida, e a massa do reagente em excesso, se houver, serão, respectivamente:
Dados de M.A.: Fe: 56 g/mol / S: 32 g/mol
Analise a reação descrita a seguir, da produção de sulfeto ferroso, um sal presente na composição de diversos minerais, e de grande interesse comercial na indústria:
8 Fe (s) + 1 S8 (s) → 8 FeS (s)
Em um reator fechado, foram adicionados 5,60 kg de ferro metálico (Fe) e 4,0 kg de enxofre (S8). O valor da massa de sulfeto de ferro obtida, e a massa do reagente em excesso, se houver, serão, respectivamente:
Dados de M.A.: Fe: 56 g/mol / S: 32 g/mol
Provas
Questão presente nas seguintes provas
Um estudante do curso técnico em Química,
matriculado na disciplina de Química Analítica
Quantitativa I, verifica que são necessários 20 mL
de uma solução de hidróxido de potássio, na
concentração de 0,4 mol/L, para neutralizar
completamente 50 mL de uma amostra de ácido
clorídrico. Dessa forma, e seguindo os cálculos do
estudante, a concentração molar do ácido em
questão será de
Provas
Questão presente nas seguintes provas
A titulação “Análise Volumétrica ou
Titrimetria” é uma técnica amplamente utilizada
nos laboratórios de química analítica, a fim de
determinar a concentração desconhecida de
determinada espécie em uma amostra em
análise. No procedimento experimental, trata-se
da adição paulatina de uma solução padrão,
denominada reagente titulante de concentração
conhecida, à amostra em análise. Dessa maneira,
pretende-se reagir completamente o analito, ou
seja, a substância de concentração desconhecida,
a fim de determinar sua concentração.
Num laboratório de pesquisa de uma universidade, há um frasco de hidróxido de sódio dentro da capela, cujo rótulo já está bastante desgastado, de modo que não é possível ler sua concentração. Com o intuito de calcular sua concentração, utilizaram-se 5 mL dessa base, tendo como titulante o ácido sulfúrico, na concentração 0,20 mol/L. Após a titulação, verificou-se que o volume total do ácido gasto foi de 12,5 mL.
A concentração da solução alcalina no frasco é de
Num laboratório de pesquisa de uma universidade, há um frasco de hidróxido de sódio dentro da capela, cujo rótulo já está bastante desgastado, de modo que não é possível ler sua concentração. Com o intuito de calcular sua concentração, utilizaram-se 5 mL dessa base, tendo como titulante o ácido sulfúrico, na concentração 0,20 mol/L. Após a titulação, verificou-se que o volume total do ácido gasto foi de 12,5 mL.
A concentração da solução alcalina no frasco é de
Provas
Questão presente nas seguintes provas
Os sulfetos apresentam valores de
solubilidade, em água, que variam de mais de cem
ordens de grandeza: enquanto o sulfeto de sódio,
Na2S, é extremamente solúvel, o produto de
solubilidade do sulfeto de bismuto, Bi2S3, é
1,0 x 10-96
, extremamente insolúvel.
Tabelas de regras de solubilidade normalmente encontradas em livros textos, trazem os sulfetos como compostos insolúveis, exceto os sulfetos dos íons NH4+ , Ca2+, Sr2+ e dos metais alcalinos. A insolubilidade de muitos sulfetos é uma propriedade importante que permite a separação dos mesmos em diversos processos. Assim, por formar compostos insolúveis mesmo em meio ácido, com vários metais, a precipitação dos sulfetos é usada na “inativação” destes (por exemplo: mercúrio, chumbo, cobre). Um dos métodos para fabricação do sulfeto de sódio, substância inorgânica que atingiu importante papel na indústria da química orgânica, envolve duas etapas, como descrito nas reações abaixo:
Reação 1: H2S + NaOH → NaHS + H2O
Reação 2: NaHS + NaOH → Na2S + H2O
Martins, C. R.; Silva, L. A.; Andrade, J. B. SULFETOS: POR QUE NEM TODOS SÃO INSOLÚVEIS? Quim. Nova, Vol. 33, No. 10, 2283-2286, 2010
Em um procedimento experimental, colocaram-se para reagir 680 gramas de ácido sulfídrico, com 880 gramas de soda cáustica, obtendo-se um rendimento de 80% de NaHS. Admitindo-se que o rendimento do sal na segunda reação foi de 75%, a massa de sulfeto de sódio obtida foi de
Tabelas de regras de solubilidade normalmente encontradas em livros textos, trazem os sulfetos como compostos insolúveis, exceto os sulfetos dos íons NH4+ , Ca2+, Sr2+ e dos metais alcalinos. A insolubilidade de muitos sulfetos é uma propriedade importante que permite a separação dos mesmos em diversos processos. Assim, por formar compostos insolúveis mesmo em meio ácido, com vários metais, a precipitação dos sulfetos é usada na “inativação” destes (por exemplo: mercúrio, chumbo, cobre). Um dos métodos para fabricação do sulfeto de sódio, substância inorgânica que atingiu importante papel na indústria da química orgânica, envolve duas etapas, como descrito nas reações abaixo:
Reação 1: H2S + NaOH → NaHS + H2O
Reação 2: NaHS + NaOH → Na2S + H2O
Martins, C. R.; Silva, L. A.; Andrade, J. B. SULFETOS: POR QUE NEM TODOS SÃO INSOLÚVEIS? Quim. Nova, Vol. 33, No. 10, 2283-2286, 2010
Em um procedimento experimental, colocaram-se para reagir 680 gramas de ácido sulfídrico, com 880 gramas de soda cáustica, obtendo-se um rendimento de 80% de NaHS. Admitindo-se que o rendimento do sal na segunda reação foi de 75%, a massa de sulfeto de sódio obtida foi de
Provas
Questão presente nas seguintes provas
O texto do experimento que segue é referente à questão.
A fim de mostrar aos seus estudantes os
conteúdos Funções e Reações Inorgânicas, uma
professora adicionou a um kitassato 15g de
carbonato de cálcio, e a este acoplou com uma
rolha de cortiça, um funil de decantação contendo
100 mL de ácido clorídrico concentrado conforme
a figura abaixo:
Provas
Questão presente nas seguintes provas
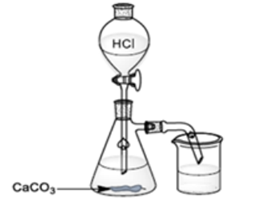
O texto do experimento que segue é referente à questão.
A fim de mostrar aos seus estudantes os
conteúdos Funções e Reações Inorgânicas, uma
professora adicionou a um kitassato 15g de
carbonato de cálcio, e a este acoplou com uma
rolha de cortiça, um funil de decantação contendo
100 mL de ácido clorídrico concentrado conforme
a figura abaixo:

Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container