Foram encontradas 300 questões.
Considere uma base forte e solúvel em água, hipotética, com massa molar de 44 g/mol e fórmula T(OH)3. O preparo de uma solução de concentração 0,01 mol/L de T(OH)3 resultará no valor de pH, aproximadamente, de
Dados: log 2 = 0,30, log 3 = 0,48, log 5 = 0,70.
Provas
Considere a meia-reação de oxidação:
Br- + 60H- → BrO3- + 3H2O + 6e-
Com base na equação química fornecida, o número de oxidação (NOX) do bromo, em BrO3-, é igual a
Provas
Observe a reação de adição eletrofílica entre os compostos a seguir.
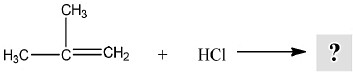
Considerando a estrutura química dos compostos fornecidos e as propriedades das reações de adição eletrofílica, o composto formado por essa reação será um
Provas
Considere os utensílios a seguir, utilizados na destilação fracionada.
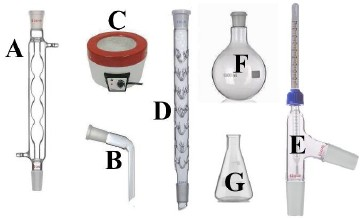
Diante desses utensílios, demarcados com letras, assinale a alternativa que mostra a ordem de montagem correta do sistema de destilação fracionada.
Provas
Avalie a estrutura química a seguir.
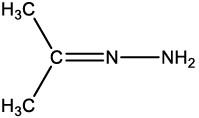
Diante dessa estrutura, assinale a alternativa que apresenta o número de átomos com hibridização sp3 e a identidade desses átomos, respectivamente.
Provas
Considere a seguinte equação química, não balanceada:
Fe2O3(s) + CO(g) → Fe(s) + CO2(g)
Assinale a alternativa que contém a massa aproximada de óxido de ferro (III) necessária para produzir 9,0 g de ferro metálico.
Dados: Fe = 56 g/mol e Fe2O3 = 160 g/mol.
Provas
Observe a seguinte estrutura química do neurotransmissor adrenalina:
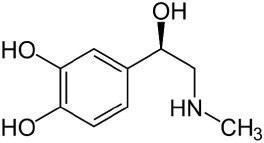
Sabendo que as massas molares dos elementos são: O = 16 g/mol, H = 1 g/mol, C = 12 g/mol e N = 14 g/mol, pode-se afirmar que a massa molar da molécula de adrenalina é igual a
Provas
Considere uma solução aquosa contendo um ácido hipotético, de fórmula química H3X, com concentração de 0,02 mol/L. Tendo em vista que se trata de um ácido forte, o pH dessa solução será, aproximadamente, igual a
Dados: log 2 = 0,30, log 3 = 0,48, log 5 = 0,70, log 6 = 0,78.
Provas
Considere a seguinte reação química, não balanceada, em equilíbrio químico, a 1000K:
SO2(g) + O2(g) ⇌ SO3(g)
Levando em conta os valores de pressão parcial de SO2 = 0,7 bar, SO3 = 0,08 bar e O2 = 0,40 bar, pode-se afirmar que o valor da constante de equilíbrio (Kp), na temperatura de 1000 K, será, aproximadamente, igual a
Provas
Considere os seguintes ácidos e seus respectivos valores de constantes de ionização (pKa).
| Ácidos | pKa |
| Ácido tricloro-acético | 0,52 |
| Ácido benzenossulfônico | 0,70 |
| Ácido sulfuroso | 1,81 |
| Ácido cloroso | 2,00 |
| Ácido nitroso | 3,37 |
Em relação às informações constantes nessa tabela, pode-se afirmar que a substância mais ácida é o
Provas
Caderno Container