Foram encontradas 50 questões.
Permanganato de potássio (KMnO4) em meio ácido é um oxidante muito utilizado em laboratórios. Nessas reações, o manganês é, tipicamente, reduzido ao estado de oxidação +2. Considerando uma reação que procede quantitativamente, quantos mols de Fe2+ podem ser oxidados a Fe3+ por um mol de KMnO4?
Provas
Quando adicionada a água pura (pH = 7), a substância capaz de produzir uma solução ácida é
Provas
Observe a figura abaixo.
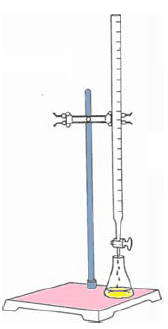
O aparato mostrado na figura é tipicamente usado em laboratório para
Provas
Um sistema de destilação simples é indicado para a separação de
Provas
Um determinado solvente orgânico foi submetido aos seguintes testes:
i) Solubilidade em água: muito solúvel.
ii) Reação frente a uma solução ácida de dicromato (ác. crômico): reativo.
iii) Reação frente a uma solução básica de I2: reativo, formando precipitado.
Com estes testes, o solvente é um(a)
Provas
Para se medir um volume de 15,30 mL de um solvente, com incerteza de 0,01 mL, a vidraria mais adequada é um(a)
Provas
A tabela abaixo apresenta os valores de Ka de cinco ácidos fracos, a 25 ºC.
|
Ácido |
Ka |
|
Fórmico |
1,6 × 10−4 |
|
Acético |
1,7 × 10−5 |
|
Benzoico |
6,3 × 10−5 |
|
Hipocloroso |
3,6 × 10−8 |
|
Nitroso |
4,7 × 10−11 |
Se uma solução aquosa (a 25 ºC) 0,10 M de um determinado ácido fraco monoprótico contém [H3O+] igual a 2,5 × 10−3 M, a solução é formada pelo ácido
Provas
Observe a reação dada abaixo.
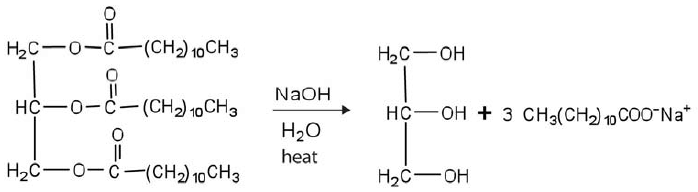
Para essa reação, são feitas as seguintes afirmações:
i) Trata-se de uma reação para a produção biodiesel.
ii) O reagente é um éster.
iii) É uma reação de saponificação.
iv) Um dos produtos da reação é um aldeído
Dentre as afirmações apresentadas, estão corretas apenas
Provas
Uma amostra de água dura contém 120 mg de CaCO3 por litro de água. Considerando que a reação com Na3PO4 promove a precipitação quantitativa dos íons Ca2+, a massa, em gramas, de Na3PO4 necessária para precipitar todos os íons Ca2+ de dois litros dessa água dura é de aproximadamente
Provas
Uma solução de 1,020 g de hidrogenoftalato de potássio (“KHF”) dissolvido em 20 mL de água foi utilizada na padronização de uma solução de hidróxido de sódio. A titulação do padrão consumiu, até atingir o ponto de equivalência, 8,7 mL da solução de NaOH. Assim, a molaridade da solução de NaOH utilizada é de aproximadamente
Provas
Caderno Container