Foram encontradas 40 questões.
Quando dois ou mais compostos, orgânicos ou inorgânicos, têm a mesma composição, mas um arranjo atômico diferente,
esses compostos são denominados isômeros. No que diz respeito à possibilidade de isomerismo em complexos
octaédricos de cobalto, identifique como verdadeiras (V) ou falsas (F) as seguintes afirmativas:
(en = etilenodiamina, H
2
N-CH
2
-CH
2
-NH
2
)
( ) [Co(en) 3 ] 3+ apresenta isomerismo ótico.
( ) trans -[Co(en) 2 Cl 2 ] + apresenta isomerismo ótico.
( ) [Co(NH 3 ) 4 Cl 2 ] + apresenta isomerismo geométrico.
( ) [Co(NH 3 ) 5 NO 2 ] 2+ apresenta isomerismo de ligação.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
( ) [Co(en) 3 ] 3+ apresenta isomerismo ótico.
( ) trans -[Co(en) 2 Cl 2 ] + apresenta isomerismo ótico.
( ) [Co(NH 3 ) 4 Cl 2 ] + apresenta isomerismo geométrico.
( ) [Co(NH 3 ) 5 NO 2 ] 2+ apresenta isomerismo de ligação.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
Provas
Questão presente nas seguintes provas
A fórmula química de um composto representa sua composição em termos de símbolos químicos dos elementos que
compõem uma determinada substância. A xantofila, uma substância encontrada em penas de aves e em flores, contém
átomos de carbono, hidrogênio e oxigênio na razão 20:28:1. Sabendo que uma molécula desse composto tem seis átomos
de oxigênio, qual é a fórmula química da xantofila?
Provas
Questão presente nas seguintes provas
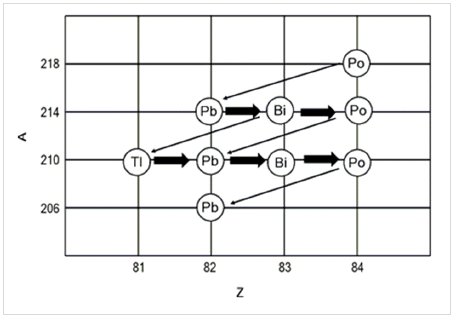
Alguns núcleos são instáveis e tendem a sofrer
decaimento até que um núcleo mais estável seja
formado. Esses núcleos decaem uma série de
etapas e dão origem a uma série radioativa. Na
figura a seguir, está mostrado o decaimento do
218
Po até
206
Pb.
Com relação a decaimento, considere as seguintes equações:
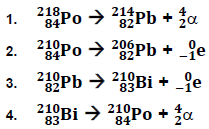
São equações de decaimento:
Com relação a decaimento, considere as seguintes equações:
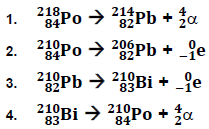

São equações de decaimento:
Provas
Questão presente nas seguintes provas
A fermentação da glicose (C
6
H
12
O
6
) produz etanol (C
2
H
6
O) e dióxido de carbono (CO
2
), conforme a equação química não
balanceada abaixo:
C 6 H 12 O 6(aq) → C 2 H 6 O (aq) + CO 2(g)
(Massas molares (g mol -1 ): C = 12; H = 1; O = 16)
Qual é a massa, em gramas, de CO 2 produzida quando 0,400 mol de glicose reage dessa maneira?
C 6 H 12 O 6(aq) → C 2 H 6 O (aq) + CO 2(g)
(Massas molares (g mol -1 ): C = 12; H = 1; O = 16)
Qual é a massa, em gramas, de CO 2 produzida quando 0,400 mol de glicose reage dessa maneira?
Provas
Questão presente nas seguintes provas
Equilíbrios químicos são fenômenos comuns às reações químicas. Em poucas palavras, numa reação que tende ou que
já atingiu o equilíbrio, os reagentes se convertem em produtos e os produtos regeneram os reagentes, sendo que a
posição equilíbrio pode ser determinada a partir da constante de equilíbrio (K
eq
), que leva em consideração a
concentração, no equilíbrio, das espécies envolvidas. Considere que uma reação química genérica atingiu o equilíbrio
químico e que a equação da constante de equilíbrio dessa reação é a apresentada a seguir:

Assumindo que as equações acima são modelos que podem ser aplicados a qualquer reação química, é correto afirmar que, no equilíbrio:
1. as concentrações de A, B, C e D são iguais. 2. as concentrações de A, B, C e D não se alteram com o tempo. 3. a reação para de acontecer, logo, a formação de produtos é interrompida. 4. a constante de velocidade da reação direta (k1) é igual à da reação inversa (k -1 ).
Assinale a alternativa correta.

Assumindo que as equações acima são modelos que podem ser aplicados a qualquer reação química, é correto afirmar que, no equilíbrio:
1. as concentrações de A, B, C e D são iguais. 2. as concentrações de A, B, C e D não se alteram com o tempo. 3. a reação para de acontecer, logo, a formação de produtos é interrompida. 4. a constante de velocidade da reação direta (k1) é igual à da reação inversa (k -1 ).
Assinale a alternativa correta.
Provas
Questão presente nas seguintes provas
Considere os seguintes aminoácidos:
(Números atômicos: H = 1; C = 6; N = 7; O = 8; S = 16).
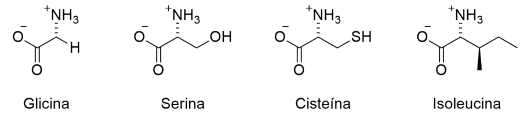
( ) A glicina é aquiral.
( ) A configuração absoluta da serina é R .
( ) A configuração absoluta da cisteína é R .
( ) A isoleucina tem um estereoisômero meso.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Heterogêneos: Produto de Solubilidade (Kps)
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Qual é a massa, em gramas, de NaCl necessária para precipitar todos os íons prata presentes em 15,0 mL de solução de
0,125 mol L
-1
de AgNO
3
?
(Massas molares (g mol
-1
): Na = 23; Cl = 35,5; Ag = 108; N = 14; O = 16)
Provas
Questão presente nas seguintes provas
Soluções aquosas que contêm um par ácido-base conjugado fraco podem resistir drasticamente às variações de
pH com a adição de pequenas quantidades de ácido ou base forte. Elas são chamadas de soluções-tampão (ou
simplesmente tampão). Nesse sentido, qual é a quantidade de matéria, em mol, de NH
4
Cl que deve ser adicionada
a 2,0 L de 0,10 mol L
-1
de NH
3
para formar um tampão cujo pH é 9,00? Suponha que a adição de NH
4
Cl não altere o
volume da solução.
(Dados: K
b
= 1,8 x 10
-5
; pOH = 14,00 – pH)
Provas
Questão presente nas seguintes provas
A diferença de potencial entre dois eletrodos em uma célula voltaica fornece a força eletromotriz que empurra os elétrons
por um circuito externo. Para uma pilha, essa força é denominada
potencial da célula
(E). Sob condições-padrão
(concentração das soluções de 1 mol L
-1
, pressão 1 atm e 25 ºC), tem-se o potencial-padrão da célula (Eº
célula
), que pode
ser determinado pela diferença dos potenciais-padrão de redução das reações que acontecem no catodo (Eº
catodo
) e anodo
(Eº
anodo
). Sabendo que os Eº das células voltaicas Zn-Cu
2+
, Ni-Cu
2+
e Zn-Fe
2+
são +1,10, +0,62 e +0,32 V, respectivamente,
assinale a alternativa que apresenta o Eº da célula voltaica Fe-Ni
2+
.
(Ordem dos Eº: Cu
2+
>Ni
2+
>Fe
2+
>Zn
2+
; Fe
2+
(aq) + 2e
-
→
Fe(s) Eº = -0,44 V).
Provas
Questão presente nas seguintes provas
A concentração dos vapores oriundos de uma solução ideal contendo dois ou mais componentes voláteis pode ser
diferente das concentrações dos componentes em solução. Assim, as pressões parciais dos vapores acima da solução
serão dadas pela Lei de Raoult, e a pressão vapor total (P
total
) será a soma das pressões parciais de cada componente.
Considere como ideal uma mistura a 20 ºC contendo 1,0 mol de benzeno (Pº = 75 torr) e 2,0 mols de tolueno (Pº = 22 torr).
Qual é a pressão de vapor total, em torr, sobre essa solução?
(PA = X
A
Pº
A
; X = fração molar; Pº = pressão de vapor do componente puro)
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container