Foram encontradas 40 questões.
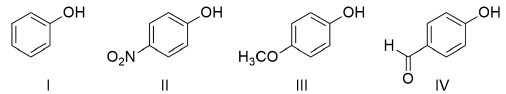
Considere os seguintes fenóis:
Provas
Questão presente nas seguintes provas
Os ácidos e bases são importantes em diversos processos químicos que ocorrem ao nosso redor, desde os industriais
até os biológicos. Essas substâncias foram primeiro identificadas pelas propriedades de suas soluções aquosas.

Considerando a dissociação de um ácido genérico (HA) em água, conforme a equação mostrada acima, identifique como verdadeiras (V) ou falsas (F) as seguintes afirmativas:
( ) Se HA = HCl, ele estará completamente dissociado e a [H 3 O + ] = [HCl] inicial .
( ) HA é o ácido conjugado da H 2 O enquanto H 3 O + é o ácido conjugado de A - .
( ) HA é um ácido de Bronsted-Lowry e H 2 O é uma base de Bronsted-Lowry.
( ) Se HA = ácido acético, ele estará completamente dissociado e a [H 3 O + ] = [ácido acético] inicial .
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
Considerando a dissociação de um ácido genérico (HA) em água, conforme a equação mostrada acima, identifique como verdadeiras (V) ou falsas (F) as seguintes afirmativas:
( ) Se HA = HCl, ele estará completamente dissociado e a [H 3 O + ] = [HCl] inicial .
( ) HA é o ácido conjugado da H 2 O enquanto H 3 O + é o ácido conjugado de A - .
( ) HA é um ácido de Bronsted-Lowry e H 2 O é uma base de Bronsted-Lowry.
( ) Se HA = ácido acético, ele estará completamente dissociado e a [H 3 O + ] = [ácido acético] inicial .
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma solução foi preparada pela dissolução de 500 mg de cloreto de potássio, 500 mg de sulfeto de potássio e 500 mg de
fosfato de potássio em 500 mL de água. Qual é a concentração final, em mol L
-1
, de íons potássio em solução?
(Massas
molares (g mol
-1
): O = 16; P = 31; S = 32; Cl = 35,5; K = 39,1)
Provas
Questão presente nas seguintes provas
Considere a reação ácido-base entre amônia e água mostrada a seguir:
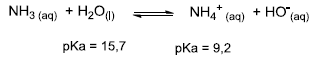
( ) A constante de basicidade da reação será K b = [NH 4 + ][HO - ]/[NH 3 ].
( ) A adição de NH 4 Cl deslocará o equilíbrio no sentido dos produtos.
( ) A água é um ácido mais fraco do que o íon amônio (NH 4 + ), e o equilíbrio está deslocado no sentido dos reagentes.
( ) A amônia (NH 3 ) é uma base mais forte do que o íon hidróxido, e o equilíbrio da reação está deslocado no sentido dos reagentes.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
Provas
Questão presente nas seguintes provas
A energia livre de Gibbs (G) é uma função de estado termodinâmica que combina as duas funções de estado, entalpia (H)
e entropia (S). Para processos que ocorrem a temperatura constante, tem-se que ∆G = ∆H – T∆S. Para um processo ou
reação ocorrendo a temperatura e pressão constantes, o sinal de ∆G relaciona-se à espontaneidade do processo. Nesse
sentido, sobre a termodinâmica das reações químicas, identifique como verdadeiras (V) ou falsas (F) as seguintes
afirmativas:
( ) Se Δ G = 0, a reação não ocorre.
( ) Uma reação espontânea ocorre em qualquer sentido (direto e indireto).
( ) Se Δ G < 0, a reação é espontânea no sentido direto (reagentes → produtos).
( ) Se Δ G > 0, a reação é espontânea no sentido indireto (produtos → reagentes).
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
( ) Se Δ G = 0, a reação não ocorre.
( ) Uma reação espontânea ocorre em qualquer sentido (direto e indireto).
( ) Se Δ G < 0, a reação é espontânea no sentido direto (reagentes → produtos).
( ) Se Δ G > 0, a reação é espontânea no sentido indireto (produtos → reagentes).
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
Provas
Questão presente nas seguintes provas
Qual é o pH de uma solução-tampão preparada pela adição de 0,060 mol de ácido lático e 0,050 mol de lactato de sódio
em 500 mL de água?
(Informações adicionais: pH = pKa + log [A
-
]/[HA]; - log Ka = 3,85; log 0,83 = -0,08; log 1,2 = +0,08; log 1 = 0)
Provas
Questão presente nas seguintes provas
Muitos dos estudos sobre as reações químicas dizem respeito à rapidez com que elas ocorrem. As velocidades de reação
variam desde aquelas que ocorrem em frações de segundos até aquelas que levam milhões de anos para acontecer. Com
base nisso, considere os dados de cinética química para a reação abaixo:
A + 3B → 2C + D
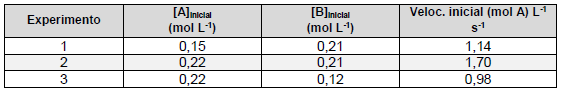
A partir dessas informações, considere as seguintes afirmativas:
1. A reação é de primeira ordem em relação ao reagente A, e também de primeira ordem em relação ao reagente B. 2. A lei de velocidade da reação, baseada na estequiometria da reação, é velocidade = k [A][B] 3 , e a ordem global da reação é 4. 3. A lei de velocidade da reação, baseada nos dados experimentais, é velocidade = k [A][B], e a ordem global da reação é 2. 4. O valor de k para o experimento 2 é 36,79 L mol -1 s -1 .
Assinale a alternativa correta.
A + 3B → 2C + D

A partir dessas informações, considere as seguintes afirmativas:
1. A reação é de primeira ordem em relação ao reagente A, e também de primeira ordem em relação ao reagente B. 2. A lei de velocidade da reação, baseada na estequiometria da reação, é velocidade = k [A][B] 3 , e a ordem global da reação é 4. 3. A lei de velocidade da reação, baseada nos dados experimentais, é velocidade = k [A][B], e a ordem global da reação é 2. 4. O valor de k para o experimento 2 é 36,79 L mol -1 s -1 .
Assinale a alternativa correta.
Provas
Questão presente nas seguintes provas
Em dias muito frios, é comum que encanamentos de água se rompam devido ao processo de congelamento. Esse
fenômeno é atribuído ao fato de a água se expandir ao congelar. Quanto trabalho, em joules, uma amostra de 100 g de
água realiza ao congelar em 0 ºC e estourar um cano de água que exerce uma pressão oposta de 1,070 atm?
(As densidades da água e do gelo, em 0 ºC, são 1,00 e 0,92 g cm
-3
, respectivamente.
w
= - P
ext
∆V; 1 L atm = 101,325 J)
Provas
Questão presente nas seguintes provas
Uma vez que entalpia (H) é uma função de estado, ∆H depende apenas dos estados inicial e final do sistema. A variação
de entalpia de um processo é a mesma se o processo for realizado em uma etapa ou em uma série de etapas. Com base
nisso, considere a transformação do carbono grafita em carbono diamante. Sabendo que a entalpia de combustão da
grafita é -393,5 kJ mol
-1
, e que a entalpia de combustão do diamante é -395,4 kJ mol
-1
, qual é a entalpia de conversão, em
kJ mol
-1
, de 2 mols de grafita em diamante?
Provas
Questão presente nas seguintes provas
Sobre a organização da Administração Pública na Constituição brasileira, assinale a alternativa correta.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container