Foram encontradas 20 questões.
Existem vários tipos de sólidos que diferem pela natureza da força que agrega suas partículas. Pode-se dizer que no iodo sólido as moléculas são mantidas unidas entre si por , na sílica existe entre os átomos de silício e oxigênio e no iodeto de potássio a força é de natureza . Entre os líquidos, ocorre diferença de polaridade. No álcool metílico existem interações do tipo , enquanto no éter metílico as interações são do tipo . Em contrapartida, nos gases, a interação entre partículas somente se torna importante em condições de pressão.
Assinale a alternativa que preenche, correta e respectivamente, as lacunas do parágrafo acima.
Provas
Questão presente nas seguintes provas
Deseja-se preparar 50 mL de uma solução aquosa de amônia na concentração 6,4 mol/L. Encontra-se disponível no laboratório uma solução de amônia 30% em massa e com densidade 0,91 g/mL. Pode-se afirmar que a concentração molar aproximada da solução de amônia disponível e o volume aproximado desta solução necessário para preparar a solução desejada são, respectivamente,
Provas
Questão presente nas seguintes provas
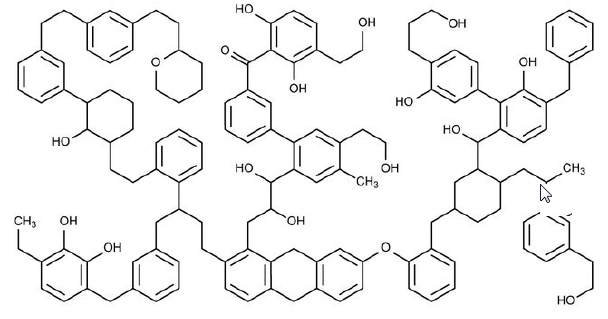
Na molécula C142H156O17 abaixo, quais funções orgânicas podem ser identificadas?
Provas
Questão presente nas seguintes provas
Um aluno de pós-graduação tem como tarefa estudar a seguinte reação química:
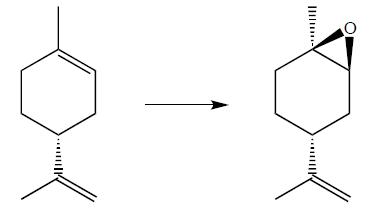
Para quantificar seus resultados, a técnica adequada a usar é a
Provas
Questão presente nas seguintes provas
Cada espécie química é capaz de absorver a radiação eletromagnética em frequências características. A lei de absorção (Lei de Beer) informa como a quantidade de luz absorvida depende da concentração do analito e da extensão do caminho ótico. Uma solução 1,0x10-4 mol/L de um determinado analito apresenta uma transmitância de 10% quando medida em uma célula de 2 cm de caminho ótico e no comprimento de 585 nm. Pode-se afirmar que a absorbância (A) dessa solução é de e a absortividade molar do analito é de L.mol-1.cm-1.
Assinale a alternativa que preenche, correta e respectivamente, as lacunas do parágrafo acima.
Provas
Questão presente nas seguintes provas
Foram misturados volumes iguais de Cu(NO3)2 0,040 mol/L e NaI 0,040 mol/L. Sabendo-se que o Kps do CuI2 é 1x10-12, pode-se afirmar que as concentrações finais dos íons Na+, Cu2+, NO3 - e I- são, respectivamente,
Provas
Questão presente nas seguintes provas
Quando dois átomos compartilham , produz-se entre os dois uma ligação . Essa união, que se verifica entre átomos de natureza semelhante, é a mais comum nos . O que participa da ligação pode ficar mais próximo do átomo que exerça sobre ele força de atração. Essa ligação, chamada , forma um pequeno dipolo elétrico, embora a molécula, no conjunto, possa ser apolar.
Assinale a alternativa que preenche, correta e respectivamente, as lacunas do parágrafo acima.
Provas
Questão presente nas seguintes provas
Alumínio metálico reage com ácido sulfúrico formando sulfato de alumínio e hidrogênio gasoso. O volume aproximado de ácido sulfúrico 7,0 mol/L necessário para reagir completamente com uma amostra de 6,0 gramas de alumínio contendo 10% de impurezas é de . Sabendo-se que a solução 7,0 mol/L tem uma densidade de 1,40 g/mL, pode-se afirmar que a porcentagem em massa de ácido sulfúrico nesta solução é de .
Assinale a alternativa que preenche, correta e respectivamente, as lacunas do parágrafo acima.
Provas
Questão presente nas seguintes provas
A correta reação de formação de CO2 nas condições padrão, de acordo com a Termodinâmica, é:
Provas
Questão presente nas seguintes provas
Considere as afirmativas abaixo.
I - Quando uma amostra contendo ferro é dissolvida, a solução resultante normalmente contém uma mistura de Fe(II) e Fe(III). Portanto, se for utilizado um oxidante padrão para determinar o ferro, primeiro será preciso tratar a solução com um agente redutor auxiliar.
II - O cromato de sódio pode servir como indicador nas determinações argentométricas de alguns haletos (método de Mohr), mas, com a descoberta do caráter carcinogênico do Cr(VI), o método de Volhard, que utiliza Fe(III) como indicador, passou a ser mais empregado.
III - Em água, o cromo pode existir na forma trivalente (não tóxica) e hexavalente (tóxica). Um dos métodos mais conhecidos para determinar seletivamente o Cr(VI) envolve a reação de redução da difenilcarbazida pelo Cr(VI).
IV - O nitrato de prata é o reagente dos métodos argentométricos utilizados na determinação de haletos. Nestes métodos os cátions prata se reduzem a prata metálica ao oxidarem os ânions dos haletos, e os cátions prata em excesso podem ser retrotitulados com KSCN.
Quais estão corretas?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container